下列有关金属腐蚀与保护的说法正确的是
| A.钢铁在潮湿空气中发生吸氧腐蚀,负极反应为Fe-3e-===Fe3+ |
| B.相同条件下,轮船在海水中比在淡水中腐蚀慢 |
| C.铁上镀锌的保护方法叫牺牲负极的正极保护法 |
| D.水库里钢闸门与电源负极相连的方法叫做外加电流的阴极保护法 |
化学与生产生活实际密切联系。下列说法不正确的是
| A.氢能可再生,没有污染,现已用作火箭和燃料电池的燃料 |
| B.在环保领域,酸性或碱性废水的处理常常利用中和反应 |
| C.为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术 |
| D.保护轮船船体,多采用外加电流的阴极保护法 |
下列与金属腐蚀有关的说法,正确的是 
| A.图1中,铁钉易被腐蚀 |
| B.图2中,滴加少量KSCN溶液,溶液变为血红色 |
| C.图3中,燃气灶的中心部位容易生锈,主要是由于高温下铁发生化学腐蚀 |
| D.图4中, 用牺牲镁块的方法来防止地下钢铁管道的腐蚀,镁块相当于原电池的正极 |
化学品船是建造或改装用于运载各种有毒、易燃、易挥发或有腐蚀性的化学物质的货船,下列说法错误的是
| A.在船舶的底部四周镶嵌铜块以保护船体 |
| B.不锈钢船舱可储藏运输散装氢氧化钠溶液 |
| C.甲醇与浓硫酸必须分开储藏运输 |
| D.造船焊接钢板时可用二氧化碳保护气 |
钢铁发生腐蚀时,正极上发生的反应是
| A.2Fe-4e— =2Fe2+ | B.2Fe2++4e— =2Fe |
| C.2H2O+O2+4e—=4OH— | D.Fe3++e—=Fe2+ |
下列叙述正确的是
| A.合成氨工业中,移走NH3可增大正反应速率,提高原料转化率 |
| B.酸碱中和滴定时,锥形瓶需用待测液润洗2次,再加入待测液 |
| C.将NO2、N2O4混合气体的体积压缩为原来的一半,则气体颜色加深 |
| D.牺牲阳极的阴极保护法和外加直流电的阴极保护法都是应用电解原理 |
5.下列有关钢铁腐蚀与防护的说法不正确的是
| A.生铁比纯铁容易生锈 |
| B.钢铁的腐蚀生成疏松氧化膜,不能保护内层金属 |
| C.钢铁发生吸氧腐蚀时,正极反应式为:O2+2H2O+4e-== 4OH- |
| D.为保护地下钢管不受腐蚀,可使其与直流电源正极相连 |
7.下列事实中,与电化学腐蚀无关的是
| A.埋在潮湿土壤里的铁管比埋在干燥土壤里的铁管更易被腐蚀 |
| B.为保护海轮的船壳,常在船壳上镶入锌块 |
| C.在空气中,金属银的表面生成一层黑色物质 |
| D.镀银铁制品,镀层部分受损后,露出的铁表面易被腐蚀 |
下列有关说法正确的是
| A.钢铁的腐蚀过程中,析氢腐蚀与吸氧腐蚀不可能同时发生 |
| B.反应NH4Cl(s)=NH3(g)+HCl(g)在室温下不能自发进行,则该反应的ΔH>0 |
| C.由于Ksp(BaSO4)<Ksp(BaCO3),因此BaSO4沉淀不可能转化为BaCO3 沉淀 |
| D.25℃时,0.1 mol·L-1CH3COOH溶液加水稀释后,c(OH-)/c(CH3COOH)增大 |
下列有关说法正确的是
| A.因为合金在潮湿的空气中易形成原电池,所以合金耐腐蚀性都较差 |
| B.常温下,MgO(s)+C(s)=Mg(s)+CO(g)不能自发进行,则其△H>0 |
| C.在NaCl和KBr的混合溶液中滴加AgNO3溶液,一定先产生淡黄色沉淀 |
| D.加热0.1 mol·L-1Al2(SO4)3溶液,水解程度增大、溶液的酸性增强 |
下列说法正确的是
| A.将高温水蒸气通过炽热的铁粉,铁粉变红色 |
| B.向Fe(OH)3胶体中滴加稀H2SO4,先出现沉淀,后沉淀溶解 |
| C.将市售食盐溶于水,滴加淀粉溶液不变蓝色,说明不是加碘盐 |
| D.Cu的金属活泼性比Fe弱,故水库铁闸门上接装铜块可减缓铁腐蚀 |
下列叙述正确的是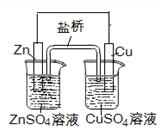
| A.电镀时,通常把待镀的金属制品作阳极 |
| B.上图Zn为负极,发生还原反应 |
| C.上图电子由Zn电极流向Cu电极,盐桥中的Cl-移向CuSO4溶液 |
| D.氢氧燃料电池(酸性电解质)中O2通入正极,电极反应为:O2+4H++4e-= 2H2O |
下列措施不合理的是
| A.久置不用的刀具涂抹凡士林后放于干燥处 |
| B.医用洒精的浓度越大,其杀菌效果越好 |
| C.高温下用焦炭还原SiO2制取粗硅 |
| D.用FeS做沉淀剂,除去废水中的Cu2+和Hg2+ |