在铁制品上镀一层一定厚度的锌层,以下方案设计正确的是
| A.锌作阳极,镀件作阴极,溶液中含有锌离子 |
| B.铂作阴极,镀件作阳极,溶液中含有锌离子 |
| C.铁作阳极,镀件作阴极,溶液中含有亚铁离子 |
| D.锌作阴极,镀件作阳极,溶液中含有亚铁离子 |
如下图所示,将紧紧缠绕不同金属的铁钉放入培养皿中,再加入含有适量酚酞和NaCl的琼脂热溶液,冷却后形成琼胶(离子在琼胶内可以移动)。下列叙述正确的是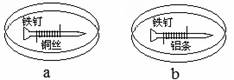
| A.a中铁钉附近呈现红色 | B.b中铁钉上发生还原反应 |
| C.a中铜丝上发生氧化反应 | D.b中铝条附近有气泡产生 |
下列说法正确的是
| A.润洗酸式滴定管时应从滴定管上口加入3~5mL所要盛装的酸溶液,倾斜着转动滴定管,使液体润湿其内壁,再从上口倒出,重复2~3次 |
| B.向酒精灯内添加酒精时,不能多于容积的2/3,若不慎洒出的酒精在桌上燃烧,应迅速用水灭火 |
| C.探究温度对反应速率的影响时,应先将硫代硫酸钠溶液、硫酸溶液分别在水浴中加热,然后混合 |
| D.在“金属析氢腐蚀”实验中,外面缠绕着铜丝的铁钉上产生气泡多,在铁钉周围出现血红色现象(溶液中滴加几滴KSCN溶液) |
拴上金属条的铁钉插在含有酚酞的NaCl溶液中,如图所示,可以看到在贴近金属条一边的溶液出现粉红色。该金属条可能是
| A.镁 | B.铝 | C.锌 | D.铜 |
某课外活动小组,为研究金属的腐蚀和防护的原理,做了以下实验:将剪下的一块镀锌铁片,放入锥形瓶中,并滴入少量食盐水将其浸湿,再加数滴酚酞试液,按如右图所示的装置进行实验,过一段时间后观察。下列现象可能出现的是
| A.B中导气管中产生气泡 | B.B中导气管里形成一段水柱 |
| C.锥形瓶中溶液无色 | D.铁被腐蚀 |
下列对钢铁制品采取的措施不能防止或减缓钢铁腐蚀的是
| A.保持表面干燥 | B.表面镀锌 |
| C.表面镶嵌铜块 | D.与直流电源负极相连 |
家用炒菜铁锅用水清洗放置后出现红棕色的锈斑,在此变化过程中不发生的化学反应是
| A.4Fe(OH)2+2H2O+O2=4Fe(OH)3 | B.2Fe+2H2O+O2=2Fe(OH)2↓ |
| C.2H2O+O2+4e―=4OH- | D.Fe-3e―=Fe3+ |
化学在工业生产和日常生活中有着重要的应用。下列说法不正确的是
| A.铁表面镀铜,铁作阳极 |
| B.明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 |
| C.钢铁吸氧腐蚀的正极反应:O2+2H2O+4e-=4OH- |
| D.在轮船外壳上镶入锌块,可减缓船体的腐蚀速率 |
下列说法正确的是
| A.明矾水解形成的Al(0H)3胶体能杀菌消毒,可用于水的净化 |
| B.镀锡的铁制品比镀锌的铁制品耐用 |
| C.乙醇和乙酸都能溶于水,都是电解质 |
| D.分别与等物质的量的HC1和CH3COOH恰好中和时,消耗NaOH的物质的量相同 |
下列说法不正确的是
| A.2014年德美科学家因开发超分辨率荧光显微镜获诺贝尔化学奖,使光学显微镜分辨率步入了纳米时代。利用此类光学显微镜可以观察活细胞内蛋白质等大分子。 |
| B.利用外接直流电源保护铁质建筑物,属于电化学中牺牲阳极的阴极保护法 |
| C.镧镍合金能大量吸收H2形成金属氢化物,可作储氢材料 |
| D.分类方法、统计方法、定量研究、实验方法和模型化方法等是化学研究的常用方法 |
下列叙述正确的是
| A.铜、铁和FeCl3溶液形成的原电池,铜极放出氢气 |
| B.电解硫酸钠溶液就是电解水,电解后溶液pH升高 |
| C.铁锅生锈的正极反应为:O2+2H2O+4e-===4OH- |
| D.工业上电解饱和食盐水的阳极反应为:2H++2e-===H2↑ |
下列有关钢铁腐蚀与防护的说法正确的是
| A.钢管与电源正极连接,钢管可被保护 |
| B.铁遇冷浓硝酸表面钝化,可保护内部不被腐蚀 |
| C.钢管与铜管露天堆放在一起时,钢管不易被腐蚀 |
| D.钢铁发生析氢腐蚀时,负极反应是Fe-3e-===Fe3+ |
关于下列各装置图的叙述不正确的是
| A.用图①装置精炼铜,a极为粗铜,b为精铜,电解质溶液为CuSO4溶液 |
| B.图②装置的盐桥中KCl的Cl-移向乙烧杯 |
| C.图③装置中钢闸门应与外接电源的正极相连获得保护 |
| D.图④两个装置中通过导线的电子数相同时,消耗负极材料的物质的量不同 |
下列有关金属腐蚀与防护的说法正确的是
| A.银器表面在空气中因电化腐蚀渐渐变暗 |
| B.当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用 |
| C.在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 |
| D.可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |