北京市西城区高三上学期期末考试化学试卷
1.下列叙述中不正确的是
| A.SO2是大气污染物之一 |
| B.食物腐败变质发生了化学变化 |
| C.凡含有添加剂的食物对人体健康均有害,不宜食用 |
| D.废弃的塑料、金属、纸制品及玻璃都是可回收再利用的资源 |
2.下列有关物质水解的说法正确的是
| A.纤维素不能水解成葡萄糖 | B.油脂水解产物之一是甘油 |
| C.蛋白质水解的最终产物是多肽 | D.蔗糖水解产物仅有葡萄糖 |
3.下列有关化学用语表示正确的是
A.氮气的电子式: |
B.羟基的电子式: |
C.氯离子的结构示意图: |
D.质子数为92、中子数为146的铀(U)原子的核素符号: |
4.下列物质的水溶液:①NaOH、②CH3COOH、③NH3、④NaHCO3、⑤Cl2,不能溶解CaCO3的是
| A.①③④ | B.①④⑤ | C.②④ | D.②⑤ |
5.下列有关钢铁腐蚀与防护的说法不正确的是
| A.生铁比纯铁容易生锈 |
| B.钢铁的腐蚀生成疏松氧化膜,不能保护内层金属 |
| C.钢铁发生吸氧腐蚀时,正极反应式为:O2+2H2O+4e-== 4OH- |
| D.为保护地下钢管不受腐蚀,可使其与直流电源正极相连 |
6. 下列应用不涉及氧化还原反应的是
| A.铝热法冶炼难熔金属 | B.工业上电解熔融状态Al2O3制备Al |
| C.Na2O2用作呼吸面具的供氧剂 | D.实验室用NH4Cl和Ca(OH)2制备NH3 |
7.化学与社会密不可分,利用化学反应可实现物质转化和能量转化,下列说法不正确的是
| A.播撒碳酸钙粉末可治理被酸雨污染的湖泊 |
| B.火力发电是将化学能直接转化为电能 |
| C.维生素C具有还原性,可消除体内具有强氧化性的物质 |
| D.过量服用阿司匹林引起酸中毒,可静脉注射NaHCO3溶液解毒 |
8.NA表示阿伏加德罗常数的值,下列说法正确的是
| A.0.1 mol甲烷含有的电子数为NA |
| B.1 L 0.1 mol/L Na2CO3溶液中含有的CO3数目为0.1 NA |
| C.1 L pH=1的硫酸溶液中含有的H+ 数为0.2 NA |
| D.标准状况下,2.24 L CO和CO2混合气体中含有的氧原子数为0.15NA |
9.已知34Se、35Br位于同一周期,根据元素在周期表中的位置,判断下列说法正确的是
| A.离子还原性:Cl->Br- | B.气态氢化物的稳定性:H2S>H2Se |
| C.原子半径:Cl>Br>Se | D.酸性:H2SeO4>HBrO4>HClO4 |
10.芥子醇是合成工程纤维的单体,结构简式如图。下列有关芥子醇的说法不正确的是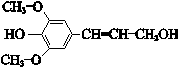
| A.分子式为C11H14O4 |
| B.存在顺反异构现象 |
| C.能发生水解反应 |
| D.能与溴水反应 |
11.能正确表示下列反应的离子方程式是
| A.铝放入烧碱溶液中溶解:Al+2OH- = AlO2- +H2↑ |
| B.碳酸钙溶于醋酸溶液:CaCO3+2H+ = Ca2++CO2↑+H2O |
| C.稀硫酸中加氢氧化钡溶液至中性:H+ + OH- = H2O |
D.氯化铁溶液呈酸性:Fe3+ + 3H2O 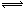 Fe(OH)3 +3H+ Fe(OH)3 +3H+ |
12.分别依据下列实验事实,得出的结论正确的是
| |
实验事实 |
结论 |
| A |
苯酚和水的浊液中,加碳酸钠溶液,溶液变澄清 |
苯酚的酸性比碳酸强 |
| B |
将“84”消毒液(含NaClO)滴入品红溶液中,褪色缓慢,若同时加入食醋,红色很快褪为无色 |
随溶液pH减小,“84”消毒液的氧化能力增强 |
| C |
铜放入稀硫酸中,无明显现象,再加入硝酸钠固体,溶液变蓝,有明显的气泡放出,铜溶解 |
硝酸钠可以加快铜与稀硫酸的反应速率 |
| D |
向2 mL 0.1 mol/L的硝酸银溶液中加入1 mL0.1 mol/L NaCl溶液,出现白色沉淀,再加入几滴0.1 mol/L Na2S溶液,有黑色沉淀生成 |
氯化银的溶解度大于硫化银 |
13.下列图示的实验操作,不能实现相应实验目的的是
| A.鉴别甲苯与己烷 |
B.研究浓度对Fe3++3SCN- Fe(SCN)3的影响 Fe(SCN)3的影响 |
 |
 |
| C.检验CH3CH2OH与浓H2SO4加热至170℃的产物乙烯 |
D.比较碳酸钠与碳酸氢钠的热稳定性 |
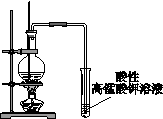 |
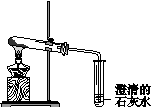 |
14.向AgCl浊液中滴加氨水后可得到澄清溶液,继续滴加浓硝酸后又有沉淀生成。经查资料得知:Ag+ + 2NH3·H2O  Ag(NH3+)2+ 2H2O。下列分析不正确的是
Ag(NH3+)2+ 2H2O。下列分析不正确的是
A.浊液中存在沉淀溶解平衡:AgCl (s)  Ag+(aq)+Cl-(aq) Ag+(aq)+Cl-(aq) |
| B.实验可以证明NH3结合Ag+能力比Cl-强 |
| C.实验表明实验室可用氨水洗涤银镜反应后的试管 |
| D.由资料信息可推知:加浓硝酸后生成的沉淀为AgCl |
15.在不同温度下,向2 L密闭容器中加入1 mol NO和1 mol活性炭,发生反应:
2NO(g)+C(s) N2(g)+CO2(g) ΔH=﹣213.5 kJ/mol,达到平衡时的数据如下:
N2(g)+CO2(g) ΔH=﹣213.5 kJ/mol,达到平衡时的数据如下:
| 温度/℃ |
n(活性炭)/mol |
n(CO2)/mol |
| T1 |
0. 70 |
_______ |
| T2 |
_______ |
0.25 |
下列说法不正确的是
A.上述信息可推知:T1<T2
B.T1℃时,该反应的平衡常数K=9/16
C.T2℃时,若反应达平衡后再缩小容器的体积,c (N2) :c (NO)不变
D.T1℃时,若开始时反应物的用量均减小一半,平衡后NO的转化率减小
16.球墨铸铁中含有一种铁碳化合物X。实验室测定化合物X的组成实验如下:
下列说法不正确的是
| A.固体2是氧化铁 |
| B.X的化学式可以表示为Fe3C2 |
| C.溶液甲中可能含有Fe3+ |
| D.X与足量的热浓硝酸反应有NO2和CO2生成 |
17.(共6分)金属Na、Mg、Al有广泛的应用。
(1)周期表中Na、Mg、Al所在周期是 。
(2)为比较Na、Mg、Al的金属性,进行了如下实验:
实验1:各取1.0 g金属钠和镁,分别加入到5 mL水中,钠与水反应剧烈,镁与水反应缓慢。
实验2:各取1.0 g的镁条和铝条,分别加入到5 mL 1.0 mol/L盐酸中,镁与盐酸反应剧烈,铝与盐酸反应较剧烈。
已知:元素金属性强弱可以从其单质与水(或酸)反应置换出氢的难易程度来判断。
由实验1和实验2得出的结论是 ,用原子结构理论解释:同周期元素从左到右, 。
(3)Na、Mg、Al都可以用于制备储氢的金属氢化物。
① NaH是离子化合物,能与水发生氧化还原反应生成H2,该反应的还原剂是 。
② NaAlH4是一种良好的储氢材料。NaAlH4与水反应的化学方程式是 。
18.(共6分)现有下列浓度均为0.1 mol/L的电解质溶液:
① Na2CO3、② NaHCO3、③ 、④ CH3COONH4、⑤ NH4HCO3
、④ CH3COONH4、⑤ NH4HCO3
(1)上述5种物质的溶液既能与盐酸又能与烧碱溶液反应的是(填写序号) 。
(2)已知溶液④呈中性,该溶液中离子浓度由大到小的顺序是 。
(3)已知溶液⑤呈碱性,比较④、⑤两溶液的酸碱性,可以得出的结论是 。
19.自然界中氮元素有多种存在形式。
(1)合成氨反应的化学方程式是 。
(2)NH3在一定条件下可被氧化。
已知:ⅰ.4NH3(g)+3O2(g)=2N2(g)+6H2O(g) ΔH=﹣1269 kJ/mol
ⅱ. 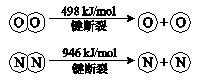
① 断开1 mol H-O 键与断开 1 mol H-N 键所需能量相差约______kJ;
② H-O 键比H-N键(填“强”或“弱”)______。
(3)下图是某压强下, N2与H2按体积比1: 3投料时,反应混合物中氨的体积分数随温度的变化曲线。其中一条是经过一定时间反应后的曲线,另一条是平衡时的曲线。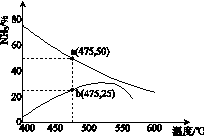
① 图中b点,U(正)______ U(逆)。(填“>”、“=”或“<”)
② 图中a点,容器内气体n(N2):n(NH3)= 。
(4)水中的氨在微生物作用下可被氧化为亚硝酸,其化学方程式是 。
(5)电解法能将碱性溶液中的NO2转化为N2而除去,其电极反应式是 。
20.某厂以重晶石(有效成分是BaSO4)为主要原料制取Ba(OH)2·8H2O晶体的示意图如下: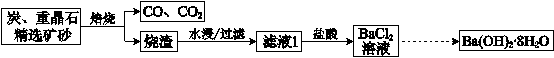
已知:i.BaSO4(s)+2C(s)=2CO2(g)+BaS(s) ΔH1=+226.2 kJ/mol
C(s)+CO2(g)=2CO(g) ΔH2=+172.5kJ/mol
ii.某些物质的溶解度(g/100g)简表
| |
10℃ |
20℃ |
40℃ |
60℃ |
80℃ |
| Ba(OH)2·8H2O |
2.48 |
3.89 |
8.22 |
20.9 |
101 |
| NaOH |
98.0 |
109 |
129 |
174 |
314 |
| NaCl |
35.8 |
35.9 |
36.4 |
37.1 |
38.0 |
| BaCl2 |
33.5 |
35.8 |
40.8 |
46.2 |
52.5 |
回答下列问题:
(1)炭与重晶石直接反应的热化学方程式是:BaSO4(s)+4C(s)=BaS(s)+4CO(g) ΔH=____kJ/mol。
(2)由BaCl2溶液可通过不同途径得到Ba(OH)2·8H2O。
途径1:
①得到固体1的离子方程式是______。
②固体2与水反应的化学方程式是______。
途径2: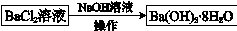
途径2中的“操作”是加热浓缩,冷却结晶,过滤。依据上述溶解度简表分析,过滤时的最佳温度是______;能从混合液中得到Ba(OH)2·8H2O晶体的原因是______。
(3)若向滤液1中加入CuO粉末,可直接得到含Ba(OH)2·8H2O晶体和CuS的浊液,反应化学方程式是______。将该浊液加热到80℃左右浓缩,趁热过滤,冷却滤液至室温,再过滤,即可得到Ba(OH)2·8H2O晶体。上述操作中趁热过滤的原因是______。
21.某中药主要含二硫化亚铁(FeS2),某学习小组欲用下图所示装置进行实验,测定其铁、硫元素的质量分数。
(1)装置中,A为高温灼烧装置,B为气体吸收装置,C为检测尾气中是否含有SO2的传感器。取m g该中药样品于装置A中,经充分反应,使硫元素全部转化为SO2和SO3,在B中得到白色沉淀,传感器(装置C)未检测到SO2。
① 装置B中的H2O2反应时表现出了 性。
② 欲计算硫元素的质量分数,需测量的数据是 。
③ 传感器的工作原理如下图所示。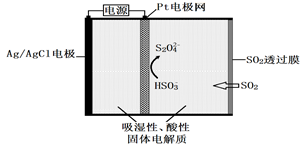
传感器中阴极的电极反应式是 。
(2)为测定铁元素的质量分数,继续实验。
a.将A装置中的剩余固体用足量盐酸酸浸,有少量H2产生。充分反应后过滤,得到黄色滤液;
b.向滤液中滴加TiCl3溶液,至恰好完全反应,TiCl3被氧化为TiO2+;
c.用滴定法测定Fe2+的量,消耗v mL n mol/LK2Cr2O7溶液。
① a中滤液含有的金属阳离子是 。
② b中反应的离子方程式是 。
③ c中K2Cr2O7被还原为Cr3+,样品中铁元素质量分数的数学表示式是 。
22.华法林是一种治疗心脑血管疾病的药物,其合成路径如下(部分反应条件略去)。
已知:
(1)A属于芳香烃,名称是 。
(2)B→C的化学方程式是______。
(3)D的含氧官能团名称是______。
(4)E的结构简式是______。
(5)F→K的化学方程式是______。
(6)由E与N合成华法林的反应类型是______。
(7)下列说法正确的是______。
a.M与N互为同分异构体
b.将L与足量的NaOH溶液反应,1 mol L消耗4 mol NaOH
c.E最多可与5 mol氢气加成
d.B可以发生消去反应
(8)L→M的转化中,会产生少量链状高分子聚合物,该反应的化学方程式是______。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号