室温时,M(OH)2(s)  M2+(aq)+2OH-(aq) Ksp=a; c(M2+)="b" mol · L -1时,溶液的pH等于
M2+(aq)+2OH-(aq) Ksp=a; c(M2+)="b" mol · L -1时,溶液的pH等于
A. |
B. |
C.14+ |
D.14+ |
下列说法正确的是
| A.常温下,NaCl(aq)+H2O(1)+CO2(g)+NH3(g)=NaHCO3(s)+NH4Cl(aq)能自发进行,则该反应的△H<0 |
| B.在等浓度NaCl和KI溶液中滴加AgNO3溶液,先产生白色沉淀 |
| C.等物质的量浓度的HA与NaA溶液等体积混合后,混合溶液不一定显酸性 |
| D.对于某△H<0的反应,加热能使该反应的反应速率和平衡常数均增大 |
(6分)氯化铜晶体(CuCl2·2H2O)含有FeCl2杂质,为制得纯净氯化铜晶体,首先将其制成水溶液,然后按下列操作步骤进行提纯:
①先加入氧化剂X,再加入物质Y,过滤得沉淀Z;
②将滤液蒸发结晶得纯CuCl2·2H2O晶体。
已知:三种离子从溶液中完全呈氢氧化物沉淀所需pH值:Fe3+:3.7,Cu2+:6.4,Fe2+:6.4试回答下列问题:
(1)加入氧化剂X的原因是____ __。
(2)下列物质都可以作为氧化剂,其中最适宜于本实验的是( )
| A.H2O2 | B.KMnO4 | C.NaClO | D.K2CrO7 |
(3)物质Y是__ ____,沉淀Z是__ ____.
(4)为分离出沉淀Z,采取的实验操作所用仪器有__ ____。
(5)操作②所用的仪器有____ __。
金属表面处理、皮革鞣制、印染等都可能造成铬污染。六价铬比三价铬毒性高,更易被人体吸收且在体内蓄积。
(1)工业上处理酸性含Cr2O72-废水的方法如下:
①向含Cr2O72-的酸性废水中加入FeSO4溶液,使Cr2O72-全部转化为Cr3+。写出该反应的离子方程式: 。
②调节溶液的pH,使Cr3+完全沉淀。实验室粗略测定溶液pH的方法为
;25℃,若调节溶液的pH=8,则溶液中残余Cr3+的物质的量浓度为 mol/L。(已知25℃时,Ksp[Cr(OH)3]=6.3×10-31)
(2)铬元素总浓度的测定:准确移取25.00mL含Cr2O72-和Cr3+的酸性废水,向其中加入足量的(NH4)2S2O8溶液将Cr3+氧化成Cr2O72-,煮沸除去过量的(NH4)2S2O8;向上述溶液中加入过量的KI溶液,充分反应后,以淀粉为指示剂,向其中滴加0.015mol/L的Na2S2O3标准溶液,终点时消耗Na2S2O3溶液20.00mL。
计算废水中铬元素总浓度(单位:mg·L-1,写出计算过程)。
已知测定过程中发生的反应如下:
①2Cr3+ + 3S2O82-+ 7H2O Cr2O72-+ 6SO42-+ 14H+
Cr2O72-+ 6SO42-+ 14H+
②Cr2O72-+ 6I-+ 14H+ 2Cr3+ + 3I2 + 7H2O
2Cr3+ + 3I2 + 7H2O
③I2 + 2S2O32- 2I-+ S4O62-
2I-+ S4O62-
①已知t℃时AgCI的Ksp=2×10-10;②在t℃时Ag2CrO4在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
| A.在t℃时,Ag2CrO4的Ksp为1×10-9 |
| B.在饱和Ag2CrO4溶液中加入K2CrO4可使溶液由Y点到X点 |
| C.在t℃时,以0.01 mol/LAgNO3溶液滴定20 mL 0.01 mol/L KCI和0.01 mol/L的K2CrO4的混和溶液,CrO42-先沉淀 |
D.在t℃时,反应Ag2CrO4(s)+2Cl-(aq) 2AgCl(s)+CrO42-(aq)的平衡常数K=2.5×107 2AgCl(s)+CrO42-(aq)的平衡常数K=2.5×107 |
下述实验设计能够达到目的的是
| 选项 |
实验目的 |
实验设计 |
| A |
证明Ksp(AgCl)﹥Ksp(AgI) |
往AgCl悬浊液中滴入KI浓溶液 |
| B |
除去Cu粉中的CuO |
向混合物中滴加适量稀硝酸 |
| C |
检验溶液中是否含有Fe2+ |
向溶液中滴入KSCN溶液,再滴加氯水 |
| D |
证明H2CO3酸性比H2SiO3强 |
Na2CO3和SiO2在高温下熔融反应 |
实验:①将0.1 mol·L-1 MgCl2溶液和0.5 mol·L-1NaOH溶液等体积混合得到浊液;
②取少量①中浊液,滴加0.1 mol·L-1FeCl3溶液,出现红褐色沉淀;③将①中浊液过滤,取少量白色沉淀,滴加0.1 mol·L-1FeCl3溶液,白色沉淀变为红褐色沉淀; ④另取少量白色沉淀,滴加饱和NH4Cl溶液,沉淀溶解。
下列说法中不正确的是
| A.将①中所得浊液过滤,所得滤液中含很少量Mg2+ |
B.①中浊液中存在溶解平衡:Mg(OH)2(s) Mg2+(aq)+2OH-(aq) Mg2+(aq)+2OH-(aq) |
| C.实验②和③均能说明Fe(OH)3比Mg(OH)2难溶 |
D.NH4Cl溶液中的NH 可能是④中沉淀溶解的原因 可能是④中沉淀溶解的原因 |
硫酸钠-过氧化氢加合物(xNa2SO4·yH2O2·zH2O)的组成可通过下列实验测定:①准确称取1.7700 g样品,配制成100.00 mL溶液A。②准确量25.00mL 溶液A,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体0.5825 g。③准确量取25.00 mL溶液A,加适量稀硫酸酸化后,用0.020 0mol/L KMnO4溶液滴定至终点,消耗KMnO4溶液25.00 mL。H2O2与KMnO4反应的离子方程式如下:2MnO4-+5H2O2+6H+===2Mn2++8H2O+5O2↑。
(1)已知室温下BaSO4的Ksp=1.1×10-10,欲使溶液中c(SO42-)≤1.0×10-6mol·L-1,应保持溶液中c(Ba2+)≥_______mol·L-1。
(2)上述滴定若不加稀硫酸酸化,MnO4-被还原为MnO2,其离子方程式为 。
(3)通过上述实验事实,该样品的组成为(写化学式) 。
(4)上述实验③KMnO4溶液滴定至终点的现象是)_____________,怎样判断滴定达到了终点 。
工业废水中常含有一定量的Cr2O 和CrO
和CrO ,它们会对生态系统造成很大的损害,其中还原沉淀法是常用的一种处理方法。流程如下:
,它们会对生态系统造成很大的损害,其中还原沉淀法是常用的一种处理方法。流程如下:
其中第①步中存在平衡:2CrO (黄色)+2H+
(黄色)+2H+ Cr2O
Cr2O (橙色)+H2O。下列有关说法正确的是
(橙色)+H2O。下列有关说法正确的是
A.第①步当2v(Cr2O )=v(CrO )=v(CrO )时,达到了平衡状态 )时,达到了平衡状态 |
B.对于上述平衡,加入适量稀硫酸后,溶液颜色变黄色,则有利于CrO 的生成 的生成 |
| C.常温下,Cr(OH)3的溶度积Ksp=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至9 |
D.第②步中,还原0.1 mol Cr2O 需要91.2 g FeSO4 需要91.2 g FeSO4 |
下列实验方案能达到目的的是
| A.除去Fe粉中混有的I2:加热使I2升华 |
| B.除去NaCl固体中混有的MgCl2:加入KOH溶液后过滤,滤液蒸发结晶 |
| C.除去碳酸钠中混有的碳酸氢钠:加入过量的氢氧化钠溶液,蒸发结晶 |
| D.除去氢氧化镁中混有的氢氧化钙:放入水中搅拌成浆状后,加入足量氯化镁溶液,充分搅拌,过滤,沉淀用蒸馏水洗涤 |
下述实验不能达到预期实验目的的是
| 选项 |
实验内容 |
实验目的 |
| A |
将2.5 g CuSO4·5H2O溶解在97.5 g 水中 |
配制质量分数为1.6%的CuSO4溶液 |
| B |
向盛有1 mL硝酸银溶液的试管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加Na2S溶液 |
说明一种沉淀能转化为另一种溶解度更小的沉淀 |
| C |
取少量待检固体溶于水中,滴加少量Ba(OH)2溶液,观察是否有白色沉淀生成 |
检验NaHCO3固体中是否含Na2CO3 |
| D |
取出分液漏斗中所需的上层液体 |
下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体从分液漏斗上口倒出 |
(实验班)(15分)钡(Ba)和锶(Sr)及其化合物在工业上有着广泛的应用,它们在地壳中常以硫酸盐的形式存在,BaSO4和SrSO4都是难溶性盐。工业上提取钡和锶时首先将BaSO4和SrSO4转化成难溶弱酸盐。
已知:SrSO4(s) Sr2+(aq)+SO
Sr2+(aq)+SO (aq) Ksp=2.5×10-7
(aq) Ksp=2.5×10-7
SrCO3(s) Sr2+(aq)+CO
Sr2+(aq)+CO (aq) Ksp=2.5×10-9
(aq) Ksp=2.5×10-9
(1)将SrSO4转化成SrCO3的离子方程式为________________________________,该反应的平衡常数为_________ ________(填具体数字);该反应能发生的原因是
_________________________________________(用沉淀溶解平衡的有关理论解释)。
(2)对于上述反应,实验证明增大CO 的浓度或降低温度都有利于提高SrSO4的转化率。判断在下列两种情况下,平衡常数K的变化情况(填“增大”、“减小”或“不变”):
的浓度或降低温度都有利于提高SrSO4的转化率。判断在下列两种情况下,平衡常数K的变化情况(填“增大”、“减小”或“不变”):
①升高温度,平衡常数K将________;②增大CO 的浓度,平衡常数K将________。
的浓度,平衡常数K将________。
(3)已知,SrSO4和SrCO3在酸中的溶解性与BaSO4和BaCO3类似,设计实验证明上述过程中SrSO4是否完全转化成SrCO3。实验所用的试剂为________;实验现象及其相应结论为_________________________________________________________。
已知常温下反应①NH3+H+ NH
NH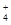 (平衡常数为K1),②Ag++Cl-
(平衡常数为K1),②Ag++Cl- AgCl(平衡常数为K2),③Ag++2NH3
AgCl(平衡常数为K2),③Ag++2NH3 Ag(NH3)
Ag(NH3)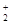 (平衡常数为K3)。
(平衡常数为K3)。
①、②、③的平衡常数关系为K1>K3>K2,据此所做的以下推测合理的是
| A.氯化银不溶于氨水 |
| B.银氨溶液中加入少量氯化钠有白色沉淀 |
| C.银氨溶液中加入盐酸有白色沉淀 |
| D.银氨溶液可在酸性条件下稳定存在 |
把Ca(OH)2放入蒸馏水中,一段时间后达到如下平衡:
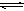
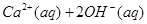 ,下列说法正确的是( )
,下列说法正确的是( )
| A.恒温下向溶液中加CaO,溶液的pH升高 |
| B.给溶液加热,溶液的pH升高 |
| C.向溶液中加入Na2CO3溶液,其中固体质量增加 |
| D.向溶液中加入少量NaOH固体,Ca(OH)2固体质量不变 |
下述实验不能达到预期实验目的的是( )
| 序号 |
实验内容 |
实验目的 |
| A |
将2.5gCuSO4·5H2O溶解在97.5g水中 |
配制质量分数为1.6%的CuSO4溶液 |
| B |
向盛有1mL硝酸银溶液的试管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加Na2S溶液 |
说明一种沉淀能转化为另一种溶解度更小的沉淀 |
| C |
室温下,用pH试纸测定浓度为0.1mol·L-1NaClO溶液和0.1mol·L-1CH3COONa溶液的pH |
比较HClO和CH3COOH的酸性强弱 |
| D |
室温下,分别向2支试管中加入相同体积、相同浓度的Na2S2O3溶液,再分别加入相同体积不同浓度的稀硫酸 |
研究浓度对反应速率的影响 |