过氧化碳酰胺(CO(NN2)2·H2O2)是一种白色晶体,易溶于水和有机溶剂,稍高温度时(>45℃)即分解,可作为高效、安全、方便的固体消毒剂。工业上常用湿法合成,工艺流程如下:
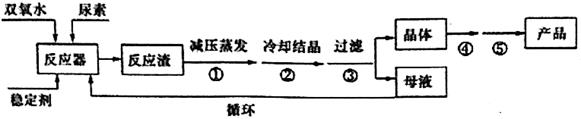
(1)反应器中发生的反应为:CO(NH2)2+H2O2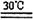 CO(NN2)2·H2O2 △H <0,应采取_______方式加热,从母液中循环利用的物质为________。
CO(NN2)2·H2O2 △H <0,应采取_______方式加热,从母液中循环利用的物质为________。
(2)操作①采用减压蒸发的原因是________,操作④、⑤名称为________、________。
(3)过氧化碳酞胺也可用干法流程制取:
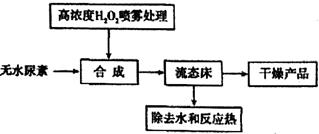
与湿法工艺对比,干法工艺的优点是________,缺点是________。
(4)为测定产品的纯度,称取3.0 g产品于锥形瓶中,加适量蒸馏水溶解,再加入几滴H2SO4,用0.2500 mol/L KMnO4标准溶液滴定,终点时消耗标准溶液40.00 mL〔己知:尿素与KMnO4溶液不反应)。
①完成并配平方程式:______MnO4-+______H2O2+ ______H+=_______Mn2 ++_____H2O+______
②产品纯度为________(结果保留到小数点后一位)。
某化工厂尝试用软锰矿、闪锌矿(含有Fe、Cu、 Al等元素杂质)联合制备工业产品MnO2和Zn。(已知:软锰矿的主要成分为MnO2,闪锌矿主要成分为ZnS。)
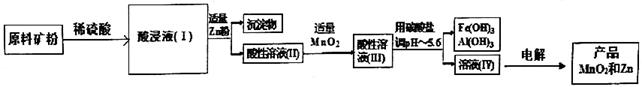
(1)原料需加工成矿粉的原因是________。
(2)己知MnO2有较强的氧化性,在酸性溶液中能氧化金属硫化物生成硫单质,请写出原料矿粉加稀硫酸后所发生的主要反应________。
(3)酸浸液(I)中含有的金属阳离子有Mn2+、Fe3+、Zn2+、________、________。
(4)酸性溶液(II)中加入适量MnO2的作用是________;酸性溶液(Ⅲ)中所加的碳酸盐可选用________ (填序号)。
①Na2CO3 ②MnCO3 ③ZnCO3 ④CaCO3
(5)电解溶液Ⅳ后阳极产物为________,若电解过程转移lmol电子,则理论上阴极产物的质量为________g。
利用废旧镀锌铁皮制备磁性Fe3O4胶体粒子及副产物ZnO,制备流程图如下:
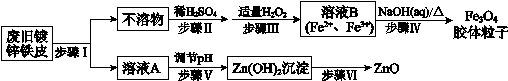
已知:Zn及其化合物的性质与Al及其化合物的性质相似。
回答下列问题:
(1)步骤I中所用的试剂是___________。
(2)步骤III中反应的离子方程式是__________________________________。
(3)步骤V可选用的试剂是_________(填序号)。
a.NaOH溶液 b.氨水 c.盐酸
(4)步骤VI的实验操作是_____________。
现代工业常以氯化钠为原料制备纯碱,部分工艺流程如下:
已知反应I为:NaCl + CO2 + NH3 + H2O === NaHCO3↓+ NH4Cl
(1)工业生产中,制备NH3的化学方程式是_____________________________。
(2)海水中含有大量的NaCl,以及少量的Ca2+、Mg2+、SO42−等离子。
① 为得到纯净的饱和NaCl溶液,进行了如下操作。请补全操作步骤:
a.向浓缩后的海水中加入过量的氢氧化钠溶液后,过滤;
b.向滤液中___________________________,过滤;
c.向滤液中___________________________,过滤;
d.向滤液中加入足量的稀盐酸;
e.加热煮沸一段时间,得到饱和NaCl溶液。
② 步骤c中反应的离子方程式是______________________________。
(3)反应II的化学方程式是_________________________________。
(4)制得的纯碱中含有少量NaCl。取5.5 g纯碱样品加入足量稀硫酸,得到标准状况下1120 mL CO2。则样品中纯碱的质量分数是_________%(保留1位小数)。
工业上用软锰矿(主要成分MnO2,杂质金属元素Fe、Al等) 制备MnSO4·H2O 的一种工艺流程如下:
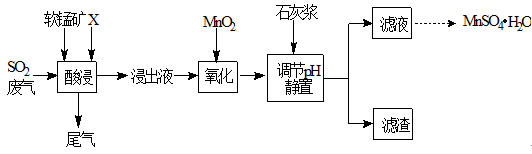
已知:
1.浸出过程中发生的主要反应化学方程式为:MnO2+SO2 =MnSO4
2.浸出液中阳离子主要有Mn2+、Fe2+、Al3+等
回答下列问题:
(1)物质X最好选用
a.盐酸 b.硫酸 c.硝酸
(2)酸浸时SO2的吸收效率与pH、温度的关系如下图所示,为提高SO2的吸收效率,酸浸适宜的条件是 。
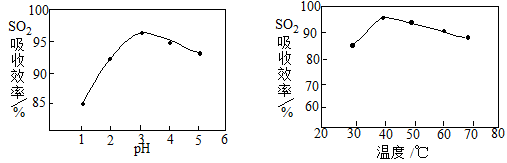
(3) 流程中“氧化”步骤主要反应的离子方程式是 。
(4) 加入石灰浆调节pH,可将氧化后的浸出液中Fe3+、Al3+形成氢氧化物除去。检验Fe3+是否除尽的最佳方法是 。
(5) 用MnSO4可测定水中溶解氧,方法是:取100 mL 水样,迅速加入足量MnSO4溶液及含有NaOH的KI溶液,立即塞上塞子、振荡,使之充分反应;打开塞子,迅速加入适量的稀硫酸,此时有I2生成;再用5.00×10-3 mol·L-1 Na2S2O3溶液和I2反应,当消耗Na2S2O3溶液 12.0 mL时反应完全。有关化学反应方程式如下:
① 2Mn2++O2+4OH-=2MnO(OH)2(反应很快);
② MnO(OH)2+2I-+4H+=Mn2++I2+3H2O;
③ I2+2S2O32-=S4O62-+2I-。
计算水样中溶解氧的浓度(以mg·L-1为单位),写出计算过程。
已知孔雀石的主要成分为Cu2(OH)2CO3,还含少量FeO、SiO2。现以孔雀石为原料制备CuSO4·5H2O。
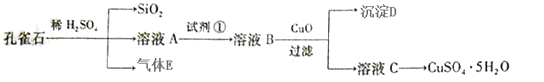
(1)实验步骤中试剂①最佳选择 (填代号);
a.H2O2 b.Cl2 c.KMnO4 d.HNO3
请写出其对应的离子方程式 。
(2)溶液B中加入CuO作用是 。
(3)由溶液C获得CuSO4·5H2O晶体,需要经___________、____________和过滤。
(4)25 ℃,Fe(OH)3的Ksp=1×10-38,若要将溶液中的Fe3+沉淀完全,必需调节溶液pH> 。
(5)实验室用惰性电极电解500ml的CuSO4溶液一段时间后,撤去电源,若加入0.2mol Cu(OH)2恰好使电解液恢复到原来状态,则电解过程中转移电子的物质的量为__________mol,原CuSO4溶液的物质的量浓度为________mol·L-1。
氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。CuCl是白色固体,难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以硫化铜精矿为原料生产CuCl的工艺过程如下:
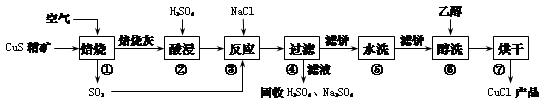
回答下列问题:
(1)CuS精矿经250 ℃低温焙烧后生成CuO,步骤②中主要反应的离子方程式是 。
(2)步骤③先加NaCl、通入SO2时无沉淀,加水稀释就产生大量白色沉淀,其原因是 。
(3)步骤⑤包括用pH=2的酸洗、水洗两步操作,酸洗采用的酸是_______(写名称);步骤⑥醇洗的作用是 。
(4)已知25℃,101 kPa时:S(s)+O2(g)==SO2(g) ∆H=-296.8 kJ/mol
2Cu(s)+O2(g)==2CuO(s) ∆H=-314.6 kJ/mol
Cu(s)+S(s)==CuS(s) ∆H=-53.1 kJ/mol
步骤①中CuS与O2反应的热化学方程式是 。
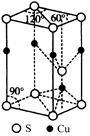
(5)CuS晶胞结构如图所示,其中含有硫原子的数目是 。
(6)假设上述①~③步反应完全转化,④~⑦步操作共损失产品3.5%,反应生成的硫酸全部被循环利用,则生产100 kg 96.5%的CuCl(Mr=99.0)产品,除循环利用之外,需要处理的尾气中含SO2 m3(标准状况)。
工业上处理含铬(主要成分是HCrO4-)污水并制备磁性铁铬氧体工艺流程如下:
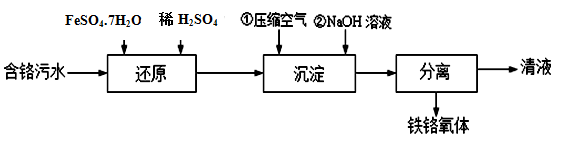
(1)还原过程中HCrO4-转化为Cr3+ 的离子方程式为 ;
(2)当沉淀池中c(Fe2+):c(Fe3+)=2:1时,能生成铁铬氧体。通入压缩空气是形成铁铬氧体的必要条件之一,通入压缩空气的目的是 、 。在加NaOH溶液之前通入的空气量不宜过多,若过多必须向沉淀池中增补的物质可能为: 。(填字母)
| A.FeSO4 | B.Cu | C.H2O2 | D.Fe |
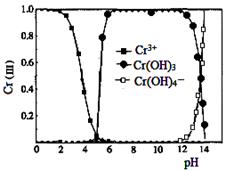
(3)已知三价铬[Cr(Ⅲ)]在水溶液中的存在形态随pH 的变化如右图,为尽可能除去铬元素实现清液达标排放,沉淀池中pH要控制在 ;若pH过高,溶液中残留铬量增大,其原因为 。
某同学设计了如图所示装置(夹持仪器省略)进行系列实验,实验时将药品A逐滴加入到固体B中,请根据下列实验回答问题:
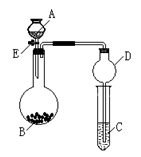
(1)若A为水,B为过氧化钠,C中盛有稀硫酸和FeCl2混合溶液,旋开 活塞E后,C中溶液颜色变化为 ,烧瓶中发生反应的化学方程式为 。
(2)若A为盐酸、B为大理石(主要成分为CaCO3粉末)、C中盛有水玻璃,则小试管中的现象是 ,固体的主要成分为(写化学式)_________________。
(3)利用上述装置可以验证SO2的性质, 若A为浓硫酸,B为亚硫酸钠粉末,那么C中盛有 溶液时可验证其具有漂白性;而C中盛有 溶液时可验证其具有还原性(各填一种物质名称)。
废弃物的综合利用既有利于节约资源,又有利于保护环境。实验室利用废旧电池的铜帽(Cu、Zn 总含量约为99%)回收Cu并制备ZnO 的部分实验过程如下:
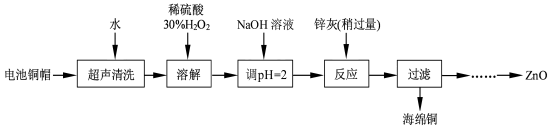
(1)写出铜帽溶解时铜与加入的稀硫酸、30%H2O2反应的离子反应方程式 ;铜帽溶解完全后,需加热(至沸)将溶液中过量的H2O2除去。
(2)为确定加入锌灰(主要成分为Zn、ZnO,杂质为铁及其氧化物)的量,实验中需测定除去H2O2后溶液中Cu2+的含量。实验操作为:准确量取一定体积的含有Cu2+的溶液于带塞锥形瓶中,加适量水稀释,调节溶液pH=3~4,加入过量的KI,用Na2S2O3标准溶液滴定至终点。上述过程中反应的离子方程式如下:2Cu2++4I-=2CuI(白色)↓+I2 2S2O32-+I2=2I-+S4O62-
①滴定选用的指示剂为 ,滴定终点观察到的现象为 ;
②某同学称取1.0g电池铜帽进行实验,得到100.00mL含有Cu2+的溶液,量取20.00mL上述含有Cu2+的溶液于带塞锥形瓶中,加适量水稀释,调节溶液pH=3~4,加入过量的KI,用0.1000mol/L Na2S2O3标准溶液滴定至终点。再重复操作实验3次,记录数据如下:
| 实验编号 |
1 |
2 |
3 |
4 |
| V(Na2S2O3)(mL) |
28.32 |
25.31 |
25.30 |
25.32 |
计算电池铜帽中Cu的质量分数为 ,(结果保留四位有效数字)若滴定前溶液中的H2O2没有除
尽,则所测定c (Cu2+)将会 (填“偏高”、“偏低”或“无影响”);
(3)常温下,若向50mL 0.0001mol/L CuSO4溶液中加入50mL0.00022mol/LNaOH溶液,生成了沉淀。已知KSP[Cu (OH)2] =2.0×10-20(mol/L)3,计算沉淀生成后溶液中c(Cu2+)= mol/L;
(4)已知pH>11 时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-。下表列出了几种离子生成氢氧化物沉淀的pH(开始沉淀的pH 按金属离子浓度为1.0 mol·L-1计算)。
| |
开始沉淀的pH |
沉淀完全的pH |
| Fe3+ |
1.1 |
3.2 |
| Fe2+ |
5.8 |
8.8 |
| Zn2+ |
5.9 |
8.9 |
实验中可选用的试剂:30%H2O2、1.0 mol·L-1HNO3、1.0 mol·L-1NaOH。由除去铜的滤液制备ZnO的实验步骤依次为:①向滤液中加入适量30% H2O2,使其充分反应;
② ;③过滤;
④ ;⑤过滤、洗涤、干燥;⑥900℃煅烧。
某研究性学习小组为合成1-丁醇,查阅资料得知一条合成路线:
CH3CH=CH2+CO+H2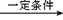 CH3CH2CH2CHO
CH3CH2CH2CHO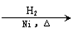 CH3CH2CH2CH2OH;
CH3CH2CH2CH2OH;
CO的制备原理:HCOOH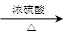 CO↑+H2O,CO的制备装置如图所示。请填写下列空白:
CO↑+H2O,CO的制备装置如图所示。请填写下列空白:
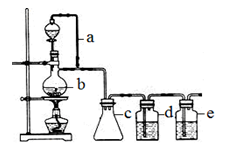
(1)装置a的作用是 ;
(2)实验时向装置b中加入几粒沸石的作用是 ,某同学进行实验时,加热后发现未加沸石,应采取的正确方法是 ;
(3)装置c的作用是 ;
(4)实验室用浓硫酸和2-丙醇制备丙烯时,还产生少量SO2、CO2及水蒸气,该小组用以下试剂检验这四种气体,混合气体通过试剂的顺序是④—_______—_______—_______—②(填序号,试剂可以重复使用);
①饱和Na2SO3溶液 ②酸性KMnO4溶液 ③石灰水 ④无水CuSO4 ⑤品红溶液
写出生成SO2、CO2及水蒸气反应的化学方程式 ;
(5)合成的1-丁醇中常含有杂质丁醛,设计出如下提纯路线:

已知:①R-CHO+NaHSO3(饱和)→RCH(OH)SO3Na↓;②沸点:乙醚 34℃,1-丁醇 118℃
试剂1为 ,操作1为 ,操作2为 ,操作3为 ;
(6)现用60g 2-丙醇制备1-丁醇,经分析知:由2-丙醇制备丙烯时的产率为85℅,由丙烯制丁醛产率为80℅,由丁醛制1-丁醇产率为75℅,则制得1-丁醇为 g。
碘化钠是实验室中常用的分析试剂,工业上用铁屑还原法制备NaI的流程如图所示。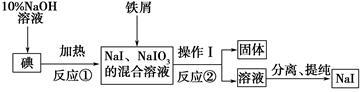
请回答下列问题。
(1)判断反应①中碘是否反应完全的方法是_______________________。
(2)操作Ⅰ的名称是_____________。
(3)反应①的离子方程式为_____________________________________。
(4)反应②中NaIO3被Fe单质还原为NaI,同时生成Fe(OH)3,该反应的化学方程式是_______________;在该反应中若有99 g NaIO3被还原,则转移电子的物质的量为________mol。
明矾石经处理后得到明矾[KAl(SO4)2·12H2O]。从明矾制备Al、K2SO4和H2SO4的工艺过程如下所示:
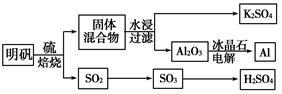
焙烧明矾的化学方程式为:4KAl(SO4)2·12H2O+3S 2K2SO4+2Al2O3+9SO2↑+48H2O
2K2SO4+2Al2O3+9SO2↑+48H2O
请回答下列问题:
(1)在焙烧明矾的反应中,还原剂是 。
(2)从水浸后的滤液中得到K2SO4晶体的方法是 。
(3)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,该电池反应的化学方程式是 。
铁及其化合物有重要用途,如聚合硫酸铁[]是一种新型高效的水处理混凝剂,而高铁酸钾(其中铁的化合价为+6)是一种重要的杀菌消毒剂,某课题小组设计如下方案制备上述两种产品: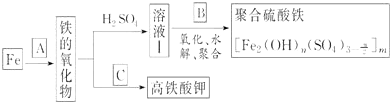
请回答下列问题:
(1)若A为H2O(g),写出反应方程式___________________________;
(2)若B为NaClO3与稀硫酸,写出其氧化Fe2+的离子方程式(还原产物为Cl-)_________________;
(3)若C为KNO3和KOH的混合物,写出其与Fe2O3加热共融制得高铁酸钾(K2FeO4)的化学方程式,并配平:
□Fe2O3+□KNO3+□KOH→□ ________ +□KNO2+□ ______
(4)为测定溶液Ⅰ中铁元素的总含量,实验操作如下:准确量取20.00mL溶液Ⅰ于带塞锥形瓶中,加入足量H2O2,调节pH<3,加热除去过量H2O2;加入过量KI充分反应后,再用0.1000mol・L-1Na2S2O3标准溶液滴定至终点,消耗标准溶液20.00mL.
已知:2Fe3++2I-═2Fe2++I2; I2+2S2O32-═2I-+S4O42-
①滴定选用的指示剂及滴定终点观察到的现象__________________________;
②溶液Ⅰ中铁元素的总含量为__________ g・L-1.若滴定前溶液中H2O2没有除尽,所测定的铁元素的含量将会________(填“偏高”“偏低”或“不变”)。
氯气的制取按照传统的方法,一般采用浓盐酸与MnO2共热来制备氯气,但是这种方法制过程中存在缺陷。某学习小组采用新的方法来制备氯气并进行性质实验。
Ⅰ.实验仪器及药品:
a.实验仪器:玻璃片、表面皿(顶部贴有湿润的蓝色石蕊试纸和干燥的石蕊试纸)、胶头滴管等
b.实验药品:KMnO4晶体、浓HCl、KBr溶液、淀粉溶液、KI溶液、FeSO4溶液、NaOH溶液、酚酞、KSCN溶液、AgNO3溶液、湿润的蓝色石蕊试纸和干燥的石蕊试纸。
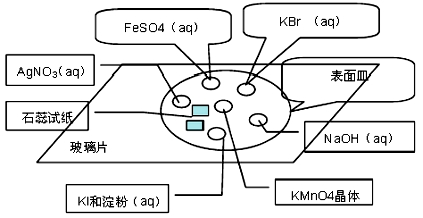
Ⅱ.实验方法及图示:
①在玻璃片上分别滴加KBr溶液、FeSO4溶液、NaOH稀溶液、KI溶液、AgNO3溶液。
②在KI溶液中滴加一滴淀粉溶液
③FeSO4溶液中滴加一滴KSCN溶液
④NaOH稀溶液中滴加一滴酚酞溶液
⑤在以上溶液分布的中心放置一块KMnO4晶体,然后滴加2-3滴浓盐酸,迅速盖上表面皿。并观察实验现象。
(1)该反应实验原理:2KMnO4+ 16HCl ="2KCl" +2MnCl2 +5Cl2↑+ 8H2O
该反应中氧化剂与还原剂的物质的量之比为 ;
(2)实验时反应一段时间后可以观察到KBr溶液由无色变为 色,其离子反应方程式为 ;
(3)滴有KSCN溶液的FeSO4溶液呈 色,其离子反应方程式为 、 ;
(4)滴加淀粉溶液的KI溶液呈 色,湿润的蓝色石蕊试纸的变化为 ,干燥的石蕊试纸的变化为 。