氧化还原反应在生活中应用广泛,酸性KMnO4、H2O2、Fe(NO3)3是重要的氧化剂.用所学知识回答问题:
(1) 3H2SO4+2 KMnO4+5H2O2=K2SO4+2MnSO4+5 O2↑+8 H2O,当有6 mol H2SO4参加反应的过程中,有 mol还原剂被氧化。
(2)在稀硫酸中,KMnO4能将H2C2O4氧化为CO2。该反应的化学方程式为
。
(3)取300mL 0.2mol/L的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则消耗KMnO4的物质的量的是 mol。
(4)在Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的离子方程式是 ,又变为棕黄色的原因是 .
根据反应8NH3+3Cl2=6NH4Cl+N2回答下列问题。
(1)氧化剂 ,还原剂
(2)用双线桥法标出反应中电子转移情况
(3)氧化剂与氧化产物的质量比__________
(4)当生成28gN2时,被氧化的物质的质量是__________g。
化合物BrFx与水按物质的量之比为3∶5发生反应,其产物为溴酸、氢氟酸、单质溴和氧气。
(1)BrFx中,x= 。
(2)该反应的化学方程式是 。
(3)此反应中的氧化剂是_________和还原剂是_________。
汽车尾气产生的NO2、CO等大气污染物,可以在催化剂的作用下转化为无毒物。其 反应式可表示为:2NO2 +4CO ="==" N2 +4CO2
反应式可表示为:2NO2 +4CO ="==" N2 +4CO2
①用双线法标出上述反应电子转移的方向和数目:
②该反应中氧化剂是________,还原剂是________,每有28g N2生成,反应中转移的电子为_____mol。
(8分)氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:NO3— + 4H+ + 3e- NO↑+2H2O; KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
NO↑+2H2O; KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)写出并配平该氧化还原反应的方程式: 。
(2)反应中硝酸体现了 等化学性质。
(3)反应中若产生0.2 mol气体,则转移电子的物质的量是 mol。
(4)若1 mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是 。
在氧化还原反应中,氧化过程和还原过程是同时发生的。
Cu2O—2e-+2H+=2Cu2++H2O是一个氧化过程的反应式,下列五种物质FeSO4、Fe2(SO4)2、CuSO4、Na2CO3、KI中的一种能使上述氧化过程顺利发生。
(1)写出并配平该反应的离子方程式: ;
反应中氧化剂和还原剂的物质的量之比是 。
(2)向(1)中反应后的溶液里,加入酸性高锰酸钾溶液,反应的离子方程式为
;CH2+、MnO4、Fe3+的氧化性由强到弱的顺序是 (用离子符号表示)。
实验室里迅速制备少量氯气可利用以下反应:
2 KMnO4+16 HCl(浓)="=" 2 KCl + 2 MnCl2 + 5 Cl2↑ + 8 H2O
此反应不需要加热,常温下就可以迅速进行。
①用“线桥法”表示出电子转移情况:
2 KMnO4+16 HCl(浓) ="==" 2 KCl + 2 MnCl2 + 5 Cl2↑ + 8 H2O
② 当电子转移的数目为6.02×1023个时生成的氯气的物质的量为 mol
磁性氧化铁(Fe3O4)可用于制造录音磁带和电讯器材,其溶于稀硝酸的化学方程式为:
3Fe3O4+28HNO3(稀)=9Fe(NO3)3+NO↑+14H2O。
(1)Fe3O4晶体的颜色为______________。
(2)Fe(NO3)2在水溶液中的电离方程式为________________________。
(3)上述反应中,氧化剂是_____________(填化学式),被还原的氮元素与未被还原的氮元素的物质的量之比为_________,每生成2.24L(标准状况下)NO时,转移电子的物质的量为____________mol。
化合物KaFeb(C2O4)c·dH2O(其中铁为正三价)是重要的光化学试剂。通过下述实验确定该晶体的组成。
步骤a:称取该样品4.91g溶于水中配成250mL溶液,取出25mL溶液,向其中加入过量的NaOH溶液,将沉淀过滤,洗涤,高温灼烧至质量不再改变,称量其固体的质量为0.08g。
步骤b:另取出25mL溶液,加入适量稀H2SO4溶液,用0.050 mol·L-1KMnO4溶液滴定,到达滴定终点时,消耗KMnO4溶液24.00mL。
已知: KMnO4+ H2C2O4+ H2SO4= MnSO4+ K2SO4+ CO2+ H2O
(1) 配平上述反应方程式
(2) 草酸为二元弱酸,其一级电离的方程式为 。
(3)滴定终点观察到的现象为 。
(4)通过计算确定样品的组成(写出计算过程)。
Cl2、Br2、I2都具有氧化性,其氧化性Cl2>Br2>I2,Cl2能把溴从溴化物中置换出来,其余类推。
(1)实验室用MnO2制备Cl2的反应中氧化剂是 ,氧化产物是 。将17.4g MnO2与足量的浓盐酸反应,则被氧化的HCl的物质的量为 。
(2)将溴水滴入KI溶液中的化学方程式为 。
Ⅰ、现有A g某气体,它由双原子分子构成,它的摩尔质量为M g·mol-1。若阿伏加德罗常数用NA表示,则:
(1)该气体所含原子的个数为________________个。
(2)该气体在标准状况下的密度为_______________ g/L。
(3)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为________________mol/L。
Ⅱ、已知食盐常加人KIO3来补充碘元素,检验食盐中是否加碘,可利用如下反应:KIO3+5KI+3H2SO4 3K2SO4+3I2+3H2O
3K2SO4+3I2+3H2O
(1)如果反应中转移0.2mol电子,则生成I2的物质的量为 mol。
(2)Cl2是一种有毒气体,如果泄漏会造成严重的环境污染。化工厂可用浓氨水来检验Cl2是否泄漏,有关反应的化学方程式为:3Cl2(气)+8NH3(气)=6NH4Cl(固)+N2(气)
若反应中消耗Cl2 1.5 mol,则被氧化的NH3在标准状况下的体积为______ L。
氧化还原反应在生产、生活中应用广泛,酸性KMnO4、H2O2、Fe(NO3)3是重要的氧化剂.用所学知识回答问题:
(1)3H2SO4+2 KMnO4+5H2O2=K2SO4+2MnSO4+5 O2↑+8 H2O,当有6 mol H2SO4参加反应的过程中,有 mol还原剂被氧化。
(2)在稀硫酸中,KMnO4与H2C2O4反应的离子方程式为
(3)取300mL 0.2mol/L的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则消耗KMnO4的物质的量的是 mol。
(4)在Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶 液先变为浅绿色的离子方程式是 ,又变为棕黄色的原因是
某学习小组用“间接碘量法”测定含有CuCl2·2H2O晶体的试样的纯度,过程如下:取0.36 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀CuI。用0.1000 mol/L Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00 mL。
已知:I2+2S2O32-=S4O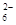 +2I-
+2I-
①可选用_____作滴定指示剂,滴定终点的现象是_______________________________ 。
②CuCl2溶液与KI反应的离子方程式为_______________________________________。
③该试样中CuCl2·2H2O的质量百分数为________。
已知KCl、K2Cr2O7、CrCl3、Cl2、HCl在溶液中可以形成一个氧化还原反应体系。
(1)已知反应中有水生成,则反应物分别是 和 (填化学式),当电子转移数为6mol时,化学方程式中水的化学计量数是 。
(2)反应过程中,发生氧化反应的物质是__________,被还原的元素是_________。
(3)当反应体系中Cl2的体积是224mL(标准状况)时,反应过程中转移电子______ mol。