现有24 mL浓度为0.05 mol·L-1的Na2SO3溶液恰好与20 mL某浓度的K2Cr2O7溶液完全反应。已知Na2SO3可被K2Cr2O7氧化为Na2SO4,元素Cr在还原产物中的化合价为+3价,则K2Cr2O7溶液的浓度为( )
| A.0.01 mol·L-1 | B.0.02 mol·L-1 | C.0.03 mol·L-1 | D.0.04 mol·L-1 |
已知RxO42-+MnO4-+H+→RO2+Mn2++H2O变化过程中,0.2molRxO42-参加反应,共转移0.4mol电子,则x为()
| A.2 | B.3 | C.4 | D.5 |
离子M2O7X-与S2-能在酸性溶液中发生如下反应:aM2O7X- +3S2- +cH+==2M3+ +eS+f H2O,则M2O7X-中M的化合价为 ( )
| A.+4 | B.+5 | C.+6 | D.+7 |
向100mL由等物质的量的FeBr2和FeI2配成的混合溶液中,缓慢通入氯气3.36L(标准状况),反应完全后,溶液中有一半的 Fe2+被氧化成Fe3+,则原混合液中FeI2的物质的量溶度为( )
| A.0.5 moL·L-1 | B.1.0 moL ·L-1 | C.1.2 moL ·L-1 | D.1.5 moL·L-1 |
已知Fe3O4可表示成FeO·Fe2O3,水热法制备Fe3O4纳米颗粒的总反应为: 3Fe2++2S2O32-+O2 +4OH-==Fe3O4+S4O62-+2H2O。下列说法正确的是( )
| A.O2和S2O32-是氧化剂,Fe2+是还原剂 |
| B.若有2 mol Fe2+被氧化,则被Fe2+还原的O2为0.5 mol |
| C.每生成1 mol Fe3O4,转移电子的物质的量为2 mol |
| D.参加反应的氧化剂与还原剂的物质的量之比为1∶1 |
若NA表示阿伏伽德罗常数,下列说法正确的是
| A.0.lmol氯气与铁反应,转移0.2NA电子 |
| B.0.lmol过氧化钠与水反应,转移0.2NA电子 |
| C.0.lmol铁与高温水蒸汽反应,转移0.3NA电子 |
| D.0.lmol二氧化锰与足量浓盐酸反应,有0.4NACl-被氧化 |
C1O2 是一种杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2:2KClO3+ H2C2O4+H2SO4=2ClO2↑+K2SO4+2CO2↑+2H2O,下列说法正确的是
| A.KClO3在反应中得到电子 | B.ClO2被氧化 |
| C.H2C2O4在反应中被还原 | D.1mol KClO3参加反应有2 mol 电子转移 |
工业上制取金刚砂的化学方程式如下:SiO2+3C=SiC+2CO↑。在这个氧化还原反应中,氧化剂和还原剂的物质的量之比为
| A.1︰2 | B.2︰1 | C.5︰3 | D.3︰5 |
已知:2Fe3++2I-=2Fe2++I2,向1L含有Fe2+、I━、Br━的溶液中通入适量氯气,溶液中各种离子的物质的量变化如下图所示。横、纵坐标的单位均为mol。有关说法不正确的是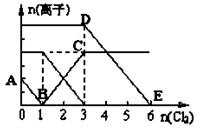
| A.线段BC代表Fe3+物质的量的变化情况 |
| B.原混合溶液中c(FeBr2)= 6 mol/L |
| C.原溶液中n (Fe2+): n (I-): n(Br-)=2:1:3 |
| D.当通入Cl22mol时,溶液中已发生的反应可表示为2Fe2++2I━+2Cl2=2Fe3++I2+4Cl━ |
心脏起搏器一般是给心跳缓慢的病人使用。某种类型的心脏起搏器工作时发生下列反应:4Li+2SOC12=4LiC1+S+SO2,下列有关判断正确的是
| A.还原剂只有锂 |
| B.SOC12中每个原子都达到8电子稳定结构 |
| C.氧化产物包括LiCl和SO2 |
| D.生成1. 12 LSO2时,反应转移电子为0.2 mol |
向VmLFeBr2溶液中缓慢通入amolCl2,结果溶液中有50%的Br-被氧化为溴单质,则原FeBr2溶液的物质的量浓度为
A.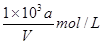 |
B.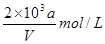 |
C.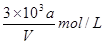 |
D.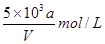 |
浓度为0.05 mol·L-1的Na2SO3溶液24 mL恰好能被20 mL浓度为0.02 mol·L-1的K2Cr2O7溶液氧化为Na2SO4,则K2Cr2O7被还原后得到的产物中Cr元素的化合价为( )
| A.+5 | B.+4 | C.+3 | D.+2 |
向27.2gCu和Cu2O的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成NO 和Cu(NO3)2。在所得溶液中加入1.0mol/L 的NaOH溶液1.0L,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为39.2g。下列有关说法不正确的是 ( )
| A.Cu与Cu2O 的物质的量之比为2:1 |
| B.硝酸的物质的量浓度为2.6mol/L |
| C.产生的NO在标准状况下的体积为4.48L |
| D.Cu、Cu2O与硝酸反应后剩余HNO3为0.2mol |
含有1mol HNO3的稀硝酸分别与不同质量的铁粉反应,所得氧化产物a、b与铁粉物质的量关系如图所示。下列有关判断正确的是
| A.a是Fe(NO3)2 |
| B.n1 = 0.375 |
| C.p = 0.20 |
| D.n2 = 0.30 |