过氧化氢(O为—1价)在二氧化锰催化作用下分解放出氧气的反应机理如下:
①MnO2 + H2O2 + 2H+ = Mn2+ + O2↑ + 2H2O ②Mn2+ + H2O2 = MnO2 + 2H+
下列说法正确的是
| A.H2O2在①中是氧化剂,在②中是还原剂 |
| B.在①中每生成1 mol O2,转移的电子数为1.204×1024 |
| C.Mn2+在①中是还原产物,在②中是氧化产物 |
| D.在二氧化锰催化作用下,1 mol H2O2分解生成22.4 L O2 |
硫代硫酸钠可作为脱氯剂,已知25.0 mL 0.100 mol·L-1Na2S2O3溶液恰好把224 mL(标准状况下) Cl2完全转化为Cl-,则S2O32—将转化为
| A.S2- | B.SO32- | C.S | D.SO42- |
已知Fe3O4可表示成FeO·Fe2O3,水热法制备Fe3O4纳米颗粒的总反应为: 3Fe2++2S2O32-+O2 +4OH-==Fe3O4+S4O62-+2H2O。下列说法正确的是( )
| A.O2和S2O32-是氧化剂,Fe2+是还原剂 |
| B.若有2 mol Fe2+被氧化,则被Fe2+还原的O2为0.5 mol |
| C.每生成1 mol Fe3O4,转移电子的物质的量为2 mol |
| D.参加反应的氧化剂与还原剂的物质的量之比为1∶1 |
向27.2g Cu和Cu2O的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成NO 和Cu(NO3)2。在所得溶液中加入1.0mol/L 的NaOH溶液1.0L,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为39.2g。下列有关说法不正确的是
| A.Cu与Cu2O 的物质的量之比为2:1 |
| B.产生的NO在标准状况下的体积为4.48L |
| C.硝酸的物质的量浓度为2.6mol/L |
| D.Cu、Cu2O与硝酸反应后剩余HNO3为0.2mol |
反应Cu+HNO3→Cu(NO3)2+NO+H2O中,9.6g Cu消耗做氧化剂的HNO3
| A.0.4mol | B.0.3mol | C.0.2mol | D.0.1mol |
若NA表示阿伏伽德罗常数,下列说法正确的是
| A.0.lmol氯气与铁反应,转移0.2NA电子 |
| B.0.lmol过氧化钠与水反应,转移0.2NA电子 |
| C.0.lmol铁与高温水蒸汽反应,转移0.3NA电子 |
| D.0.lmol二氧化锰与足量浓盐酸反应,有0.4NACl-被氧化 |
24mL浓度为0.05mol・L-1的Na2SO3溶液,恰好与20mL浓度为0.02mol・L-1的K2Cr2O7溶液完全反应,已知Na2SO3能被K2Cr2O7氧化为Na2SO4,则元素Cr在还原产物中的化合价为
| A.+2 | B.+3 | C.+4 | D.+5 |
已知镁和稀硝酸反应时,每有1mol HNO3反应,就有0.8 mol电子转移,此时硝酸的还原产物可能是
| A.N2O | B.NO2 | C.N2O4 | D.NO |
向VmLFeBr2溶液中缓慢通入amolCl2,结果溶液中有50%的Br-被氧化为溴单质,则原FeBr2溶液的物质的量浓度为
A.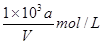 |
B.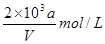 |
C.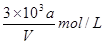 |
D.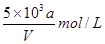 |
浓度为0.05 mol·L-1的Na2SO3溶液24 mL恰好能被20 mL浓度为0.02 mol·L-1的K2Cr2O7溶液氧化为Na2SO4,则K2Cr2O7被还原后得到的产物中Cr元素的化合价为( )
| A.+5 | B.+4 | C.+3 | D.+2 |
向27.2gCu和Cu2O的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成NO 和Cu(NO3)2。在所得溶液中加入1.0mol/L 的NaOH溶液1.0L,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为39.2g。下列有关说法不正确的是 ( )
| A.Cu与Cu2O 的物质的量之比为2:1 |
| B.硝酸的物质的量浓度为2.6mol/L |
| C.产生的NO在标准状况下的体积为4.48L |
| D.Cu、Cu2O与硝酸反应后剩余HNO3为0.2mol |
含有1mol HNO3的稀硝酸分别与不同质量的铁粉反应,所得氧化产物a、b与铁粉物质的量关系如图所示。下列有关判断正确的是
| A.a是Fe(NO3)2 |
| B.n1 = 0.375 |
| C.p = 0.20 |
| D.n2 = 0.30 |
实验室将NaClO3和Na2SO3按物质的量之比为2∶1倒入烧瓶中,同时滴入适量稀H2SO4,并用水浴加热,产生棕黄色的气体X,反应后测得NaClO3和Na2SO3恰好完全反应,则X为
| A.Cl2 | B.Cl2O | C.ClO2 | D.Cl2O3 |