甲酸和乙酸都是弱酸,当它们的浓度均为0.10 mol·L-1时,甲酸中的c(H+)约为乙酸中c(H+)的3倍。现有两种浓度不等的甲酸溶液a和b,以及0.10 mol·L-1的乙酸,经测定它们的pH从大到小依次为a、乙酸、b。由此可知
| A.a的浓度必小于乙酸的浓度 |
| B.a的浓度必大于乙酸的浓度 |
| C.b的浓度必小于乙酸的浓度 |
| D.b的浓度必大于乙酸的浓度 |
下列有关说法中,不正确的是
| A.a mol/L的HCN溶液与b mol/L的NaOH溶液等体积混合,所得溶液中c(Na+)>c(CN-),则a一定小于b |
| B.常温下,CH3COONa溶液的pH=8,则c(Na+) -c(CH3COO-)=9.9×10-7mol/L |
| C.常温下,0.1mol/L的某酸溶液中,若c(OH-)/c(H+) =1×10-8,则溶液中由水电离出的c(H+) =1×10-11mol/L |
| D.在0.1 mol/L Na2SO3溶液中加入少量NaOH固体,c(SO32-)与c(Na+)均增大 |
下列说法正确的是
| A.NaHCO3溶液加水稀释,c(Na+)/c(HCO3-)的比值保持增大 |
| B.浓度均为0.1 mol·L-1的Na2CO3、NaHCO3混合溶液:2c(Na+)=3[c(CO32-)+c(HCO3-)] |
| C.在高锰酸钾溶液中,H+、K+、SO42-、葡萄糖分子可以大量共存 |
| D.已知:Ksp(AgCl)=1.8×10-10, Ksp(Ag2Cr2O4)=2.0×10-12,则Ag2CrO4的溶解度小于AgCl |
常温下,下列溶液中的微粒浓度关系正确的是
A.氯气通入氢氧化钠溶液中: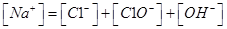 |
B.pH=8.3的NaHCO3溶液: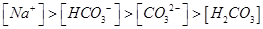 |
C.pH=11的氨水与pH=3的盐酸等体积混合: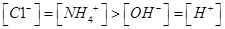 |
D.某溶液中只存在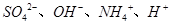 四种离子,则可能存在: 四种离子,则可能存在: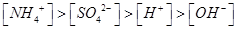 |
根据下表信息,下列判断正确的是
| 酸 |
电离常数(常温下) |
| CH3COOH |
Ki=1.8×10-5 |
| H2CO3 |
Ki1=4.3×l0-7, Ki2= 5.6×10-11 |
| H2S |
Ki1= 9.1×10-8, Ki2= 1.1×10-12 |
A.0.10mol/L的下列各溶液pH:Na2S<Na2CO3
B.HCO3-+CH3COOH→H2O+CO2↑+CH3COO-
C.硫化钠溶液可以与碳酸氢钠溶液反应
D.pH相同的CH3COOH、H2CO3、H2S,溶液浓度依次减小
常温下,0.2mol/L的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是
| A.HA为强酸 |
| B.该混合液pH=7 |
| C.图中X表示HA,Y表示OH-,Z表示H+ |
| D.该混合溶液中:c(A-)+ c(Y)=c(Na+) |
50℃时,下列各溶液中,离子的物质的量浓度关系正确的是
| A.pH=4的醋酸中:c(H+)=4.0mol·L-1 |
| B.饱和小苏打溶液中:c(Na+)= c(HCO3-) |
| C.饱和食盐水中:c(Na+)+ c(H+)= c(Cl-)+c(OH-) |
| D.pH=12的纯碱溶液中:c(OH-)=1.0×10-2mol·L-1 |
下列离子方程式中,属于水解反应的是
A.HCOOH+H2O HCOO-+H3O+ HCOO-+H3O+ |
B.CO2+H2O HCO3—+H+ HCO3—+H+ |
C.CO32—+H2O HCO3—+OH- HCO3—+OH- |
D.HS-+H2O S2-+H3O+ S2-+H3O+ |
常温下,物质的量浓度均为0.1mol·L-1的下列溶液:①CH3COONa ②NaOH ③NaCl ④NH4Cl,溶液的pH由大到小的顺序排列正确的是
| A.①>②>③>④ | B.②>①>③>④ |
| C.②>③>①>④ | D.②>③>④>① |
下列说法错误的是
| A.pH=2与pH=1的CH3COOH溶液中c(H+)之比为1︰10 |
| B.0.1 mol·L-1的CH3COOH溶液中,由水电离的c(H+)为10-13 mol·L-1 |
| C.常温下,等体积pH=12的NaOH溶液和pH=2的CH3COOH溶液混合,混合后溶液pH<7 |
| D.1.0 mol·L-1Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) |
物质的量浓度相同的下列溶液中,符合按pH由小到大顺序排列的是
| A.Na2CO3 NaHCO3 NaCl NH4Cl | B.Na2CO3 NaHCO3 NH4Cl NaCl |
| C.(NH4)2SO4 NH4Cl NaNO3 Na2S | D.NH4Cl (NH4)2SO4 Na2S NaNO3 |
常温下,取0.3 mol/L HY溶液与0.3 mol/L NaOH溶液等体积混合(不计混合后溶液体积变化),测得混合溶液的pH=9,则下列说法(或关系式)正确的是
| A.混合溶液中由水电离出来的c(OH-)=1×10-9 mol/L |
| B.混合溶液中离子浓度大小次序为:c(Y-)>c(Na+)>c(OH-)>c(H+) |
| C.c(OH-)-c(HY)=c(H+)=1×10-9 mol/L |
| D.c(Na+)=c(Y-)+c(HY)="0.3" mol/L |
(6分)按要求回答下列问题
(1)已知反应:mA(g) + nB(g) pC(g) + qD(g),v(A):v(B)= _________________;
pC(g) + qD(g),v(A):v(B)= _________________;
(2)任何情况下判断水溶液呈中性的依据是:_________________;
(3)NH4Cl溶液中离子浓度由大到小的顺序是:_________________。
将0.2 mol·L-1 HCN溶液和0.1 mol·L-1的NaOH溶液等体积混合后,溶液显碱性,下列关系中正确的是
| A.c(HCN) < c(CN—) | B.c(Na+)= c(CN—) |
| C.c(HCN)— c(CN—) = c(OH—) | D.c(HCN)+ c(CN—) =" 0.1" mol·L-1 |