上海市黄浦区高三上学期期末调研测试化学试卷
环保问题一直是社会的热门话题。下列相关叙述中错误的是
| A.乙醇和汽油都是可再生能源,应大力推广“乙醇汽油” |
| B.利用太阳能等新能源代替化石燃料 |
| C.在含硫的燃料中加入适量生石灰,以减少二氧化硫的排放量 |
| D.含次氯酸盐的漂水与含盐酸的洁厕灵混合使用会产生有毒气体 |
下列表达正确的是
A.氟原子中能量最髙的电子其电子云图: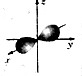 |
B.CO2的分子模型示意图: |
C.2-甲基丁醛的结构简式: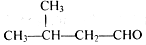 |
D.N2的结构式: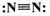 |
放射性元素碘131(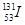 )和铯137(
)和铯137(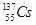 )是核反应物中的主要元素。下列叙述正确的是
)是核反应物中的主要元素。下列叙述正确的是
A.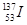 与 与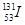 的所有性质都相同 的所有性质都相同 |
B.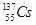 原子中含有中子数比质子数多27 原子中含有中子数比质子数多27 |
C.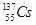 与 与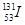 的中子数相同 的中子数相同 |
D.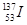 与 与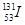 是同素异形体 是同素异形体 |
在下列变化过程中,被破坏的作用力正确的是
| A.干冰升华一一共价键 |
| B.二氧化硅熔融——范德华力 |
| C.氢氧化钠熔融——离子键、共价键 |
| D.硫酸氢钠溶于水——离子键、共价键 |
下列关于相关反应的叙述错误的是
| A.硫化钠溶液中通入硫化氢气体不发生化学反应 |
| B.向铜粉中加入稀硫酸,铜粉不溶解,再加入Cu(NO3)2固体,铜粉溶解 |
| C.将少量氯气通入碘化亚铁和淀粉混合溶液,溶液变蓝 |
| D.硫化亚铁加入稀硫酸后可以产生硫化氢气体 |
下列关于NH4+与CH4的相关数目比较前者大于后者的是
| A.电子数 | B.化学键数 | C.质子数 | D.原子数 |
下列反应中,浓硫酸既表现出强氧化性又表现出酸性的是
A.2NaCl+H2SO4(浓)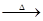 Na2SO4+2HCl↑ Na2SO4+2HCl↑ |
B.Na2SO3+H2SO4(浓)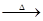 Na2SO4+SO2↑+H2O Na2SO4+SO2↑+H2O |
C.C+2H2SO4(浓)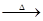 CO2↑+2SO2↑+2H2O CO2↑+2SO2↑+2H2O |
D.2FeO+4H2SO4(浓)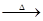 Fe2(SO4)3+SO2↑+4H2O Fe2(SO4)3+SO2↑+4H2O |
有四组同一族元素所形成的不同物质,在101kPa时测定它们的沸点(℃)如下表所示:
| 第一组 |
A -268.8 |
B -249.5 |
C -185.8 |
D -151.7 |
| 第二组 |
F2 -187.0 |
Cl2 -33.6 |
Br2 58.7 |
I2 184.0 |
| 第三组 |
HF 19.4 |
HCl -84.0 |
HBr -67.0 |
HI -35.3 |
| 第四组 |
H2O 100.0 |
H2S -60.2 |
H2Se -42.0 |
H2Te -1.8 |
下列各项判断正确的是
A.第四组物质中H2O的沸点最高,是因为H2O分子中化学键键能最强
B.第三组与第四组相比较,化合物的稳定性顺序为:HBr>H2Se
C.第三组物质溶于水后,溶液的酸性:HF>HCl>HBr>HI
D.第一组物质是分子晶体,一定含有共价键
电解尿素[CO(NH2)2]的碱性溶液制氢的装置示意图如图,其中电解池中隔膜仅阻止气体通过,阴、阳极均为石墨电极。下列相关叙述正确的是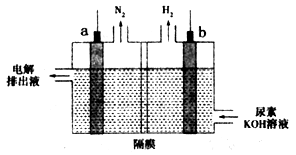
| A.b电极为阳极 |
| B.电子由b电极经过溶液流入a电极形成回路 |
| C.b电极上发生失去电子的反应 |
| D.尿素在a电极发生氧化反应 |
聚乳酸的结构为 有机物的相关叙述正确的是
有机物的相关叙述正确的是
| A.其单体不能发生消去反应 |
| B.其单体可以通过反应形成六元环状化合物 |
C.其单体含有 |
| D.聚乳酸是由加聚反应获得 |
对于某酸性溶液(可能含有Br-、SO42-、HSO3-、NH4+),分别进行如下实验:①加热时放出的气体可使品红溶液褪色;②加入碱溶液使溶液呈碱性,再加热时放出的气体可使湿润的红色石蕊试纸变蓝;③加入氯水时,溶液略呈橙红色;④加入BaCl2液和稀硝酸,产生不溶于稀硝酸的白色沉淀。对于下列微粒不能确定其在原溶液中是否存在的是
| A.Br- | B.SO42- | C.HSO3- | D.NH4+ |
常温下,下列各组离子在指定溶液中可能大量共存的是
| A.水电离出的c(OH-)=0.001mol/L的溶液:H+、Fe2+、Cl-、SO42- |
| B.c(H+)=0.001mol/L的溶液:NH4+、Ba2+、A1O2-、Cl- |
| C.pH=12的溶液:K+、Fe2+、ClO-、Br- |
| D.与铝反应产生大量氢气的溶液:Na+、NH4+、Cl-、NO3- |
关于下列各实验装置的叙述中,错误的是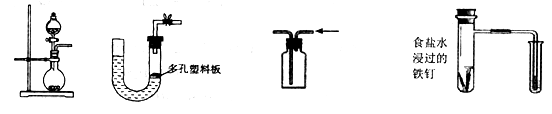
| A.装置①可用于实验室制取少量O2 |
| B.不用其它装置就可以检验装置②的气密性 |
| C.按图示气流方向实验室可用装置③收集HCl |
| D.装置④用于研究铁的吸氧腐蚀实验 |
在恒容密闭容器中通入一定量的X气体与Y气体并发生反应:2X(g)+Y(g) 2Z(g),测得在温度T1、T2下X的物质的量浓度c(x)随时间t变化的曲线如图所示,下列叙述正确的是
2Z(g),测得在温度T1、T2下X的物质的量浓度c(x)随时间t变化的曲线如图所示,下列叙述正确的是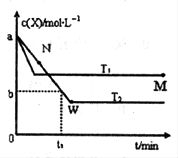
| A.该反应进行到M点放出的热量大于进行到W点放出的热量 |
B.T2下,在0〜t1时间内,υ(Y)=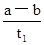 mol/(L·min) mol/(L·min) |
| C.M点的平衡常数比W点的平衡常数小 |
| D.M点时再加入一定量的X,平衡后X的转化率增大 |
根据表中信息,判断下列叙述中正确的是
| |
氧化剂 |
还原剂 |
其他反应物 |
氧化产物 |
还原产物 |
| ① |
Cl2 |
FeBr3 |
|
|
Cl- |
| ② |
KClO |
浓盐酸 |
|
Cl2 |
|
| ③ |
KMnO4 |
H2O2 |
H2SO4 |
O2 |
Mn2+ |
A.第③组反应的离子方程式为:2MnO4-+3H2O2+6H+→2Mn2++4O2↑+6H2O
B.第②组事实可以推测:ClO-、Cl-不能在溶液中大量共存
C.氧化性强弱的比较:KClO<Cl2
D.第①组的反应只可能有一种元素被氧化
表示阿伏加德罗常数,下列说法正确的是
| A.常温常压下,104 g苯乙烯中含有的碳碳双键数为NA |
| B.5.6克铁与足量盐酸反应,转移0.3NA个电子 |
| C.2mol的甲基(-CH3)所含电子数为14NA |
| D.标准状况下,22.4L辛烷完全燃烧生成二氧化碳分子数为8NA |
向80mL 0.1mol•L-1稀HNO3溶液中加入铜粉和铁粉混合物,固体完全溶解,在反应后溶液中滴加硫氰化钾溶液,溶液没有出现血红色。铜粉和铁粉混合物的质量可能是
| A.0.168g | B.0.184g | C.0.192g | D.0.200g |
下列实验操作正确且能达到预期目的的是
| |
实验目的 |
操作 |
| A |
证明二氧化硫漂白性 |
将二氧化硫通入溴水,溴水褪色 |
| B |
证明碳酸酸性强于苯酚 |
在苯酚钠溶液中通入二氧化碳,溶液变浑浊 |
| C |
除去苯中混有的苯甲酸 |
加入氢氧化钠溶液,振荡静置分液 |
| D |
比较锌铜金属活泼性 |
用导线连接两个石墨电极,放入ZnSO4、CuSO4的混合液 |
洋蓟属高档蔬菜,从洋蓟提取的物质A具有良好的保健功能和药用价值,A的结构如图。下列关于A的相关叙述正确的是
| A.A在酸性条件下可以发生水解反应 |
| B.1mol A和足量NaOH溶液反应,最多消耗9mol NaOH |
| C.A能和浓溴水发生加成和取代反应 |
| D.A含4种官能团 |
向NaHCO3和Na2CO3的混合液中逐滴加入Ba(OH)2溶液。下列离子方程式与事实不符的是
| A.OH-+HCO3-+Ba2+→BaCO3↓+H2O |
| B.CO32-+Ba2+→BaCO3↓ |
| C.2OH-+2HCO3-+Ba2+→BaCO3↓+CO32-+H2O |
| D.OH-+HCO3-→H2O+CO2 |
室温下,下列混合溶液中,各离子浓度的关系正确的是
A.pH=12的一元弱碱的溶液浓度一定比pH=2的一元强酸溶液浓度大
B.浓度均为0.1mol/L的硫酸氢钠溶液与氢氧化钠溶液等体积混合后:c(Na+)=2c(SO42-)=0.2mol•L-1
C.H2C2O4为二元弱酸,浓度为0.1 mol/L的Na2C2O4溶液中: c(Na+) =2c(C2O42-) +c(HC2O4-) + c(H2C2O4)
D.浓度均为0.l mol/L的NaHSO3溶液和NaHCO3溶液中(R表示S或C):c(H+)<c(RO32-)+c(OH-)
根据下表信息,下列判断正确的是
| 酸 |
电离常数(常温下) |
| CH3COOH |
Ki=1.8×10-5 |
| H2CO3 |
Ki1=4.3×l0-7, Ki2= 5.6×10-11 |
| H2S |
Ki1= 9.1×10-8, Ki2= 1.1×10-12 |
A.0.10mol/L的下列各溶液pH:Na2S<Na2CO3
B.HCO3-+CH3COOH→H2O+CO2↑+CH3COO-
C.硫化钠溶液可以与碳酸氢钠溶液反应
D.pH相同的CH3COOH、H2CO3、H2S,溶液浓度依次减小
(本题共13分)氨的催化氧化是工业制硝酸的重要反应,500°C,其反应方程式为:
4NH3(g) +5O2(g) 4NO(g)+6H2O(g)+Q,完成下列填空:
4NO(g)+6H2O(g)+Q,完成下列填空:
23.如果要提高上述反应的反应速率,可以采取的措施是
a.减压 b.增加NH3的浓度 c.升温 d.将水液化移走
24.在500℃时,在2L密闭容器中加入10mol NH3、10mol O2,上述可逆反应达到平衡,过程如图所示,在a时刻改变反应条件,重新达到平衡,该改变的条件可能是 ,比较b时刻与c时刻反应氨的转化率大小(填“>”或“<”)b c。其它条件不变,c时刻加压后,若平衡正向移动,其原因可能是 ,若在d时刻重新达到平衡,请在图中画出c到d的相关变化图像。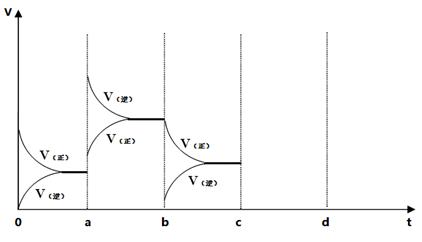
25.工业上以氨和空气为原料生产硝酸,请画出硝酸工业的物质流程图。
26.氨中氮元素原子最外层电子排布的轨道表达式是 ,短周期元素原子所形成的与N3-电子排布相同的离子所对应的原子的半径从大到小的排列顺序为 。其中非金属元素形成的氢化物的稳定性由强到弱为的顺序为(用化学式表示) 。
27.已知NH3与N2H4都是氮的氢化物,N2H4的电子式是 。NH3与N2H4都具有还原性,可以与其它强氧化剂反应,例如在一定条件下,氨可以被双氧水氧化为游离态氮,写出该反应的化学方程式 。
(本题共17分)铁元素、氮元素有多种可变价态,在氧化还原反应中常以不同价态出现,根据题中信息,完成下列填空:
28.金属与硝酸反应通常还会生成NO和NO2,当n(NO): n(NO2)<1时,产生的气体可以完全被氢氧化钠溶液吸收,写出除去这两种气体的方法,以化学方程式表示 、
29.室温下,0.1mol/L的亚硝酸、次氯酸钠的电离常数HNO2:Ki ="7.1×" 10-4, HClO: Ki ="2.98×" 10-8,将0.1mol/L的亚硝酸稀释100倍,c(H+)=将(填“不变”、“增大”、“减小”) ;Ki值将(填“不变”、“增大”、“减小”) 。写出HNO2、HClO、NaNO2、NaClO四种物质,可能相互之间发生的离子互换反应的离子方程式 。
30. 亚硝酸钠与氯酸钠都是白色粉末,且都有咸味,但亚硝酸盐都有毒性,通常它们可以通过加入热的白醋鉴别,亚硝酸钠遇到白醋会产生红棕色刺激性气味气体,该气体为 ;实验室鉴别氯化钠和亚硝酸钠的方法之一是测定等浓度NaNO2、NaClO的pH,其鉴别的理由是 。
31.现有11.2g铁单质恰好与稀硝酸反应,生成无污染的单质气体,该单质气体为 ,在反应后的溶液中加入铜粉,铜粉可以继续溶解,且无气体生成,铁与稀硝酸的反应产物中一定含有的金属阳离子是 ,若反应后的溶液最多可溶解铜粉6.4g,写出上述过程中铁与稀硝酸反应的化学方程式 。
(本题共11分)下图是制备二氧化硫制取和吸收装置(加热装置已省略)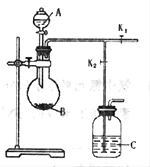
分液漏斗中是液体反应试剂A,烧瓶中盛反应试剂B。完成下列填空:
32.实验室制备二氧化硫的试剂是 和 。
33.检验该气体发生装置气密性的方法是 。
34.装置C是吸收多余二氧化硫的装置,其中盛放的吸收剂为 ,实验结束进行尾气吸收时,对活塞开关K1、K2的控制是 。
35.如果用该套装置制备盐酸,此时C瓶所加试剂为 ,此时C中液体可能会发生倒吸,如果不改变现有的装置,要克服这一安全隐患,可以在C瓶中再加入有机试剂封住长导管管口,该有机试剂可以为___________,吸收后,将 C瓶中的液体经过 操作获得盐酸。
36.甲同学用该装置测定一定质量小苏打样品(含少量NaCl)中碳酸氢钠的纯度,可以在C中加入氢氧化钠溶液吸收二氧化碳,通过C瓶增重得到二氧化碳质量,计算出碳酸氢钠的含量,实验结果小苏打含量偏低,你认为实验结果偏低的原因是 。
(本题共12分)钨在自然界主要以钨(+6价)酸盐的形式存在。黑钨矿的主要成分是铁和锰的钨酸盐,化学式常写成FeWO4、MnWO4。黑钨矿冶炼金属钨的流程如下图(已知:钨酸是一种难溶性强酸、对热不稳定)。其中A、B、C都是钨的化合物。完成下列填空:
37.上述从黑钨矿获得单质钨的过程中属于氧化还原反应的是(填数字序号) 。
38.操作①的名称为 ,得到的滤液为钨酸的钠盐,写出反应②的化学方程式 。该过程中产品C为 ,从产品C获得纯度较高的钨的另一反应原料应该为 。
39.若制得的钨中含有少量金属铁,为测定其中金属钨的含量(已知金属钨不溶于盐酸),甲同学用下列装置进行测定,相关实验步骤①加好称量好的样品和盐酸,记录B的液面位置;②检查气密性。③待A中不再有气体产生并恢复至室温后,记录B的液面位置;④将A中盐酸与样品混合;正确的操作顺序是 (填序号)。
40.若实验用样品的质量为a g,加入20mL盐酸与之充分反应后,测得排出水的体积为VL(标准状况下),测得的H2的体积应为 L,样品中的钨的质量分数的计算式为 。
41.在读取C装置液面数据时,应先 ,再平视读数,若样品中含有不溶于酸,也不与酸反应的物质,则测得钨的质量分数将 (填“偏大”、“偏小”或“不受影响”)。
(本题共8分)已知碳碳双键可以被臭氧氧化,反应如下: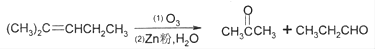
现由有机物 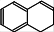 合成
合成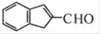 ,具体合成途径如下:
,具体合成途径如下: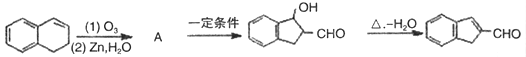
完成下列填空:
42. 所属的同系物的通式为 ,A的结构简式是 。
所属的同系物的通式为 ,A的结构简式是 。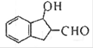 的一种同分异构体是一种芳香酸,且分子只含有一个环,写出满足条件的任意一种同分异构体的结构简式 。
的一种同分异构体是一种芳香酸,且分子只含有一个环,写出满足条件的任意一种同分异构体的结构简式 。
43.这三步反应的反应类型是 、 、 。
44.写出最后一步反应的反应方程式_____________________。
(本题共14分)贝诺酯是一种解热镇痛药,在酶的作用下可以释放出阿司匹林和扑热息痛,其结构为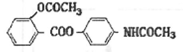 ,其合成途径如下:
,其合成途径如下: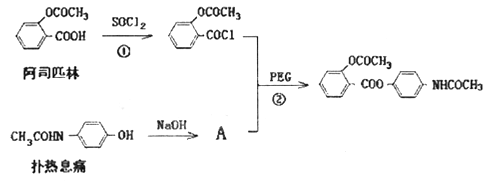
完成下列填空:
45.反应①的反应类型为 ,有机物A与扑热息痛的式量相差
46.贝诺酯所含的含氧官能团是
47.写出反应②的化学方程式 。
48.关于阿司匹林性质叙述正确的是(填选项编号)
| A.能与氯化铁溶液发生显色反应 | B.能与氢氧化铜悬浊液反应 |
| C.能发生消去反应 | D.能发生酯化反应 |
49.符合下列条件的扑热息痛的同系物共有 种,写出其中一种的结构简式 。
①碳原子数比扑热息痛多2个 ②苯环上只有2个对位的支链 ③含有2个甲基
50.若已知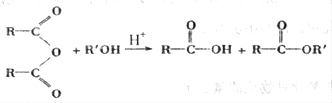
现以苯酚和乙酸酐(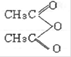 )为有机原料,合成阿司匹林,请设计完成下列合成途径(合成路线常用的表示方法为:
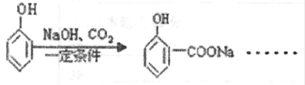
)为有机原料,合成阿司匹林,请设计完成下列合成途径(合成路线常用的表示方法为: ):
):
(本题共14分)元素周期表中大多数元素是金属元素,金属及其化合物在生活生产中有着重要应用,根据试题信息,完成下列计算:
51.某常见二价金属12.6g与足量稀硫酸反应,生成氢气5.04L(S.T.P),该元素原子的摩尔质量为 g/mol。
52.39.32g某金属混合物,由12.32g镁和0.25mol另一种比镁不活泼的金属元素A组成,该混合物与一定量盐酸反应,产生氢气4.928L(S.T.P),则参加反应的HCl为 mol,金属A的相对原子质量为 。
53.由NaCl、NaHCO3、Na2CO3·10H2O组成的混合物157.8g,充分加热后,产生的气体(气体温度150℃)依次通过无水CaCl2和碱石灰,两种吸收剂分别增重59.4g和13.2g,则混合物中NaHCO3的质量分数为 ,若等质量的该混合物与足量盐酸反应,产生二氧化碳(S.T.P) L。
54.将一包铝热剂(铝粉和氧化铁的混合物)进行如下实验
①向一份铝热剂中加入800mL 2.0mol/L的NaOH溶液,使其充分反应后,收集到的气体体积为20.16L(S.T.P)。
②另一份等质量的铝热剂在高温下充分反应后,向反应后固体中加入2L 2.5mol/L的盐酸溶液,使固体完全溶解,反应后溶液pH=0(假设过程中溶液体积不变),取少量反应后溶液,滴加硫氰化钾,没有出现血红色。完成下列计算:
(1)计算该铝热剂中铝与氧化铁物质的量之比。
(2)实验②产生的气体体积是多少(S.T.P)?
 粤公网安备 44130202000953号
粤公网安备 44130202000953号