常温下,用0.1000 mol·L-1 NaOH溶液滴定20.00 mL 0.1000 mol·L-1 CH3COOH溶液所得滴定曲线如下图。下列说法正确的是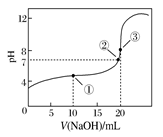
| A.点①所示溶液中:c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+) |
| B.点②所示溶液中:c(Na+)=c(CH3COOH)+c(CH3COO-) |
| C.滴定过程中可能出现:c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-) |
| D.点③所示溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) |
下列溶液中各微粒的浓度关系不正确的是( )
| A.0.1mol•L-1HCOOH溶液中:c(HCOO-)+c(OH-)=c(H+) |
| B.1L0.1mol•L-1CuSO4·(NH4)2SO4•6H2O的溶液中:c(SO42-)>c(NH4+)>c(Cu2+)>c(H+)>c(OH-) |
| C.0.1mol•L-1NaHCO3溶液中:c(Na+)+c(H+)+c(H2CO3)≠c(HCO3-)+c(CO32-)+c(OH-) |
| D.等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液中:c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-) |
下列溶液中微粒的物质的量浓度关系正确的是( )
| A.Ca(ClO)2溶液中:c(Ca2+)>c(ClO-)>c(OH-)>c(H+) |
| B.等体积、等物质的量浓度的NaX和弱酸HX混合:c(Na+)=c(X-)>c(OH-)=c(H+) |
| C.常温下,将25mL0.2mol/L的盐酸与100mL0.1mol/L的氨水混合,所得溶液中: c(Cl-)>c(NH4+)> c(NH3·H2O)>c(OH-)>c(H+) |
| D.将0.1mol/L的Na2S溶液与0.1mol/L的NaHS溶液等体积混合,所得溶液中: |
c(S2-)+2c(OH-)=2c(H+)+c(HS-)+3c(H2S)
次氯酸可用于杀菌消毒。已知25°C时:
①HClO(aq)+OH-(aq)= ClO-(aq)+ H2O(l) ΔH=-Q1kJ·mol-1
②H+(aq) +OH-(aq) = H2O(l) ΔH=-57.3kJ·mol-1
下列说法正确的是
A.在25°C时,次氯酸的电离方程式及热效应可表示为:HClO(aq)  H+(aq)+ClO-(aq) ΔH=-(57.3+Q1)kJ·mol-1 H+(aq)+ClO-(aq) ΔH=-(57.3+Q1)kJ·mol-1 |
| B.将20ml 1mol/L HClO与10ml 1mol/L NaOH混合后的溶液,一定存在:2C(H+)-2C(OH-)=C(ClO-)-C(HClO) |
| C.已知酸性H2SO3>HClO>HSO3-, 则向Na2SO3溶液中加入HClO的离子方程式为:SO32-+ HClO= HSO3-+ ClO- |
| D.已知酸性CH3COOH>HClO,则等浓度CH3COONa和NaClO的混合液中:C(Na+)> C(ClO-)> C(CH3COO-)> C(OH-)> C(H+) |
0.1 mol•L-1 KHCO3溶液中下列表达式不正确的是
| A.c(K +)+c(H+)= c(OH-)+ c(HCO3-)+2 c(CO32-) |
| B.c(K+)> c (HCO3-)> c(OH-)> c(CO32-)> c(H+) |
| C.c(HCO3-)+ c(CO32-)+ c(H2 CO3)=" 0.1" mol•L-1 |
| D.c(K+)> c(HCO3-)> c(OH-)> c(H+)> c(CO32-) |
常温下,0.1mol/L Na2CO3溶液中各微粒浓度关系正确的是
| A.c(Na+)>c(CO32-)>c(HCO3-)>c(H2CO3) |
| B.c(Na+)>c(CO32-)>c(H+)>c(OH—) |
| C.c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-) |
| D.c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
下列叙述正确的是
A.0.1mol·L-1氨水中,c(OH-)=c(NH4+)
B.在0.1mol·L-1CH3COONa溶液中,c(OH-)=c(CH3COOH)+c(H+)
C.等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液中:c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-)
D.0.1mol·L-1某二元弱酸强碱盐NaHA溶液中,c(Na+)=2c(A2-)+c(HA-)+c(H2A)
草酸是二元弱酸,草酸氢钾溶液呈酸性。在O.1mol·L-1 KHC2O4溶液中,下列关系正确的是
| A.c(HC2O4-)+c(C2O42-)="0.1" mol·L-1 |
| B. c(C2O42—)>c(H2C2O4) |
| C.c(K+)=2c(H2C2O4)+2c(HC2O4-)+2c(C2O42—) |
| D.c(K+)+c(H+)=c(HC2O4—)+c(OH—)+c(C2O42-) |
25oC时,取浓度均为0.1mol·L-1的醋酸溶液和氨水溶液各20 mL,分别用0.1mol·L-1NaOH溶液、0.1 mol·L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示。
下列说法正确的是
| A.曲线I中滴加溶液到10 mL时:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| B.曲线I中滴加溶液到25 mL时:c(NH4+)>c(C1-)>c(H+)>c(OH-) |
| C.曲线II中滴加溶液在10 mL~25 mL之间存在:c(NH4+)=c(Cl-)>c(OH-)=c(H+) |
| D.曲线II中滴加溶液到10mL时:c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)] |
某酸性溶液中只有Na+、CH3COO-、H+、OH-四种离子。则下列描述正确的是
| A.该溶液由pH=3的CH3COOH与pH=11的NaOH溶液等体积混合而成 |
| B.该溶液由等物质的量浓度、等体积的NaOH溶液和CH3COOH溶液混合而成 |
| C.加入适量NaOH,溶液中离子浓度为c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
| D.加入适量氨水,c(CH3COO-)一定大于c(Na+)、c(NH4+)之和 |
部分弱酸的电离平衡常数如下表:
| 弱酸 |
HCOOH |
HCN |
H2CO3 |
| 电离平衡常数 (25℃) |
Ka=1.77×10-4 |
Ka=4.9×10-10 |
Ka1=4.3×10-7 Ka2=5.6×10-11 |
下列选项正确的是
A.2CN-+H2O+CO2=2HCN+CO32-
B.中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者大于后者
C.物质的量浓度相等的HCOONa和KCN溶液中,c(Na+)-c(HCOO-) < c(K+)-c(CN-)
D.c(NH4+) 相等的HCOONH4溶液、NH4CN溶液、NH4HCO3溶液中,c(NH4HCO3)>c(NH4CN) >c(HCOONH4)
下列说法正确的是
| A.Na2CO3溶液中c(Na+)与c(CO32-)之比为2:1 |
| B.pH=2与pH=1的硝酸中c(H+)之比为1:10 |
| C.0.2 mol•L-1与0.1mol/L醋酸中c(H+)之比为2:1 |
| D.相同体积的0.1 mol•L-1盐酸和0.1mol/L醋酸分别与足量镁条反应,放出H2的体积比大于1:1 |
常温下,向20mL 0.10mol·L-1 NaHCO3溶液中滴加0.10mol·L-1 CaCl2溶液至pH=7,有白色沉淀生成,无气体放出。对反应所得混合液的下列说法错误的是
| A.存在电离平衡、水解平衡和沉淀溶解平衡 |
| B.c(Na+)=c(Cl-)>c(HCO3-)>c(CO32-)=c(Ca2+) |
| C.c(Na+)+2c(Ca2+)=c(HCO3-)+2c(CO32-)+c(Cl-) |
| D.反应的离子方程式:2 HCO3-+Ca2+==CaCO3↓+H2CO3 |
下表是在相同温度下三种酸的一些数据,下列判断正确的是( )
| 酸 |
HX |
HY |
HZ |
||
| 浓度(mol/L) |
0.12 |
0.2 |
0.9 |
1 |
1 |
| 电离度 |
0.25 |
0.2 |
0.1 |
0.3 |
0.5 |
| 电离常数 |
K1 |
K2 |
K3 |
K4 |
K5 |
A.在相同温度,从HX的数据可以说明:弱电解质溶液,浓度越低,电离度越大,且K1>K2>K3=0.01
B.室温时,若在NaZ溶液中加水,则c(Z−)/[c(HZ)⋅c(OH−)]的比值变小,若加少量盐酸,则比值变大
C.等物质的量的NaX、NaY和NaZ的混合,c(X−)+c(Y−)−2c(Z−)=2c(HZ)−c(HX)−c(HY),且c(Z−)<c(Y−)<c(X−)
D.在相同温度下,K5>K4>K3