室温下,将0.100 0 mol·L-1盐酸滴入20.00 mL 未知浓度的某一元碱MOH溶液中,溶液pH随加入盐酸体积变化曲线如右图所示。下列有关说法不正确的是( )

| A.该一元碱溶液浓度为0.100 0 mol·L-1 |
| B.a、b、c点的水溶液导电性依次增强 |
| C.室温下,MOH的电离常数Kb=1×10-5 |
| D.b点:c(M+)+c(MOH)=c(Clˉ) |
某学生用0.1000 mol•L-1NaOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
A.用蒸馏水洗干净滴定管
B.用待测定的溶液润洗酸式滴定管
C.用酸式滴定管取稀盐酸 20.00mL,注入锥形瓶中,加入酚酞.
D.另取锥形瓶,再重复操作一次
E.检查滴定管是否漏水
F.取下碱式滴定管用标准的KOH溶液润洗后,将标准液注入碱式滴定管刻度“0”以上2-3cm处,再把碱式滴定管固定好,调节液面至刻度“0”或“0”刻度以下
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度
完成以下填空:
(1)正确操作的顺序是_________
A.EABCFGD B.CABEFGD
(2)滴定时边滴边摇动锥形瓶,眼睛应观察________
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
(3)滴定结果如表所示:
| 滴定次数 |
待测液体积/mL |
标准溶液的体积/mL |
||
| |
滴定前刻度 |
滴定后刻度 |
||
| 1 |
20 |
1.02 |
21.03 |
|
| 2 |
20 |
2.00 |
25.00 |
|
| 3 |
20 |
0.60 |
20.60 |
|
滴定中误差较大的是第___________次实验,造成这种误差的可能原因是_______;
A.碱式滴定管在装液前未用标准NaOH溶液润洗2~3次
B.滴定开始前碱式滴定管尖嘴部分有气泡,在滴定终点读数时未发现气泡
C.滴定开始前碱式滴定管尖嘴部分没有气泡,在滴定终点读数时发现尖嘴部分有气泡
D.达到滴定终点时,仰视溶液凹液面最低点读数
E.滴定过程中,锥形瓶摇荡得太剧烈,以致有些液滴飞溅出来
(4)该盐酸的浓度为_______mol/L。
(5)如果准确移取20.00mL 0.1000mol/L NaOH溶液于锥形瓶中,滴入酚酞指示剂,然后用未知浓度的盐酸(装在酸式滴定管中)滴定,是否也可测定出盐酸的物质的量浓度?_______(填“是”或“否”)。
(1)今有①CH3COOH ②HCl ③H2SO4三种溶液,当它们温度相同、pH相同时,其物质的量浓度由大到小排列的顺序是 (用序号表示)。
(2)某温度下,纯水中的c(H+)=2.0×10-7mol/L,则此时溶液中c(OH-)为__________mol/L。
(3)在25℃下,向浓度均为0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,请写出最先生成沉淀的离子方程式为 。
(已知25℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20)。
(4)下列说法不正确的是 (填序号)。
| A.用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小 |
| B.物质的溶解度随温度的升高而增加,故物质的溶解都是吸热的 |
| C.除去氯化钠溶液中的Mg2+,用NaOH溶液沉淀Mg2+比用Na2CO3溶液效果好,说明相同温度时Mg(OH)2的溶解度比MgCO3大 |
| D.沉淀反应中常加适当过量的沉淀剂,其目的是使相关离子沉淀完全 |
t℃时,某NaOH稀溶液中,c(H+ )=10-amol·L-1,c(OH-)=10-bmol·L-1,已知a+b=13, 则在该温度下,将100 mL0.10 mol·L-1的稀硫酸与100 mL0.40 mol·L-1的NaOH溶液混合后,溶液的pH为( )(已知:忽略溶液混合时体积的变化;lg2=0.30;lg3=0.48)
| A.12.00 | B.11.82 | C.11.70 | D.11.52 |
测血钙的含量时,可将2 mL血液用蒸馏水稀释后,向其中加入足量草酸铵(NH4)2C2O4晶体,反应生成CaC2O4沉淀。将沉淀用稀硫酸处理得H2C2O4后,再用酸性KMnO4溶液滴定,氧化产物为CO2,还原产物为Mn2+,若终点时用去20mL 1.0×10-4 mol·L-1的KMnO4溶液。
(1)写出用KMnO4滴定H2C2O4的离子方程式 。
(2)判断滴定终点的方法是 。
(3)计算:血液中含钙离子的浓度为 mol/L。
(1)25℃时,浓度为0.1mol•L-1的6种溶液,①HCl ②CH3COOH ③Ba(OH)2 ④Na2CO3 ⑤KCl ⑥NH4Cl溶液pH由小到大的顺序为_____________(填写编号);
(2)25℃时,醋酸的电离常数Ka=1.7×10-5 mol•L-1,则该温度下CH3COONa的水解平衡常数Kh="_____" mol•L-1 (保留到小数点后一位)
(3)25℃时,pH=3的醋酸和pH=11的NaOH溶液等体积混合,溶液呈_________(“酸性”、“中性”、“碱性”),请写出溶液中的电荷守恒式:_______________。
某学生用0.1000mol/L盐酸标准溶液测定某烧碱样品的纯度(杂质不与盐酸反应)。实验步骤如下:
(1)配制待测液:用2.50g含有少量杂质的固体烧碱样品配制500mL溶液。需用的玻璃仪器除了烧杯、胶头滴管、玻璃棒外,还需要___________。
(2)滴定:
Ⅰ.用蒸馏水洗涤酸式滴定管,并立即注入盐酸标准溶液至“0”刻度线以上。
Ⅱ.固定好滴定管并使滴定管尖嘴充满液体,调节液面至“0”刻度线以下,并记录读数。
Ⅲ.移取20.00mL待测液注入洁净的锥形瓶中,并加入2滴酚酞试液。
Ⅳ.用标准液滴定至终点,记录滴定管液面读数。
①上述滴定步骤中有错误的是(填编号)____________。该错误操作会导致测定结果___________(填“偏大”、“偏小”或“无影响”)。
②排去碱式滴定管中气泡的方法应采用右图的___________操作。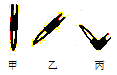
③步骤Ⅳ中滴定时眼睛应____________;判断滴定终点的现象是_____________。
④若步骤Ⅱ中仰视读数,步骤Ⅳ中俯视读数,则会使测定结果___________(填“偏大”、“偏小”或“无影响”)
(3)按正确操作测得有关数据记录如下:按正确操作测得有关数据记录如下:
| 滴定次数 |
待测液体积 |
标准盐酸体积(mL) |
|
| 滴定前读数(mL) |
滴定后读数(mL) |
||
| 第一次 |
20.00 |
0.20 |
20.38 |
| 第二次 |
20.00 |
4.00 |
24.20 |
| 第三次 |
20.00 |
2.38 |
a |
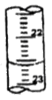
①a的读数如图所示,则a=___________;②烧碱样品的纯度为_________ %
在某NaHSO4溶液中离子的总浓度为0.06mol•L-1,若其中加入等体积离子总浓度为0.06mol•L-1的Ba(OH)2溶液,混合后溶液的体积不变,则溶液的pH值为
| A.2 | B.1.7 | C.12 | D.12.3 |
氨气在工农业生产中有重要应用。
Ⅰ. (1)如下图所示,向NaOH固体上滴几滴浓氨水,迅速盖上盖,观察现象。

①浓盐酸液滴附近会出现白烟,发生反应的化学方程式为_____________________。
②FeSO4液滴中先出现灰绿色沉淀,过一段时间后变成红褐色,发生的反应包括Fe2++2NH3·H2O=Fe(OH)2↓+2NH和________________________。
(2)已知氨气极易溶于水,而难溶于有机溶剂CCl4。下列装置中不适宜做氨气尾气吸收的是 。

Ⅱ.现代传感信息技术在化学实验中有广泛的应用。

某小组用传感技术测定喷泉实验中的压强变化来认识喷泉实验的原理(图1)。
(1)关闭a,将吸有2mL水的胶头滴管塞紧颈口c,打开b,完成喷泉实验,电脑绘制三颈瓶内气压变化曲线(图2)。图2中 点时喷泉最剧烈。
(2)从三颈瓶中量取25.00mL氨水至锥形瓶中,加入 做指示剂;用0.0500 mol•L-1HCl滴定。终点时溶液颜色由 色变为 色,用pH计采集数据、电脑绘制滴定曲线如下图。

(3)据图,计算氨水的浓度为 mol•L-1;比较当VHCI=17.50ml时溶液中离子浓度大小关系 。
(4)关于该滴定实验的说法中,正确的是 。
| A.锥形瓶中有少量蒸馏水导致测定结果偏低 |
| B.酸式滴定管在滴定前有气泡,滴定后气泡消失测得氨水的浓度偏高 |
| C.酸式滴定管未用盐酸润洗会导致测得氨水的浓度偏高 |
| D.滴定终点时俯视读数会导致测得氨水的浓度偏低 |
常温下下列各组离子在指定溶液中能大量共存的是( )
| A.pH=1 的溶液中:Fe2+、NO-3、SO24-、Na+ |
| B.由水电离出的 c(H+)=1×10-14mol/L 的溶液中:Ca2+、Cl-、HCO-3、K+ |
| C.c(H+)/c(OH-)=1×1012的溶液中:NH+4、Cl-、NO-3、Al3+ |
| D.c(Fe3+)=0.1mol/L 的溶液中:K+、ClO-、SO42-、SCN- |
一定温度下,水溶液中H+和OH-的浓度变化曲线如图,下列说法正确的是( )
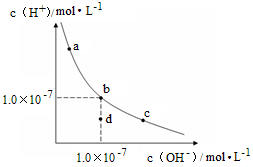
| A.升高温度,可能引起由c向b的变化 |
| B.该温度下,水的离子积常数为1.0×10-13 |
| C.该温度下,加入FeCl3可能引起由b向a的变化 |
| D.该温度下,稀释溶液可能引起由c向d的变化 |
A、B、C、D、E五种溶液分别是NaOH溶液、氨水、醋酸、盐酸、NH4HSO4溶液的一种。常温下进行下列实验:
①B、D均能与pH=3的A溶液反应,当它们以等物质的量混合时均能恰好反应,反应后得到的溶液前者呈酸性,后者呈中性;
②浓度均为0.1mol/LC与D溶液等体积混合,溶液呈酸性.
回答下列问题:
(1)D是__________,(填化学式,下同)E是__________;
(2)将等体积、等物质的量浓度B和C混合后溶液,升高温度(溶质不会分解)溶液pH随温度变化如图中__________曲线(填写序号).
(3)室温下,向0.01mol/LC溶液中滴加0.01mol/LD溶液至中性,得到的溶液中所有离子的物质的量浓度由大到小的顺序为__________.
(4)写出C的稀溶液和足量的D溶液反应的离子方程式______________________。
滴定实验是化学学科中重要的定量实验。请回答下列问题:
(1)酸碱中和滴定——用标准盐酸滴定未知浓度的NaOH溶液。
①酸式滴定管、碱式滴定管、温度计、量筒、玻璃棒、烧杯。若要进行中和滴定实验,还缺少的玻璃仪器是_________________。
②上述滴定过程中操作滴定管的图示,正确的是____________。
③若在接近滴定终点时,用少量蒸馏水将锥形瓶内壁冲洗一下,再继续滴定至终点,则所测得NaOH溶液浓度_________________(填“偏大”、“偏小”或“无影响”)。
(2)氧化还原滴定——用标准高锰酸钾溶液滴定未知浓度的草酸(H2C2O4)溶液。
①课外小组里有位同学设计了下列两种滴定方式(夹持部分略去),引起了同学们的讨论,最后取得共识,你认为合理的是___________________(填字母符号)。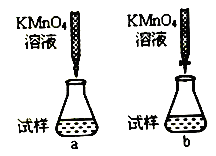
②判断滴定终点的依据是____________。
③某次滴定时记录滴定前滴定管内液面读数为0.50mL,滴定后液面如下图,则此时消耗标准溶液的体积为______________。
水溶液中的行为是中学化学的重要内容。
(1)25 ℃时,某溶液中由水电离出c(H+)=1×10-10 mol/L,该溶液pH为_______________。
(2)25 ℃时,测得亚硫酸氢钠溶液的pH<7,解释该溶液显酸性的原因(用离子方程式表示,并作适当解释) 。
(3)电离常数是衡量弱电解质电离程度强弱的物理量。已知:
| 化学式 |
电离常数(25 ℃) |
| HCN |
K=4.9×10-10 |
| HClO |
K=3×10-8 |
| H2CO3 |
K1=4.3×10-7、K2=5.6×10-11 |
25 ℃时,将浓度相同的四种盐溶液:① NaCN ② NaClO ③ Na2CO3 ④ NaHCO3,按pH由大到小的顺序排列 (填序号),向84消毒液中通入少量的CO2,该反应的化学方程式为 。
(4)25 ℃时,将n mol·L-1的氨水与0.2mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-),则溶液显_______________性(填“酸”、“碱”或“中”), NH3·H2O的电离常数Kb=_____________(用含n的代数式表示)。
(1)化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1 mol化学键时释放(或吸收)的能量。已知:N≡N键的键能是948.9kJ·mol-1,H-H键的键能是436.0 kJ·mol-1;由N2和H2合成1mol NH3时可放出46.2kJ的热量。N-H键的键能是_________
(2)由氢气和氧气反应生成1mol水蒸气,放热241.8KJ。写出该反应的热化学方程式:① 。
已知常温下NO与O2反应生成1molNO2的焓变为-57.07KJ,1molNO2与H2O反应生成HNO3溶液和NO的焓变为-46KJ,写出NO与O2及水生成HNO3溶液的热化学方程式② 。
(3)某温度下纯水中的c(H+) = 2×10-7mol/L,则此时c(OH-) =________mol/L,该纯水的pH_______(填“>7”、“<7”、“=7”)。若温度不变,滴入稀硫酸使c(H+) = 5×10-6mol/L,则c(OH-) =________mol/.
(4)纳米MgO可用于尿素与氯化镁合成。某小组研究该反应在温度为378~398K时的反应时间、反应物配比等因素对其产率的影响。请完成以下实验设计表:
| 编号 |
温度/K |
反应时间/h |
反应物物质的量配比 |
实验目的 |
| ① |
378 |
3 |
3:1 |
实验②和④探究a 实验②和b 探究反应时间对产率的影响 |
| ② |
378 |
4 |
4:1 |
|
| ③ |
378 |
3 |
c |
|
| ④ |
398 |
4 |
4:1 |