⑴有下列四种溶液:①100mL 0.1mol/L H2SO4溶液;②100mL 0.15mol/L HCl溶液 ③100mL 0.2mol/L CH3COOH溶液;④200mL 0.1mol/L CH3COOH溶液。
其中pH最小的是 (填序号,下同),由水电离的H+浓度最大的是 ,与足量的Zn反应,生成H2最少的是 ;①和③分别与100mL 0.2mol/L NaOH溶液反应,放出热量少的是 ,理由是 。
⑵实验室中有一未知浓度的稀盐酸,某学生用0.10 mol·L-1 NaOH标准溶液进行测定盐酸的浓度的实验。该学生取20.00 mL待测盐酸放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用NaOH标准溶液进行滴定。滴定达到终点的标志是 ;在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有________(填字母序号)。
| A.滴定终点读数时俯视 |
| B.酸式滴定管使用前,水洗后未用待测盐酸润洗 |
| C.锥形瓶水洗后未干燥 |
| D.称量NaOH固体中混有Na2CO3固体 |
E.碱式滴定管尖嘴部分有气泡,滴定后消失
常温下pH为2的盐酸,下列叙述正确的是
| A.该溶液中盐酸电离出的c(H+)与水电离出的c(H+)之比为1010∶1 |
| B.向该溶液中加入等体积pH为12的氨水恰好完全中和 |
| C.将10 mL该溶液稀释至100 mL后,pH小于3 |
| D.该溶液中由水电离出的c(H+)水×c(OH-)水=1×10-14 |
下列说法正确的是
| A.pH=11的氨水与pH=3的盐酸等体积混合:c(Cl-)=c(NH4+)>c(OH-)=c(H+) |
| B.0.2mol/L的CH3COOH溶液与0.1mol/L的NaOH溶液等体积混合:2c(Na+)=c(CH3COO-) |
| C.浓度均为0.10mol/L的氨水和氯化铵溶液等体积混合后:c(NH3·H2O)+c(NH4+)=0.1mol/L |
| D.pH=3的盐酸和pH=11的氢氧化钡等体积混合pH>7 |
下列说法正确的是
| A.室温下用广范pH试纸测得某氯水的pH=4 |
| B.酸式滴定管的润洗操作:关闭滴定管活塞,往上口加入3~5mL待装液,倾斜着转动滴定管,使液体润湿滴定管内壁,然后将液体从上口倒出,重复此操作2~3次 |
| C.若酸碱中和滴定过程中用待测液润洗锥形瓶,则测定结果偏高 |
| D.酸碱中和滴定的终点是指酸和碱恰好完全反应,此时溶液一定呈中性 |
下列溶液一定呈酸性的是
| A.pH=6.8的溶液 |
| B.由水电离的OH-离子浓度为1×10-13 mol/L |
| C.加入酚酞,不显红色的溶液 |
| D.常温下,溶液中的H+离子浓度为5×10-7 mol/L |
现用物质的量浓度为a mol·L-1的标准NaOH溶液去滴定V mL盐酸的物质的量浓度,请填写下列空白:
(1)碱式滴定管用蒸馏水洗净后,接下来应该进行的操作是________________。
(2)用标准NaOH溶液滴定时,应将标准NaOH溶液注入________(填“甲”或“乙”)中。
(3)如图是碱式滴定管中液面在滴定前后的读数,c(HCl)________mol·L-1。
常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表,请回答:
| 实验编号 |
HA物质的量浓度/(mol·L-1) |
NaOH物质的量浓度/(mol·L-1) |
混合溶液的pH |
| 甲 |
c |
0.2 |
pH=7 |
| 乙 |
0.2 |
0.1 |
pH>7 |
| 丙 |
0.1 |
0.1 |
pH=9 |
(1)不考虑其它组的实验结果,单从甲组情况分析,c是否一定等于0.2________(选填“是”或“否”)。
(2)单从乙组实验结果分析,HA是________酸(选填“强”或“弱”)。该混合溶液中离子浓度由大到小的顺序是_______________。
(3)丙组实验所得混合溶液中下列算式的精确结果:c(OH-)-c(HA) =_________mol/L。
25℃时,下列各组离子在特定溶液中一定能大量共存的是( )
| A.由水电离的c(H+)=1×10﹣14mol•L﹣1的溶液中:Ca2+、K+、Cl﹣、HCO3﹣ |
| B.甲基橙呈红色的溶液:NH4+、Ba2+、AlO2﹣、Cl﹣ |
| C.在pH=0的溶液中:Na+、NO3﹣、SO32﹣、K+ |
| D.pH=12的溶液:K+、Na+、CH3COO﹣、Br﹣ |
若1体积硫酸恰好与10体积pH=11的氢氧化钠溶液完全反应,则二者的物质的量浓度值比应为( )
| A.10:1 | B.5:1 | C.1:1 | D.1:10 |
某同学用中和滴定法去测定某烧碱的纯度,实验过程如下:
(1)配制待测液称取得 5.0g 固体烧碱样品(杂质不与酸反应)配制成 250 mL 溶液,
(2)用 0.2000 mol·L-1标准盐酸滴定待测烧碱溶液,实验操作如下
| A.用碱式滴定管取上述烧碱溶液10.00 mL,注入锥形瓶中,加入指示剂。 | B.用待测定 的溶液润洗碱式滴定管。 | C.用蒸馏水洗干净滴定管。 | D.取下酸式滴定管用标准的盐酸 溶液润洗后,将标准液注入酸式滴定管刻度“0”以上2~ 3 cm处,再把酸式滴定管固定好, 调节液面至刻度“0”或“0”刻度以下。E.检查滴定管是否漏水。F.另取锥形瓶,再重复 操作一次。G.把锥形瓶放在滴定管下面,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面的刻度。 |
①滴定操作的正确顺序是(用序号填写):________________
②该滴定操作中应选用的指示剂是:________________
③在G操作中如何确定终点?________________
(3)数据处理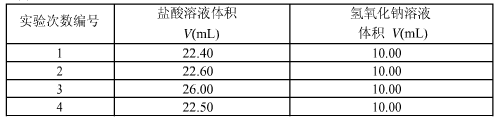
根据上述各数据,选取合适的三组,计算待测烧碱溶液的浓度为__________,烧碱的纯度为_________。
(4)下列操作,会导致实验结果偏低的是________(填序号)。
①碱式滴管用蒸馏水洗净后没有用待测液润洗 ②锥形瓶用蒸馏水洗净后没有用待测液润洗 ③终点读数时俯视(滴定前读数准确) ④酸式滴定管尖端气泡没有排除,滴定后消失 ⑤振荡时锥形瓶中液滴飞溅出来 ⑥酸式滴定管用蒸馏水洗净后没有用标准液润洗
欲用0.2000mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,下列有关说法正确的是
| A.滴定管在装溶液前,先用蒸馏水洗涤干净后,再用待装溶液润洗 |
| B.锥形瓶在装待测溶液前,先用蒸馏水洗涤干净后,再用待装溶液润洗 |
| C.滴定过程中,两眼注视滴定管装液面的变化 |
| D.装标准液的滴定管中有气泡而滴定前未排出,则滴定结果将偏低 |
已知酸H2B在水溶液中存在下列关系:①H2B=H++HB-,②HB- H++B2- ,则下列说法中一定正确的是
H++B2- ,则下列说法中一定正确的是
A、在Na2B溶液中一定有:c(OH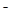 )=c(H
)=c(H )+c(HB
)+c(HB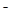 )+2c(H2B)
)+2c(H2B)
B、NaHB溶液可能存在以下关系:c(Na )>c(HB
)>c(HB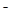 )>c(OH
)>c(OH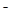 )>c(H
)>c(H )
)
C、NaHB水溶液中一定有:c(Na )+c(H
)+c(H )=c(HB
)=c(HB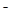 )+c(OH
)+c(OH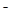 )+c(B
)+c(B )
)
D、NaHB溶液一定呈酸性,Na2B溶液一定呈碱性
25℃时,水的电离达到平衡:H2O H++OH-;DH>0,则下列叙述正确的是
H++OH-;DH>0,则下列叙述正确的是
| A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低 |
| B.向水中加入少量固体硫酸氢钠,c(H+)增大,KW不变 |
| C.向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低 |
| D.将水加热,KW增大,pH不变 |
用0.1000mol·L-1标准NaOH溶液测定食醋中醋酸的含量,下列说法正确的是( )
| A.酸式滴定管、碱式滴定管及锥形瓶均需洗净后再润洗内壁2~3次 |
| B.应该选择酚酞作指示剂 |
| C.滴定过程中眼睛应始终注视滴定管内液面变化 |
| D.读取标准液的刻度时,滴定前平视,滴定后仰视,测定结果偏低 |