陕西省宝鸡市岐山县高二上学期期末理化学试卷
下列反应中,不能形成原电池反应的是
| A.氢氧化钠与盐酸反应 | B.金属锌与稀硫酸反应 |
| C.甲烷燃烧 | D.金属铜溶于氯化铁溶液 |
下列能量变化表示氢气燃烧热的是
| A.H2(g) + 1/2O2(g) = H2O(g)△H =" -241.8" kJ/mol |
| B.2H2(g) + O2(g) = 2H2O(g)△H =" -483.6" kJ/mol |
| C.2H2(g) + O2(g) = 2H2O(l)△H =" -571.6" kJ/mol |
| D.H2(g) + 1/2O2(g) = H2O(l)△H =" -285.8" kJ/mol |
下列溶液中导电性最强的是
| A.5L 0.1mol / L NH3·H2O | B.0.1L 0.2mol / L 盐酸 |
| C.5L 0.1mol / L 醋酸溶液 | D.0.1L 0.1mol / L NaOH溶液 |
下列说法正确的是
| A.水解反应是吸热反应 | B.升高温度可以抑制盐类的水解 |
| C.正盐水溶液pH均为7 | D.硫酸钠水溶液pH小于7 |
对于CH3COOH、HCl、H2SO4三种溶液,下列判断正确的是
| A.pH相同的三种溶液,物质的量浓度最小的是HCl |
| B.物质的量浓度相同的三种溶液,pH最小的是H2SO4 |
| C.含溶质的物质的量相同的三种溶液与过量镁粉反应,CH3COOH产生的H2最多 |
| D.相同pH、相同体积的三种溶液用NaOH溶液完全中和时,消耗NaOH溶液一样多 |
在气体反应中,能使反应物活化分子数和活化分子百分数同时增加的方法是①增加反应物的浓度 ②升高温度 ③移去生成物 ④增大压强 ⑤加入催化剂
| A.①③ | B.①⑤ | C.②⑤ | D.②④ |
如图所示,a、b、c均为石墨电极,d为碳钢电极,通电电解一段时间。假设在电解过程中产生的气体全部逸出,下列说法正确的是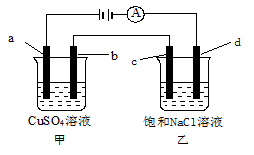
| A.甲、乙两烧杯中溶液的pH均保持不变 |
| B.当b极增重3.2 g时,d极产生的气体为0.56 L(标准状况) |
| C.当电解一段时间后,将甲、乙两溶液混合,一定会产生蓝色沉淀 |
| D.甲烧杯中a电极反应式为:4OH--4e-===O2↑+2H2O |
铜锌原电池(如图)工作时,下列叙述正确的是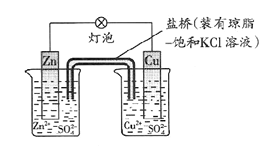
| A.一段时间后铜片增重,盐桥中K+移向CuSO4溶液 |
| B.正极反应为:Zn-2e-=Zn2+ |
| C.电子从铜片经导线流向锌片 |
| D.电池工作时Zn2+和Cu2+ 的浓度保持不变 |
下列叙述正确的是
| A.将纯水加热,水的离子积变大、pH变小、溶液呈酸性 |
| B.Na2CO3溶液加水稀释后,恢复至原温度,pH和Kw均减小 |
| C.pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,c(H+)相等 |
| D.中和体积和pH都相等的HCl溶液和CH3COOH溶液所消耗的NaOH物质的量相同 |
下列电离或离子方程式正确的是
A.亚硫酸的电离:H2SO3 2H++ SO32- 2H++ SO32- |
B.氯化铵水解的离子方程式为: NH4+ +H2O  NH3·H2O + H+ NH3·H2O + H+ |
C.NaHCO3水解的离子方程式为:HCO3-+H2O  CO32-+H3O+ CO32-+H3O+ |
D.向氯化铝溶液中加入过量的氨水:A13++3NH3·H2O Al(OH)3+3NH4+ Al(OH)3+3NH4+ |
欲用0.2000mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,下列有关说法正确的是
| A.滴定管在装溶液前,先用蒸馏水洗涤干净后,再用待装溶液润洗 |
| B.锥形瓶在装待测溶液前,先用蒸馏水洗涤干净后,再用待装溶液润洗 |
| C.滴定过程中,两眼注视滴定管装液面的变化 |
| D.装标准液的滴定管中有气泡而滴定前未排出,则滴定结果将偏低 |
已知:(1)Zn(s)+ 1/2O2(g)= ZnO(s),ΔH =" -350" kJ/mol,
(2)2Ag(s) + 1/2O2(g)= Ag2O(s),ΔH =" -25" kJ/mol,
则Zn(s)+ Ag2O(s) =" ZnO(s)+" 2Ag(s)的ΔH等于
| A.-375 kJ/mol | B.-325 kJ/mol |
| C.+375 kJ/mol | D.+325 kJ/mol |
已知:Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.5×10-16 ,Ksp(AgBr)=7.7×10-13,则下列难溶盐的饱和溶液中,Ag+浓度大小顺序正确的是
| A.AgCl>AgI> AgBr | B.AgBr >AgI>AgCl |
| C.AgBr >AgCl>AgI | D.AgCl> AgBr>AgI |
化学反应都有能量变化,吸热或放热是化学反应中能量变化的主要形式之一。
(1)化学反应中有能量变化的本质原因是反应过程中有 的断裂和形成。
(2)已知拆开1molH-H键、1molCl-Cl键、1molH—Cl键分别需要的能量是436kJ、243kJ、432kJ,则反应H2(g)+ Cl2(g)=2HCl (g) 的△H = 。
(3)已知:CO(g) + 1/2O2(g) = CO2(g) △H = -283.0 kJ/mol
CH3OH(l) + 3/2O2(g) = CO2(g)+2H2O(l) △H = -726.5kJ/mol
则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为 。
(4)已知25℃、101 kPa下,稀的强酸与稀的强碱溶液反应的中和热为 -57.3 kJ/mol。
①表示稀硫酸与稀烧碱溶液中和反应的热化学方程式为 ;
②测定中和热实验中所需的玻璃仪器有烧杯、量筒、环形玻璃搅拌棒、 。
下列四个装置图均与电化学有关,请根据图示回答相关问题:
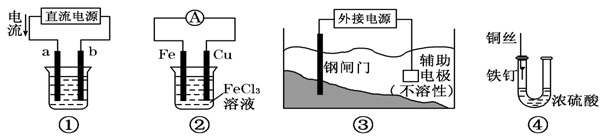
(1)这四个装置中,利用电解原理的是 (填装置序号);
(2)装置①若用来精炼铜,则a极的电极材料是 (填“粗铜”或“精铜”),电解质溶液为 ;
(3)装置②的总反应方程式是 ;
(4)装置③中钢闸门应与外接电源的 极相连(填“正”或“负”)
(5)装置④中的铁钉几乎没被腐蚀,其原因是 。
下表是不同温度下水的离子积的数据。试回答以下问题:
| 温度/℃ |
25 |
t1 |
t2 |
| 水的离子积 |
1×10-14 |
a |
1×10-12 |
(1)若25<t1<t2,则a________1×10-14(填“>”、“<”或“=”),做此判断的理由是 。
(2)25℃时,某Na2SO4溶液中c(SO42-)=5×10-4 mol/L,取该溶液1 mL加水稀释至10 mL,则稀释后溶液中c(Na+)∶c(OH-)= 。
(3)在t2温度下测得某溶液pH=7,该溶液显__________(填“酸”、“碱”或“中”)性,将此温度下pH=11的NaOH溶液a L与pH=1的H2SO4溶液b L混合:
①若所得混合液为中性,则a∶b=____________;
②若所得混合液pH=2,则a∶b=____________。
已知A(g)+B(g)  C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
| 温度/ ℃ |
700 |
800 |
830 |
1000 |
1200 |
| 平衡常数 |
1.7 |
1.1 |
1 |
0.6 |
0.4 |
回答下列问题:
(1)该反应的平衡常数表达式K= ,△H 0(填“<”“ >”“ =”);
(2)830℃时,向一个5 L的密闭容器中充入0.20mol的A和0.80mol的B,如反应初始6s内A的平均反应速率v(A)="0.003" mol·L-1·s-1,则6s时c(A)= mol·L-1, C的物质的量为 mol;若反应经一段时间后,达到平衡时A的转化率为 ,如果这时向该密闭容器中再充入1 mol氩气,平衡时A的转化率为 ;
(3)判断该反应是否达到平衡的依据为 (填正确选项前的字母):
a.压强不随时间改变 b.气体的密度不随时间改变
c.c(A)不随时问改变 d.单位时间里生成C和D的物质的量相等
(4)1200℃时反应C(g)+D(g)  A(g)+B(g)的平衡常数的值为 。
A(g)+B(g)的平衡常数的值为 。
 2NO(g),在2000℃时K=6.2×10-4。2000℃时,向10L密闭容器中放入3×10-3molNO、2.50×10-1molN2和4.00×10-2molO2。
2NO(g),在2000℃时K=6.2×10-4。2000℃时,向10L密闭容器中放入3×10-3molNO、2.50×10-1molN2和4.00×10-2molO2。 粤公网安备 44130202000953号
粤公网安备 44130202000953号