下列表示对应化学反应的离子方程式正确的是
| A.醋酸除去水垢中的CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑ |
| B.碘水中通入足量的SO2:I2 +SO2+2H2O=2I-+SO42-+4H+ |
| C.NaHSO4溶液与Ba(OH)2溶液反应至中性:H++SO42-+Ba2++OH-=BaSO4↓+H2O |
| D.惰性电极电解MgCl2溶液:Cl-+2H2O = 2OH-+H2↑+Cl2↑ |
下列热化学方程式或离子方程式中,正确的是
| A.氯化镁溶液与氨水反应:Mg2+ + 2OH- = Mg(OH)2 ↓ |
| B.500℃、30MPa下,将0.5molN2和1.5mol H2置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为: N2(g) + 3H2(g)  2NH3(g)△H= -38.6kJ·mol-1 2NH3(g)△H= -38.6kJ·mol-1 |
| C.甲烷的标准燃烧热△H= -890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为: CH4(g) + 2O2(g) = CO2(g)+2H2O(g) △H= -890.3kJ·mol-1 |
| D.氧化铝溶于NaOH溶液:Al2O3 + 2OH- =2AlO2- + H2O |
下列电离方程式正确的是
A.NaHSO4 Na++H++SO42- Na++H++SO42- |
B.HCO3-+H2O=== H3O++CO32- |
| C.HClO===H++ClO- | D.H2S H++HS- H++HS- |
下列相关反应的离子方程式书写错误的是
| A.在强碱溶液中NaClO与Fe(OH)3反应生成Na2FeO4:3ClO—+4OH—+2Fe(OH)3=3Cl—+5H2O+2FeO42— |
| B.少量SO2通入苯酚钠溶液中:2C6H5O—+SO2+H2O=2C6H5OH+SO32— |
| C.用稀硫酸酸化的KMnO4溶液与H2O2反应:2MnO4—+6H++5H2O2=2Mn2++5O2↑+8H2O |
| D.少量SO2通入NaClO溶液中:SO2+ClO—+OH—=SO42—+Cl—+H+ |
工业上可用以下方案使饮用水中NO3-含量达标。

请回答下列问题:
(1)调节pH不宜过大或过小,否则会造成Al的利用率降低;试剂X可选用________(填序号)。
A NaOH B Ca(OH)2 C NH3.H2O D CuO E CO2
(2)流程中操作①的名称为__________,若在实验室中进行此操作,所需要的玻璃仪器是___________。
(3)写出溶液中铝粉和NO3-反应的离子方程式:______________________。
(4)还可用以下化学反应使饮用水中NO3-含量达标,产物之一是空气的主要成分。完成下列离子方程式:

铁及其化合物有丰富多彩的化学性质。回答下列问题:
(1)铁元素在周期表中的位置为第___________周期第__________族。
(2) FeCl3溶液可用于吸收尾气中的SO2,写出该反应的离子方程式:_____________。
(3)某化学兴趣小组同学用下图装置,充分加热硫酸亚铁晶体(FeSO4.xH2O)至完全分解。
①装置A中需持续通入N2,其目的是
②充分反应一段时间后,小组同学观察到实验现象为:装置A中残留有红棕色固体,装置B中固体变蓝,C中溶液褪色,请写出FeSO4分解的化学方程式:________。
③装置D中干燥管的作用为__________。
④小组同学利用数字化实验仪器测定了不同温度时FeSO4.xH2O分解的质量变化情况,得到下
图关系:
实验结束后后,装置B质量增加12. 6g,结合上图数据,确定FeSO4·xH2O中的x=
金属铈(58Ce)常用于制作稀土磁性材料,可应用于制造玻璃、打火石、陶瓷和合金等。已知:Ce4++Fe2+=Ce3+ +Fe3+。下列说法正确的是
| A.可用电解熔融CeO2制取金属铈,铈在阳极生成 |
B.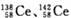 是同素异形体 是同素异形体 |
| C.铈能溶于HI溶液,发生反应的离子方程式为:Ce+4H+=Ce4++2H2 |
| D.铈的原子核外有58个电子 |
在以下各种情形下,下列电离方程式的书写正确的是 ( )。
| A.熔融状态下的NaHSO4电离:NaHSO4===Na++H++SO42- |
B.Fe(OH)3的电离:Fe(OH)3 Fe3++3OH- Fe3++3OH- |
C.H2CO3的电离:H2CO3 2H++CO32- 2H++CO32- |
| D.水溶液中的NaHSO4电离:NaHSO4===Na++HSO4- |
浅黄色粉末A跟无色液体B反应有无色气体C产生,金属D在C中燃烧可生成A,D跟B反应放出气体E,E和C又化合为B。从以上实验现象可判断(用化学式填空):
(1)A ,B ,C ,D ,E ;
(2)A与B反应的化学方程式为 ,此反应中 是氧化剂, 是还原剂;
(3)金属D在C中燃烧的化学方程式为 ,D与B反应的离子方程式为 。
(1)鉴别NaCl溶液和Na2CO3溶液的试剂是_________,离子方程式为____________________。
(2)除去混在NaCl溶液中少量NaHCO3杂质的试剂是________,离子方程式为 ______。
(3)除去Na2CO3粉末中混入的NaHCO3杂质用________方法,化学方程式为______________________。
下列电离方程式错误的是( )
| A.KNO3 = K+ + NO3- | B.NaHSO4 = Na+ + H+ + SO42- |
| C.BaCl2 = Ba2+ + Cl2- | D.Na2SO4 = 2Na+ + SO42- |
(1)PH=10的Na2CO3溶液、NaOH溶液和PH=4的NH4Cl溶液、HCl溶液中水的电离程度的大小关系是 。(用化学式表示)
(2)对于Ag2S(s)  2Ag+(aq)+ S2-(aq),其Ksp=____________。
2Ag+(aq)+ S2-(aq),其Ksp=____________。
(3)NH4HSO4的电离方程式为
(1)某校学生用中和滴定法测定某NaOH溶液的物质的量浓度。
①盛装0.2000 mol/L盐酸标准液应选用的滴定管是_________(填字母序号)。
②当接近滴定终点时,很少量的碱或酸就会引起溶液的 突变。
③有关数据记录如下:
| 实验编号 |
待测液体积(mL) |
所消耗盐酸标准液的体积(mL) |
|
| 滴定前 |
滴定后 |
||
| I |
20.00 |
0.50 |
20.70 |
| II |
20.00 |
6.00 |
26.00 |
| III |
20.00 |
1.40 |
21.20 |
根据数据计算NaOH溶液的物质的量浓度是______________mol/L。
④若只用蒸馏水冲洗锥形瓶,则测定结果_________(填“无影响”.“偏高”或“偏低”)。
(2)25℃,将一元酸HA溶液和NaOH的溶液等体积混合,两种溶液的浓度和混合后溶液的pH见下表:
| 实验编号 |
c(HA)/mol﹒L-1 |
c(NaOH)/mol﹒L-1 |
混合溶液的pH |
| I |
0.2 |
0.2 |
pH=a |
| II |
c1 |
0.2 |
pH=7 |
| III |
0.2 |
0.1 |
pH>7 |
| IV |
0.1 |
0.1 |
pH=9 |
请回答:
①不考虑其它组实验结果,单从I组实验情况分析,若a_____7(填“>”“<”或“=”),则HA为强酸。
②在II组实验的混合溶液中,c(A-)______ c(Na+)(填“>”“<”或“=”)。
③不考虑其它组实验结果,单从III组实验情况分析,HA是_____酸(填“强”或“弱”);用离子方程式表示混合溶液中存在的两种平衡:_________________,____________________。
④IV组实验的混合溶液中,由水电离出的c (OH-)=___________。
(现有下列6种物质:①稀豆浆 ②K2CO3溶液③Cl2 ④SO2 ⑤稀盐酸 ⑥氢氧化钠。其中属于胶体的是 (填序号、下同),属于非电解质的是 ,属于单质的是 ,属于电解质的是 。KHCO3的电离方程式是 。