已知X、Y和Z三种元素的原子序数之和等于42。X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子。X跟Y可形成化合物X2Y3,Z元素可以形成负一价离子。请回答下列问题:
(1)X元素原子基态时的电子排布式为 ,该元素的符号为 ;
(2)Y元素原子的价层电子的电子排布图为 ,该元素的名称是 ;
(3)比较X的氢化物与同族第二、三周期元素所形成的氢化物稳定性 。
(1)以下列出的是一些原子的2p能级和3d能级中电子排布的情况。试判断,违反了泡利原理的是 ,违反了洪特规则的是 。

(2)某元素的激发态(不稳定状态)原子的电子排布式为1s22s22p63s13p33d2,则该元素基态原子的电子排布式为 ;其最高价氧化物对应水化物的化学式是 。
(3)用符号“>”“<”或“=”表示下列各项关系。
①第一电离能:Na Mg, Mg Ca。
②电负性:O F, F Cl。
③能量高低:ns (n+1)s, ns np。
④主族序数 价电子数 元素最高正化合价。
A、B、C、D、E、F是原子序数依次增大的短周期主族元素,A的最外层电子数是次外层电子数2倍,B是短周期中金属性最强的元素,C是同周期中阳离子半径最小的元素,D元素的最高价氧化物对应水化物与B元素的最高价氧化物对应水化物反应的产物M是制备木材防火剂的原料,E的最外层电子数与内层电子数之比为3﹕5。请回答:
(1)D的元素符号为 。
(2)F在元素周期表中的位置 。
(3)用电子式表示由元素B和F组成的化合物的形成过程: 。
(4)B单质与氧气反应的产物与C的单质同时放入水中,产生两种无色气体,有关的化学方程式为 、 。
(5)工业上将干燥的F单质通入熔融的E单质中可制得化合物E2F2。该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,该反应的化学方程式为 。
五种短周期元素A、B、C、D、E,原子序数逐渐增大,A、B处于同一周期,C、D、E同处另一周期。C、B可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙。A原子的最外层电子数比次外层电子数多3个。E周期序数等于E原子最外层电子数。根据以上信息回答下列问题:
(1)A、B、C、D、E五种元素的原子半径由小到大的顺序是 (用元素符号填写)
(2)乙物质中存在的化学键类型是 。
(3)选用恰当的试剂除去D中少量的E,写出发生反应的化学方程式 。
(4)化合物乙的电子式 。
(5)将D、E的单质插入NAOH溶液中,构成原电池,其负极反应是 。
W、X、Y和Z都是周期表中前20号元素,已知:
①W的阳离子和Y的阴离子具有相同的核外电子排布,且能形成组成为WY的化合物;
②Y和Z属同族元素,它们能形成两种常见化合物;
③X和Z属同一周期元素,它们能形成两种气态化合物;
④W和X能形成组成为WX2的化合物;
⑤X和Y不在同一周期,它们能形成组成为XY2的化合物。
请回答:
(1)W元素是______;Z元素是________。
(2)化合物WY和WX2的化学式分别是____________和 ____________。
(3)Y和Z形成的两种常见化合物的分子式是________和________。
(4)写出X和Z形成的一种气态化合物跟WZ反应的化学方程式:___________
有X、Y、Z、W四种短周期元素,原子序数依次增大。X的阳离子就是一个质子。Z、W在周期表中处于相邻位置,它们的单质在通常状况下均为无色气体。Y原子的最外层电子数是次外层电子数的2倍。请回答:
(1)Y的原子结构示意图为 ,YW2的结构式为 。
(2)将X2、W2按下图所示通人某燃料电池中,其中,b电极的电极反应式为 。

若有16gW2参加反应,转移的电子是 NA。
(3)由X、Y、Z、W四种元素组成的无机酸酸式盐,与足量的NaOH溶液在加热条件下反应的离子方程式为 。
下表是元素周期表的一部分,针对a~k十一种元素回答下列问题(请用具体化学式回答,否则不给分):
| 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
| 2 |
a |
c |
d |
|
e |
f |
g |
| 3 |
b |
h |
i |
|
|
j |
k |
(1)这些元素中非金属性最强的单质是 ,最高价氧化物对应水化物酸性最强的是 ,最高价氧化物对应水化物碱性最强的是 。
(2)表中k的氢化物的化学式为 ,它的还原性比j的氢化物还原性 (填“强”或“弱”),它水溶液的酸性比j的氢化物水溶液的酸性 (填“强”或“弱”)。
(3)e单质为 ,其结构式为 。
(4)用电子式表示h与k构成化合物的形成过程
(5)写出i的氧化物与强碱溶液反应的离子方程式
(6)H2和e的单质化合的反应是可逆反应,且该反应正方向放热。将等物质的量的H2、e的单质充入一恒容密闭容器中,在适当条件下反应。下列说法正确的是 (填写选项)。
A.升高温度,不论正反应方向还是逆反应方向速率都加快
B.向上述容器中充入适量Ar气可加快反应速率
C.反应过程中,e的单质的体积分数始终为50%
D.反应器内压强不随时间变化而变化,说明反应到达平衡
结构决定物质的性质、变化,请结合下图回答问题。
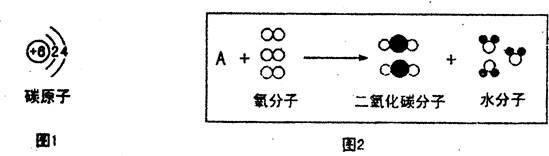
(1)由图1可知,在常温下,碳的化学性质不活泼的微观原因是 ;
(2)图2中A的化学式可能是 ,写出与图2反应微观本质不同的一个化学方程式 。
(5分)麻醉剂的发现和使用,是人类医疗史上了不起的一项成就,它可使患者在接受治疗中感觉不到疼痛。
(1)一种常用的麻醉剂氯仿(CHCl3),常因保存不善被氧化而变质,产生剧毒物光气(COCl2)。
2CHCl3+O2 2HCl+2COCl2.为防止发生事故,使用前可用于检验是否变质的试剂是(填序号)________。
2HCl+2COCl2.为防止发生事故,使用前可用于检验是否变质的试剂是(填序号)________。
| A.淀粉碘化钾溶液 | B.NaOH溶液 |
| C.酚酞溶液 | D.硝酸酸化的硝酸银溶液 |
(2)稀有气体氙气(Xe)在医疗上很受重视,常常作为麻醉剂,氙气能溶于细胞的油脂里,引起细胞麻醉和膨胀,从而神经末梢作用暂时停止。人们曾试用体积分数为80%氙气和20%的氧气组成的混合气体,作为无副作用的麻醉剂。氙在元素周期表中位于_______周期,______族,它的原子序数是______。
(3)作为稀有气体,氙的化学性质不活泼,但它可在一定条件下生成化合物。取1molXe和3.5mol氟气于一密闭容器内充分反应,后来余下了1.5mol的氟气同时有白色固体生成,此白色固体的化学式为_________。
五种短周期元素A、B、C、D、E,原子序数逐渐增大,A、B处于同一周期,C、D、E同处另一周期。C、B可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙。A原子的最外层电子数比次外层电子层多3个。D周期序数等于D原子最外层电子数。E原子半径是同周期中最小的(除稀有气体外)根据以上信息回答下列问题:
(1)A、B、C、D、E五种元素的原子半径由小到大的顺序是 (用元素符号填写),其中D的最高价氧化物是 氧化物。
(2)乙物质中存在的化学键类型是 。
(3)化合物乙的电子式 。
(4)写出C与D的最高价氧化物对应的水化物反应的离子方程式 。
(5)E的单质通入C的最高价氧化物对应的水化物的溶液中反应生成的“84”消毒液的主要成分的化学式为 。
W、X、Y、Z是原子序数依次增大的同一短周期元素,W、X是金属元素,Y、Z是非金属元素。
(1)W、X的最高价氧化物对应的水化物可以反应生成某复杂化合物,该离子方程式为___________。
(2)W与Y可形成化合物W2Y,该化合物的电子式为_______________。
(3)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为___________。
(4)比较Y、Z气态氢化物的稳定性:__________(用化学式表示)。
(5)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是_______________。
下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。
| A |
|
|
|
|
|||
| |
|
|
|
B |
C |
|
|
| D |
E |
|
|
|
|
F |
|
回答下列问题(对应物质书写相应化学式):
(1)元素B的元素符号为 ,它在元素周期表中的位置是 。
(2)D的简单离子的结构示意图为 ,它的最高价氧化物对应水化物中含有的化学键有 ,工业上冶炼D单质的化学方程式为 。
(3)用电子式表示EF2的形成过程 。
(4)由A2、C2构成碱性燃料电池,则该电池的负极反应方程式为 ,该电池工作过程中每通过2mol电子所需要的C2体积为 (标准状况)。
①~⑩十种元素,在元素周期表中的位置如图所示。回答下列问题:

(1)在上述十种元素中,置换酸中氢的能力最强的元素为 (填化学符号,下同);最高价氧化物的水化物的酸性最强的化合物的化学式是 ,碱性最强的化合物的化学式是 ,显两性的氢氧化物的化学式是 ;原子半径最大的元素是 ,半径最小的离子是 。
(2)上述十种元素中,金属性最强的元素在周期表中的位置是第 周期 族,该元素的单质在空气中燃烧的化学方程式为 。
(3)试用电子式表示元素①和③形成分子的过程 。
短周期的三种元素X、Y、Z,原子序数依次变小,原子核外电子层数之和是5。X元素原子最外电子层上的电子数是Y和Z两元素原子最外电子层上的电子数的总和;Y元素原子的最外电子层上的电子数是它的电子层数的2倍,X和Z可以形成XZ3的化合物。请回答:
(1)X元素是________;Y元素是________;Z元素是:________。
(2)XZ3化合物的分子式是_________,电子式是_________。
(3)分别写出X、Y的含氧酸的分子式_________、_________。
下表是元素周期表的一部分, 针对表中的①~⑧种元素,填写下列空白:
| 族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA[ |
零 |
| 2 |
|
|
|
① |
② |
③ |
|
|
| 3 |
④[ |
|
⑤ |
⑥ |
|
|
⑦ |
⑧ |
(1)上述元素中,化学性质最不活泼的是 (填元素符号)。
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是 (填元素符号)。
(3)元素②的气态氢化物分子属于 (填电解质或非电解质);元素⑦与④形成化合物的电子式是 。
(4)元素⑤的最高价氧化物与氢氧化钠溶液反应的离子方程式为: 。
(5)元素④的某氧化物可作供氧剂,该氧化物中所含的化学键类型有 ,写出其与二氧化碳反应的化学方程式 。