某同学用如图装置验证质量守恒定律。称取一定质量的碳酸钠装入气球,将气球套在锥形瓶上。将药品全部倒入装有足量稀盐酸的锥形瓶中,气球迅速胀大。称量反应前后装置的总质量,实验数据如下表所示。
| 实验次数 |
1 |
2 |
3 |
| 碳酸钠质量/克 |
0.53 |
1.06 |
2.12 |
| 反应前装置总质量/克 |
66.33 |
66.86 |
67.92 |
| 反应后装置总质量/克 |
66.19 |
66.62 |
67.42 |
(1)计算第1次反应产生的二氧化碳质量。
(2)分析数据发现每次反应前后装置的总质量均不相等,请以第1次反应为例,通过计算说明该反应是否遵循质量守恒定律。(空气密度取1.3克/升,二氧化碳密度取2.0克/升,结果精确到0.01)

2018年2月《自然》杂志上发表了一项新研究,展示了一种全新的加工木材的方法(如图),把天然木材放在NaOH和Na 2SO 3的混合液中煮沸以除去部分木质素,接着在100℃以上的高温中进行机械压缩制成致密木材。
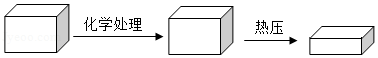
(1)致密木材是由天然木材加工而成的,其密度为天然木材的3倍。
①加工致密木材的材料主要取自于植物的 (填植物器官名称)。
②充分压缩后木材的厚度减小到原天然木材的20%,这一过程主要是 变化。若在压缩过程中底面保持不变,则说明处理过程中木材的质量减少了 (用百分数表示)。
(2)致密木材的硬度、拉伸强度都很大,为天然木材的10倍左右,甚至超过了部分金属。
①致密木材的拉伸强度和纤维素有关。纤维素的化学式为(C 12H 10O 5)n,则其中三种元素的质量比是C:H:O= 。
②拉伸强度  ,它用来表示材料的坚韧程度。拉伸强度与我们所学的科学量 的单位是相同的。
,它用来表示材料的坚韧程度。拉伸强度与我们所学的科学量 的单位是相同的。
(3)与其他材料相比,致密木材的优点是 。
A.加工过程中没有任何污染
B.可代替部分金属材料,具有广阔的应用前景
C.原料来源丰富,能通过无限制砍伐树木加工制成
科学家尝试通过多种途径减少CO 2的排放,或将CO 2转化为有用的物质。其中一种途径是利用NaOH溶液来"捕捉"CO 2,并将CO 2储存或利用,反应流程如图所示。

(1)反应分离室中分离物质的操作是 。
(2)上述反应流程中,可循环利用的物质是 。
(3)若反应分离室中有溶质质量分数为10.6%的Na 2CO 3溶液100千克,求完全反应后,理论上可生成CaCO 3的质量(要求根据化学方程式计算)。
为测定CuCl 2和FeCl 2组成的混合溶液中FeCl 2的质量分数,进行如下实验:
①取200g混合溶液加入足量的AgNO 3溶液,经过滤、洗涤、干燥、称量,得到143.5g AgCl固体;
②另取原混合溶液各200g与含有杂质的废铁屑反应(杂质不溶于水,也不参与反应),共做了五组实验,其实验数据如下表。
| 实验组别 |
一 |
二 |
三 |
四 |
五 |
| 混合溶液质量/g |
200 |
200 |
200 |
200 |
200 |
| 铁屑质量/g |
6 |
9 |
12 |
15 |
18 |
| 析出铜的质量/g |
6.4 |
9.6 |
m |
16 |
16 |
请分析计算:
(1)表中第三组实验的m值为 。
(2)第 组实验恰好完全反应。
(3)铁屑中铁的质量分数为多少?(计算结果精确到0.1%)
(4)原混合溶液中FeCl 2的质量分数为多少?(计算结果精确到0.1%)
某拓展性学习小组在学校科学实验创新比赛中,做了一个有趣的实验,装置如图。
实验设计:三颈烧瓶中充满二氧化碳气体,A颈、B颈分别连接充满氢氧化钠溶液和盐酸的注射器,C颈插有两端开口的玻璃导管(伸入瓶内的一端连有小气球),装置气密性良好。
实验操作:先通过A颈往瓶内注入氢氧化钠溶液,观察到小气球的形状发生了变化;过一段时间后再通过B颈往瓶中注入盐酸,发现小气球的形状又发生了改变。
请描述小气球形状的变化情况,并对此作出合理的解释。

2018年2月《自然》杂志上发表了一项新研究,展示了一种全新的加工木材的方法(如图),把天然木材放在NaOH和Na 2SO 3的混合液中煮沸以除去部分木质素,接着在100℃以上的高温中进行机械压缩制成致密木材。
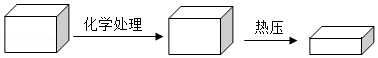
(1)致密木材是由天然木材加工而成的,其密度为天然木材的3倍。
①加工致密木材的材料主要取自于植物的 (填植物器官名称)。
②充分压缩后木材的厚度减小到原天然木材的20%,这一过程主要是 变化。若在压缩过程中底面保持不变,则说明处理过程中木材的质量减少了 (用百分数表示)。
(2)致密木材的硬度、拉伸强度都很大,为天然木材的10倍左右,甚至超过了部分金属。
①致密木材的拉伸强度和纤维素有关。纤维素的化学式为(C 12H 10O 5)n,则其中三种元素的质量比是C:H:O= 。
②拉伸强度= ,它用来表示材料的坚韧程度。拉伸强度与我们所学的科学量 的单位是相同的。
(3)与其他材料相比,致密木材的优点是 。
A.加工过程中没有任何污染
B.可代替部分金属材料,具有广阔的应用前景
C.原料来源丰富,能通过无限制砍伐树木加工制成
有一种管道疏通剂,主要成分为铝粉和氢氧化钠混合粉末。工作原理是:利用铝和氢氧化钠遇水反应放出大量的热,加快氢氧化钠对毛发等淤积物的腐蚀,同时产生氢气增加管道内的气压,利于疏通。小柯利用如图装置测定疏通剂中铝的质量分数。
Ⅰ.取样品20g,倒入容积为200mL的锥形瓶中,然后在分液漏斗中加入水,置于电子天平上测出总质量m 1。
Ⅱ.打开活塞,加入足量的水充分反应,直到没有固体剩余,静置一段时间,测出总质量m 2。
Ⅲ.实验数据如下表:
| 反应前总质量m 1 |
反应后总质量m 2 |
| 371.84g |
371.24g |
回答下列问题:
(1)配平化学方程式:2Al+2NaOH+2H 2O  NaAlO 2+3H 2↑
NaAlO 2+3H 2↑
(2)根据化学方程式计算样品中铝的质量分数。
(3)以下情形会导致样品中铝的质量分数测量结果偏高的原因可能有 。
A.向锥形瓶中倒入样品时,撒出了部分粉末
B.在反应过程中有水蒸气逸出
C.没有等装置中氢气全部排尽就称量

实验室有一瓶碳酸钙和氯化钙粉末组成的均匀混合物,小科用相同溶质质量分数的稀盐酸和该混合物反应(所得溶液均为不饱和溶液),四组实验数据记录如表,请分析计算:
实验组别 |
一 |
二 |
三 |
四 |
稀盐酸质量/g |
100.0 |
100.0 |
100.0 |
100.0 |
混合物质量/g |
3.0 |
6.0 |
9.0 |
12.0 |
所得溶液质量/g |
101.9 |
103.8 |
105.0 |
a |
剩余固体质量/g |
0 |
0 |
m |
n |
(1)反应后,稀盐酸还有剩余的是第 组;
(2)求混合物中碳酸钙和氯化钙质量之比;
(3)表中a的值为 ;
(4)求表中m的值。
BaCl2是一种重金属盐,其水溶液具有很强的毒性,若误服了BaCl2溶液,可立即服用MgSO4溶液解毒,为测定某BaCl2溶液的溶质质量分数,现取100克BaCl2溶液,不断加入MgSO4溶液,反应过程中溶液总质量与加入MgSO4溶液的质量关系如图所示,请回答:
(1)P点时溶液的溶质名称是 ;
(2)反应生成沉淀的最大质量为 克;
(3)求原BaCl2溶液的溶质质量分数。

碱式碳酸镁[Mg2(OH)2CO3]和过氧化镁(MgO2)都是重要化工原料。
Ⅰ.以Mg2(OH)2CO3为原料,制备产品MgO2的步骤如下:
(1)煅烧:煅烧Mg2(OH)2CO3得到三种氧化物,其中一种常温下是气体,且能使澄清石灰水变浑浊,煅烧时反应的化学方程式为 。
(2)转化:向所得固体中加双氧水充分搅拌,发生反应MgO+H2O2=MgO2+H2O,温度升高,说明该反应 热量(填“放出”或“吸收”)。其他条件相同,煅烧温度、煅烧时间不同,所得MgO对MgO2产率(产率= ×100%)的影响分别如图1所示,则最佳的煅烧温度为 ℃、煅烧时间为 小时。
×100%)的影响分别如图1所示,则最佳的煅烧温度为 ℃、煅烧时间为 小时。

(3)分离:得到产品。
(4)测定:假设产品中仅少量MgO,某小组设计图2装置,通过测定生成O2体积,计算MgO2的质量分数。
已知:a.MnO2与稀盐酸不反应 b.MgO2+2HCl=MgCl2+H2O2
c.2MgO2 2MgO+O2↑ d.MgO+C
2MgO+O2↑ d.MgO+C Mg+CO↑
Mg+CO↑
①仪器M的名称是 ,MnO2的作用是 。
②相同条件下, 能使测定结果更准确。(填图2中“装置A”或“装置B”)
③实验室用溶质质量分数为37%、密度是1.18g•mL-1的浓盐酸配制10%的稀盐酸110g,需要水 mL.(水的密度是1g•mL﹣1,计算结果保留一位小数)
④经讨论,该小组又设计了下列3种方案,分别取5.0g产品进行实验,能确定MgO2质量分数的是 。(填序号)
a.加热,使MgO2完全分解,测出剩余固体的质量
b.与足量炭粉在高温下充分反应,测出生成Mg的质量
c.先加足量稀盐酸,再加足量NaOH溶液,充分反应,测出Mg(OH)2质量
Ⅱ.MgCl2是制备Mg2(OH)2CO3的原料,现用含碳酸镁84%的菱镁矿制备MgCl2,反应如下:MgCO3+Cl2+CO MgCl2+2CO2(设杂质不参加反应)。生产19吨MgCl2需要这样的菱镁矿多少吨?(写出计算过程)
MgCl2+2CO2(设杂质不参加反应)。生产19吨MgCl2需要这样的菱镁矿多少吨?(写出计算过程)
二氧化锰因在工业生产中应用广泛而备受关注,制备二氧化锰是一项有意义的工作,某研究性小组对此展开了系列研究。
Ⅰ.用高锰酸钾制备
资料一:(1)3K2MnO4+2H2SO4═2KMnO4+MnO2↓+2K2SO4+H2O
(2)K2MnO4易溶于水
实验室加热高锰酸钾制氧气,反应的化学方程式为 。其反应类型是 。将反应后的固体剩余物用稀硫酸浸取一段时间后过滤、洗涤、烘干即得MnO2,用稀硫酸而不用水浸取的原因是 。
Ⅱ.用硫酸锰制备:电解MnSO4溶液可制得活性MnO2,同时生成氢气和硫酸,该反应的化学方程式为 ,一段时间后溶液的pH将 (填“变大”、“变小”或“不变”)
Ⅲ.用废锂电池制备
资料二:2Al+2NaOH+2H2O═2NaAlO2+3H2↑
用废锂电池正极材料(LiMn2O4、碳粉等涂覆在铝箔上)制备纳米MnO2,并进行锂资源回收,流程如下:

请回答下列问题:
(1)“滤液”中溶质的主要成分是 (填化学式)。
(2)在实验室进行“过滤”操作时,需要的玻璃仪器有烧杯、漏斗和 。
(3)MnO2与碳粉经下列三步反应制得纳米MnO2:
①2MnO2+C  2MnO+CO2↑
2MnO+CO2↑
②MnO+H2SO4═MnSO4+H2O
③3MnSO4+2KMnO4+2H2O═5MnO2↓+K2SO4+2H2SO4
上述涉及元素化合价变化的反应有 (填序号)。
IV.用碳酸锰制备
控制一定的温度,焙烧MnCO3制取MnO2的装置如下:

(1)实验中观察到澄清石灰水变浑浊,写出石英管中发生反应的化学方程式 。
(2)MnCO3在空气中加热易转化为锰的不同氧化物,其残留固体质量随温度的变化如图所示。图中B点对应固体成分的化学式为 (请写出计算过程)
实验室常会产生含硫酸的废水,需经处理至中性。某兴趣小组同学配制一定质量分数的氢氧化钾溶液来处理酸性废水。
(l)定性检测废水
检测废水呈酸性的方法是 。
(2)配制200g质量分数为5.6%的氢氧化钾溶液
①计算
m (KOH)= g,V(H 2O)= mL(水的密度近似为1.0g•mL ﹣ 1)。
②称取氢氧化钾
调节托盘天平平衡后,将一只烧杯放在托盘天平的左盘,称量其质量。然后 (按操作先后顺序,填字母),直至天平平衡。
A.向烧杯中加氢氧化钾固体 B.按需要添加砝码、移动游码 C.量取水 D.溶解 E.转移。
(3)定量测定废水
取酸性废水样品100g,逐滴加入5.6%的氢氧化钾溶液,废水中硫酸的质量分数变化如图所示。(假设废水中其他成分不与氢氧化钾反应且不含硫酸钾)
①P点对应溶液中一定存在的阳离子有 (填离子符号)。
②酸性废水中硫酸的质量分数为 (用百分数表示,保留到0.1%)。
③计算当废水处理至中性时,溶液中硫酸钾的质量分数(写出计算过程,结果用百分数表示,保留到0.l%)。

维生素C主要存在于蔬菜、水果中,其分子式为C 6H 8O 6,在空气中易氧化变质.
(1)维生素C中C、H、O三种元素的质量比为 (用最简比表示).
(2)为测定某鲜榨橙汁中维生素C的含量,兴趣小组进行如下实验:
步骤1 取橙汁样品,加入活性炭,振荡、静置、过滤,滤液移至小烧杯中,盖上玻
璃片.
步骤2 配制碘(I 2)溶液,测得其浓度为1.27g/L(即1升碘溶液中含有1.27克I 2).
步骤3 快速移取20.00mL处理后的橙汁样品置于锥形瓶中,滴入碘溶液,恰好完全反应时消耗碘溶液10.00mL.(测定原理:C 6H 8O 6+I 2═C 6H 6O 6+2HI)
①步骤1中活性炭的作用是 .
②步骤3必须在步骤1、步骤2之后立即进行的原因是 .
③计算1L该橙汁样品中含有维生素C的质量: g.(请写出计算过程)
"氧泡泡"系列产品去污能力强、绿色环保,已成为中国氧系清洁品类领导品牌,其主要成分是过碳酸钠(2Na 2CO 3•3H 2O 2)。某化学活动小组对过碳酸钠产生了浓厚的兴趣,决定对其进行探究。
【查阅资料】
Ⅰ.过碳酸钠在水中易离解成Na 2CO 3和H 2O 2,其水溶液具有Na 2CO 3和H 2O 2的双重性质;
Ⅱ.过碳酸钠与盐酸反应:2(2Na 2CO 3•3H 2O 2)+8HCl═8NaCl+4CO 2↑+3O 2↑+10H 2O;
Ⅲ.过碳酸钠的去污能力主要与其在反应中释放处的"活性氧"有关,"活性氧"含量越高,去污能力越强。
(1)20℃时,测得1%过碳酸钠水溶液的pH为10.5,说明其溶液呈 (选填"酸性"、"中性"或"碱性")。
(2)向过碳酸钠水溶液中加入少量MnO 2时产生大量气泡,发生反应的化学方程式是 。
(3)过碳酸钠样品中"活性氧"含量可按如下公式计算:
"活性氧"含量=  ×100%
×100%
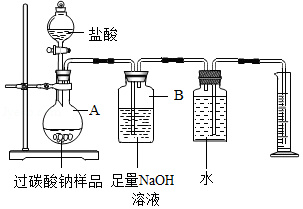
为测定某过碳酸钠样品中"活性氧"含量,取20g样品按如图实验装置与足量盐酸反应。(已知样品中杂质不溶于水且不与盐酸反应,装置气密性良好)
①将盐酸慢慢地入A中,反应一段时间,观察到 ,停止滴加盐酸。
②装置B可吸收生成的CO 2,该反应的化学方程式是 。
③甲同学认为若要得出生成氧气的质量,除要记录量筒内液体的读数外,还需要知道的数据是该实验条件下的 。
④将反应后A中所得溶液过滤、蒸发、结晶、烘干,称得固体质量为11.7g,乙同学据此计算出该过碳酸钠样品的"活性氧"含量,写出其计算过程。
⑤完成上述探究后,丙同学提出:称量反应前后装置B的质量,其质量差就是反应生成CO 2的质量,据此可计算出样品中"活性氧"含量。但丁同学认为该方案不合理,丁同学的理由是 (填写一条即可)
某学校兴趣小组在参与"五水共治"行动中,考察了某工厂的废水处理工程,并取该厂未经处理的废水样品进行测定分析:
(1)用紫色石蕊试液检验废水的酸碱性,石蕊试液呈 色,说明该废水显酸性.
(2)另取废水样品少量,滴加适量Ba(NO 3) 2,有白色沉淀产生,说明该废水中一定含有的酸根离子是 .
(3)同学们进一步了解到该废水中中含有一种酸,为测定其所含酸的质量分数,取该废水200克于烧杯中,逐渐加入硝酸钡溶液,生成的沉淀质量与加入硝酸钡溶液的质量关系如图所示,请计算废水中硫酸的质量分数.(假设该废水中的其他物质均溶于水且不与硝酸钡溶液反应).
