开春以来,为提高水稻产量,某农场积极做好科学施肥、精准防治病虫害等工作。
(1)水稻不同生长期需要不同的肥料。如在水稻抽穗、开花时期,为促进穗数增多、籽粒饱满,需要多施磷肥。下列属于磷肥的是 。
| A. |
碳酸钾( ) |
| B. |
尿素[ ] |
| C. |
磷酸二氢钙[ ] |
(2)氮肥能促进水稻幼苗生长。一百亩水稻需要施碳酸氢铵3950千克,用氨气、水和二氧化碳反应来制取,化学方程式为 ,需要氨气多少千克?
(3)井冈霉素是防治水稻纹枯病的常用药。要为一百亩水稻喷洒一次这种农药,需要配制溶质质量分数为0.01%的药液7500千克,应购买5%的井冈霉素药液 千克。
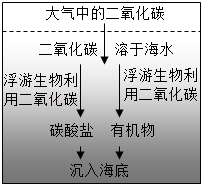
我国政府承诺在2060年前实现碳中和。为此,控制碳排放和增加碳吸收都至关重要。研究发现,除了陆地植物固碳外,海洋也是重要的固碳之地,如图是海洋吸收二氧化碳的三种方式。
碳酸盐泵:贝壳类、珊瑚等海洋生物将碳元素以碳酸钙的形式沉积起来。某地贝壳堤储存了约4亿吨贝壳,其中95%为碳酸钙,则该地贝壳堤固定了多少亿吨碳元素?
2022年我国将有6名航天员生活在空间站。氧气、水、食物等是维持航天员驻留空间站的必要物质。为提高物质的利用率,目前空间站通过以下途径实现物质循环利用:
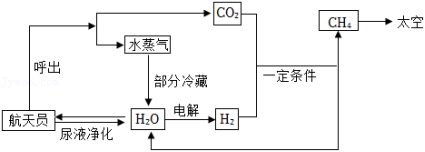
(1)由图可知,目前空间站通过物质循环获得水的途径共有 条,其中尿液净化时必须除去尿液中的 等代谢废物。
(2)为实现氧的循环,目前空间站内利用氢气和航天员呼出的二氧化碳,在一定条件下转化为甲烷和水,化学方程式为 。据测算,正常情况下一位航天员一天呼出的二氧化碳质量约1.1千克,若这些二氧化碳全部与氢气反应,则可生成水多少千克?
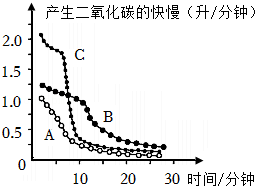
实验室制取二氧化碳时,选择合适溶质质量分数的盐酸,有利于减少盐酸浪费。小明分别取400克溶质质量分数为7.3%、14.6%、21.9%的盐酸与足量的石灰石反应,进行A、B、C三组实验,产生二氧化碳的快慢与时间关系如图所示,算得盐酸利用率如表(盐酸利用率是指收集到的气体体积理论上所需要的盐酸量与实际消耗的盐酸总量的比值)。
盐酸利用率与盐酸溶质质量分数的关系
|
组别 |
A |
B |
C |
|
盐酸溶质质量分数 |
7.3% |
14.6% |
21.9% |
|
盐酸利用率 |
82.5% |
81.5% |
72.1% |
(1)小明在实验过程中发现,发生装置中的锥形瓶外壁发烫。推测图中C组在第5~10分钟时反应快速变慢的主要原因是 。
(2)小明用400克盐酸进行A组实验,可收集到二氧化碳气体约多少升?(盐酸与石灰石反应的化学方程式为: ,常温常压下二氧化碳的密度约为2克/升)
(3)实验中,小明想在10分钟内制取10升二氧化碳气体,综合考虑各种因素,选用哪种溶质质量分数的盐酸更合适,并说明理由。 。
图甲是一款潜水艇紧急供氧设备的结构示意图,产氧药块主要成分是氯酸钠,需要镁粉氧化放热启动并维持反应进行,快速产生氧气。
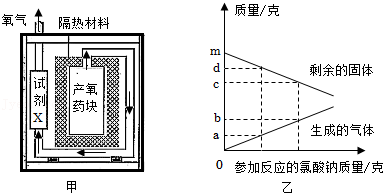
(1)启动时,镁粉( )与氧气反应生成氧化镁( )。其化学方程式为: 。
(2)产氧药块反应会产生极少量有毒的氯气,推测图甲中试剂 应具有的性质是 。
(3)氯酸钠受热分解生成氯化钠和氧气。 克氯酸钠分解过程中各物质质量变化如图乙所示,选择a、b、c、d、m中的部分数据,列出它们的等式关系以体现质量守恒定律。
“海洋强国”是国家战略,绍兴作为浙江海洋经济发展示范区的重要战略节点,正以积极的姿态规划发展海洋经济。利用海洋资源是海洋科技创新的新引擎。
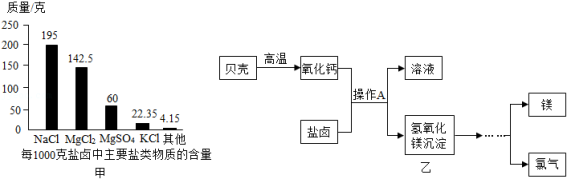
①盐化工是我国重要海洋产业。盐卤中主要盐类物质及其含量如图甲,利用盐卤生产金属镁的流程如图乙。由图甲可知,盐卤中含量最多的盐是 ;流程图中操作A的名称是 ;若生产过程中镁元素没有损失,且其他盐类中的镁元素质量可忽略不计,则1000克盐卤可制备金属镁 克。
②地球表面70%以上是海洋,各种海洋能源有待开发,你觉得开发前景广阔的能源有 。
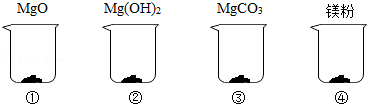
举重前运动员常常会抓一把“镁粉”在手里搓,以起到防滑效果,某种“镁粉”中只含有 、 、 中的一种或几种固体。某兴趣小组对其成分展开了探究:分别取4.2克 、 、 和“镁粉”置于烧杯中,逐滴加入相同溶质质量分数的稀盐酸直至粉末恰好消失。四种固体消耗稀盐酸的质量如表所示,且烧杯③和烧杯④中产生了大量气泡。请结合实验现象和数据回答问题。
|
物质 |
|
|
|
“镁粉” |
|
消耗稀盐酸的质量/克 |
121.8 |
|
58.0 |
61.9 |
(1)烧杯③中产生的气体是 。
(2)“镁粉”中不只含有 一种物质,理由是 。
(3)表格中 的值为多少?(请写出计算过程)
(4)为确定“镁粉”的具体成分,兴趣小组补充了如下实验:取“镁粉”和 各4.2克,加入足量稀盐酸,生成相同条件下的气体体积分别为952毫升和1120毫升。由此可知该种“镁粉”的成分是 。
某兴趣小组用硝酸钾进行了图甲所示的实验,硝酸钾溶解度与温度的关系如图乙。
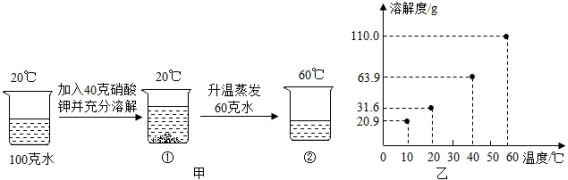
(1)①中未溶解的硝酸钾质量为 克。
(2)②中硝酸钾溶液为 (选填“饱和”或“不饱和”)溶液。
(3)计算②中溶液的溶质质量分数。
萤石是我市的优势矿产资源,也是我国“战略性矿物”。为探讨萤石的形成、开采、浮选等跨学科问题,兴趣小组对某萤石矿区开展项目化研究。
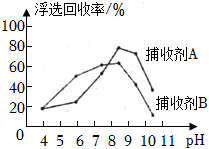
【萤石浮选】萤石矿开采后,将矿石破碎,研磨成矿粉,加水调成矿浆,往矿浆中添加捕收剂等药剂进行浮选,使目标矿粉粘附在泡沫上浮至水面,得到纯度较高的精矿。
(1)如图是pH值、捕收剂种类对浮选回收率影响的图像。为获得高浮选回收率,浮选时的最佳条件是 。
【纯度测定】萤石的主要成分为氟化钙( )。
已知:
(2)为测定精矿样品中氟化钙的含量,该小组称取10克样品和浓硫酸充分反应,生成的气体全部被碱性溶液吸收,测得碱性溶液增重4.4克,计算样品中氟化钙的质量分数。
【项目评估】萤石是我市优势矿产资源,但对萤石开采项目一直有不同观点。
(3)请选出你认同的一种观点 (填字母)。
A.我市应该立足资源优势,大力发展萤石开采项目
B.在勘探技术和环境监测到位的情况下,可以发展萤石开采项目
C.萤石开采项目会引发地表沉陷,诱发地质灾害,应禁止萤石开采项目
思维模型是依据事物发展内在规律所建立的解决问题的基本框架,能引导有序思维、增进深度理解、促进问题解决。小科建构了“混合物提纯”的思维模型:
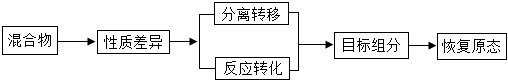
【初步理解】根据混合物组分的性质差异,获得混合物中目标组分。
(1)海水淡化是将海水中的盐与水分开,常压加热蒸馏法是其中的一种:常压下将海水加热形成水蒸气,再液化得到淡水的过程。从建模角度分析,海水加热形成水蒸气属于上述模型中的 (填“分离转移”或“反应转化”)。
【探究本质】根据组分的性质差异,选择合适方法,实现物质提纯。
(2)从含少量氯化钠的硝酸钾固体中提纯硝酸钾,是通过溶解、蒸发浓缩、冷却结晶、过滤、洗涤、干燥实现的。其中过滤操作将硝酸钾晶体与溶液分离是根据 不同。
【实践应用】根据混合物中某组分发生化学反应,提高混合物中目标组分纯度。
(3)小科取10克混有少量硫酸的盐酸溶液,滴入氯化钡溶液至不再产生沉淀,经过滤、洗涤和干燥得到沉淀0.233克,则原混合溶液中硫酸的溶质质量分数为 。
【融合创新】依据科学原理,融合技术与工程,形成新颖而有价值的解决实际问题方案。
(4)常压加热蒸馏法,能耗大、成本高。小科查阅资料获知,现在世界上的许多大型海水淡化工厂,都已经采用低压加热蒸馏法,请解释其蕴含的科学道理 。
某项目学习小组用传感器开展“影响铁锈蚀因素”的探究,设计如图1所示实验装置并完成实验。实验过程中,传感器采集数据绘制得到如图2的甲、乙两幅曲线图。
【资料1】一定条件下,碳和氯化钠溶液可加快铁的锈蚀,但它们本身不参加反应。
【资料2】该实验步骤如下:
①检查装置气密性;
②装药品,将5克铁粉和2克碳粉加入锥形瓶,并加入2毫升饱和氯化钠溶液;
③立即塞紧橡皮塞,橡皮塞上已插有一支装有5毫升稀盐酸的注射器及传感器;
④观察现象,采集数据。
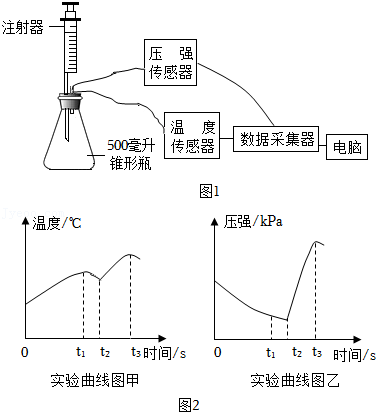
用所学知识及以上资料信息完成下列问题:
(1)实验进行一段时间后,注射器中的盐酸会自动注入瓶内,原因是 ;
(2)图2甲、乙曲线图中, 段温度升高,瓶内压强减小; 段温度升高,瓶内压强增大。解释产生这两个不同现象的原因。
为了保护生态环境,针对全球气候变化,中国政府向全球承诺,力争于2060年前实现“碳中和”。“碳中和”是指在一定时间内,使二氧化碳的排放总量与吸收总量平衡,实现“零排放”。实现“碳中和”通常可采取如下措施:
Ⅰ.碳减排:减少人类生产和生活中二氧化碳的排放量。
(1)下列做法不能实现“碳减排”的是 。
A.加高烟囱排放工业废气
B.推进新能源汽车使用
C.废弃物分类投放并回收利用
D.养成节约用水用电习惯
Ⅱ.碳吸收:①利用植物光合作用,这是自然界消耗二氧化碳的最重要途径;②利用“碳捕捉与封存技术”,即通过一定的方法,将工业生产中产生的 分离出来进行储存。在实际生产中,经常用 溶液来“捕捉” 流程如图所示(部分条件及物质未标出)。
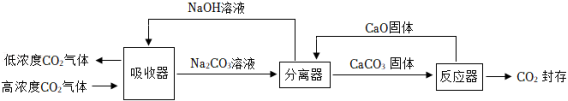
(2)用该技术进行“碳捕获”有效利用了原材料,该过程中被循环利用的物质有 。
(3)分离器中发生的反应:① ,② 。现有溶质质量分数为10.6%的 溶液100千克,求完全反应后,理论上可生成 的质量(要求根据化学方程式计算)。
Ⅲ.碳转化:指二氧化碳的资源化利用。
在化学实验中,经常需要对药品用量进行估算。既能确保实验成功,又能养成节约和环保的习惯。某化学兴趣小组为了体验估算方法,进行了如下实验:
【实验目的】对选定实验中所需药品用量进行估算并验证估算用量足够。

(1)【实验活动一】估算稀盐酸用量
①写出碳酸钙与稀盐酸反应的化学方程式: 。
②取2g石灰石样品进行实验(样品中除碳酸钙外,其余成分既不与盐酸反应,也不溶解于水),请估算,至少需要溶质质量分数为7.3%的稀盐酸 g。
(2)【实验活动二】验证估算的稀盐酸用量足够
方案一:
实验过程如图所示:

①将石灰石研细的目的是 。
②若图中试剂X为紫色石蕊试液,观察到的现象是 ,说明估算的稀盐酸用量足够。
③为达到与②相同的实验目的,试剂X还可以选择下列试剂中的 (填字母序号)。
| A. |
溶液 |
| B. |
溶液 |
| C. |
溶液 |
| D. |
|
方案二:
④只用以下两种规定用量的药品:2g石灰石样品和估算用量的稀盐酸,设计实验进行验证,请简述实验方案。(实验仪器任选)
|
实验操作 |
实验现象 |
实验结论 |
|
|
|
估算的稀盐酸用量足够 |
从宏观、微观、符号相结合的视角探究物质及其变化规律是化学独特的研究方法。根据所给信息,回答下列问题:
宏观辨识
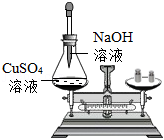
(1)通过科学探究可以认识化学反应中各物质质量之间的关系,如图实验中,将 溶液滴入锥形瓶中,反应结束后,再次称量,观家到托盘天平的指针 (填“向左”“向右”或“不”)偏转。
微观探析
(2)如图是氢气在空气中燃烧的微观示意图,该反应的基本反应类型为 反应。从微观角度分析,过程I表示分子分解成 的过程。

符号表征
(3)氢化镁( )是一种很有发展前景的贮氢材料,能与水反应生成氢氧化镁和一种常见的气体,反应的化学方程式为: 。请补全该反应的化学方程式并写出补全依据。
依据一:化学反应前后原子的种类和 不变。
依据二: 。
化学是一门以实验为基础的自然科学
(一)实验帮助我们研究物质的组成
如图是测定空气中氧气体积分数的实验装置,请回答下列问题:

(1)红磷在空气中燃烧的现象是 ,发生反应的化学方程式为: 。
(2)实验结论:氧气约占空气总体积的 。
(二)实验帮助我们研究物质的性质
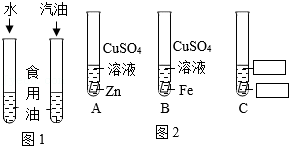
(3)图1实验中,食用油溶解于 中,该实验表明影响物质溶解性的因素是 。
(4)图2试管B中发生反应的化学方程式为: 。
(5)为了探究 、 、 的金属活动性顺序,图2试管C中需要补全的一组试剂是 。
(三)实验帮助我们研究物质的制法
实验室模拟炼铁原理的装置如图所示,请回答下列问题:
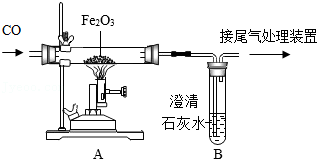
(6)写出A装置玻璃管中发生反应的化学方程式: ,该反应前后碳元素化合价发生的变化是 。
(7)B装置中的现象是 。
(8)实验中需要进行尾气处理的原因是 。