下列有关化学实验的“目的→操作→现象→结论”的描述都正确的是
| 选项 |
目的 |
操作 |
现象 |
结论 |
| A |
比较铝和铜的金属活动性 |
将砂纸打磨过的铝丝 浸入到硫酸铜溶液中 |
铝丝表面有红色固体析出 |
铝比铜活泼 |
| B |
检验露置在空气中的氢氧化钠溶液是否变质 |
取氢氧化钠溶液,滴入稀盐酸 |
开始时没有观察到气泡产生 |
氢氧化钠溶液没有变质 |
| C |
探究物质溶解于 水时的热量变化 |
向一定量水中加入硝酸铵晶体,充分搅拌 |
溶液温度下降 |
盐类物质溶解于水时,都会吸热 |
| D |
检验集气瓶中是否集满二氧化碳 |
将燃着的木条伸入集 气瓶中 |
木条火焰熄灭 |
集气瓶中已集满 二氧化碳 |
甲、乙、丙、丁分别是CO、O2、Fe2O3、CO2中的一种。已知在一定条件下,甲和乙可以反应,丙和乙也可以反应。下列说法中,正确的是
| A.甲一定是一氧化碳 |
| B.乙一定是氧气 |
| C.丙一定是氧化铁 |
| D.丁一定是二氧化碳 |
下列各组转化中,一定条件下均能一步实现的组合是
| A.①② | B.②③ | C.①③ | D.①②③ |
按下列装置进行实验,能达到对应目的的是



| A.比较溶解性 | B.检验铵盐 | C.制二氧化碳 | D.证明酸碱能反应 |
为除去下列物质中混有的少量的杂质,所用试剂正确的是
| |
物质 |
杂质 |
所用试剂、方法 |
| A. |
CaO |
CaCO3 |
高温煅烧 |
| B. |
N2 |
O2 |
通过灼热CuO |
| C. |
FeCl2 溶液 |
CuCl2 |
加入过量铁粉、过滤 |
| D. |
CO2 |
H2O |
通过NaOH固体 |
某化学兴趣小组对某品牌牙膏中摩擦剂成分及其含量进行探究,查阅资料如下:
1、该牙膏摩擦剂由碳酸钙、氢氧化铝组成;
2、牙膏中其它成分遇到盐酸无气体生成;
3、碱石灰的主要成分为生石灰和氢氧化钠固体。
利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定B中生成的BaCO3沉淀的质量,以确定碳酸钙的质量分数。请回答下列问题: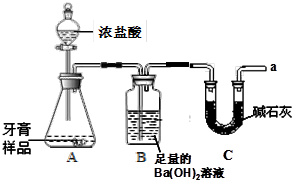
(1)B中反应生成BaCO3的化学方程式是 。
(2)C装置的作用是 。
(3)下列各项措施中,不能提高测定准确度的是 (填序号)。
| A.在加入盐酸之前,应排净装置内的CO2气体 |
| B.滴加盐酸不宜过快 |
| C.在A~B之间增添盛有浓硫酸的洗气装置 |
| D.在A~B之间增添盛有饱和碳酸氢钠溶液的洗气装置 |
(4)有同学认为该装置测定出来的碳酸钙质量分数会偏低,他的理由是
,解决方法是 。
(5)某同学认为不必测定B中生成的BaCO3质量,将B中的Ba(OH)2溶液换成浓H2SO4 ,通过测定C装置反应前后的质量差也可以测定CaCO3的质量分数。实验证明按此方法测定的结果明显偏高,原因是 。
(6)实验中准确称取8.00g样品三份,进行三次测定,测得BaCO3平均质量为3.94g 。请计算样品中碳酸钙的质量分数。(写出计算过程)
下列物质所用的分离和提纯方法不正确的是
A除氢氧化钠溶液中的硫酸钠,加入适量氢氧化钡溶液后过滤;
B利用过滤方法分离硝酸钾与氯化钠;
C通过灼热的氧化铜方法除去二氧化碳中混有的少量一氧化碳
D除去一氧化碳中混有的少量二氧化碳通入氢氧化钠溶液;
如图所示为实验室中常见的气体制备、净化、收集和性质实验的部分仪器。试根据题目要求,回答下列问题:
(1)以石灰石和稀盐酸为原料制取并收集干燥、纯净的二氧化碳气体,(提示:盐酸中会挥发出的少量HCl气体可用饱和碳酸氢钠溶液吸收)
①所选仪器的连接顺序为 (填写仪器序号字母)。
②生成二氧化碳时,所发生反应的化学方程式为 。
(2)收集CO2时,他们如何检验已CO2收集满?
(3)实验室制取气体要选择适当反应物.我们知道实验室制取大量CO2气体不能用浓盐酸,因为 。
(4)他们对实验室制取CO2的实验条件展开了进一步的探究,做了如下四个对比实验:
①取m g块状大理石与足量的溶质质量分数为5%的盐酸反应;
②取m g块状大理石与足量的溶质质量分数为10%的盐酸反应.
实验现象:产生气泡的快慢顺序为②>①;
实验结论:影响大理石和盐酸反应快慢的因素有 ;
你认为影响大理石和盐酸反应快慢的因素还有 。
下列反应制取气体,可用如图装置制取、干燥和收集的是
A Zn+H2SO4=ZnSO4+H2↑
B 2H2O2 2H2O+O2↑
2H2O+O2↑
C CaCO3+2HCl=CaCl2+H2O+CO2↑
D 2NH4Cl+Ca(OH)2 CaCl2+2NH3↑+2H2O
CaCl2+2NH3↑+2H2O
在学习过程中,小雨同学提出一个问题:“碳燃烧时可能生成CO2,也可能生成C0,那么碳与氧化铜反应生成的气体也有多种可能?”
[猜想]碳与氧化铜反应生成的气体中:①只有CO2 ②只有CO③既CO2,又有CO。
[查阅资料]浸有磷钼酸溶液的氯化钯试纸遇CO2无变化,但遇到微量CO会立即变成蓝色。
[方案设计]通过上述资料和已有知识,小雨初步设想用浸有磷钼酸溶液的氯化钯试纸和澄清的石灰水对碳与氧化铜反应生成的气体进行检验。根据小雨的设想,请你完成填空:
(1)若试纸不变色,石灰水变浑浊,则只有C02;
(2)若试纸 ,石灰水 ,则只有C0;
(3)若试纸 ,石灰水 ,则既有CO2,又有CO。
[实验验证]经过思考之后,小雨设计了如图所示实验装置: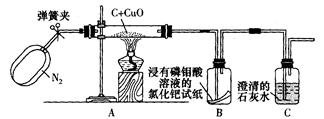
实验步骤:
(1)打开弹簧夹,先通一会儿纯净、干燥的N2;
(2)关闭弹簧夹,点燃酒精灯,加热。
结论:小雨通过分析实验现象,确认猜想③是正确的,请你写出装置C中发生反应的化学方程式: ;
[反思与评价]
(1)该实验开始通一会儿N2的目的是 ;
(2)请从环保的角度分析该实验装置的不完善之处 。
用下图所示的仪器组装一套实验装置,并完成—下列实验任务:①用干燥的CO气体还原CuO②检验CO还原CuO的气体生成物(浓硫酸具有吸水性,能干燥CO气体),请回答下列问题:
(1)实验进行时,若要气体从左向右流动,则这套装置的连接顺序应是(填仪器接口字母):
( )接( ),( )接( ),( )接( );
(2)实验开始时,先通入CO气体,后加热氧化铜的理由是 ;
(3)A中澄清石灰水的作用是 ;
(4)该套实验装置从环境保护的角度考虑可能存在的不足是 ,
你提出的合理处理建议是 。
探究小组用如图装置进行实验.胶头滴管和集气瓶中分别盛装某种试剂,挤压胶头滴管向集气瓶中滴加适量液体后,能观察到气球变大的组合是
| A.胶头滴管中的试剂:稀硫酸;集气瓶中的试剂:Na2CO3 |
| B.胶头滴管中的试剂:稀盐酸;集气瓶中的试剂:Zn |
| C.胶头滴管中的试剂:NaOH溶液;集气瓶中的试剂:CO2 |
| D.胶头滴管中的试剂:浓硫酸;集气瓶中的试剂:水 |
实验室可以用草酸(H2C2O4)在浓硫酸的作用下来制取一氧化碳,反应原理为:
H2C2O4 CO↑+ CO2↑+ H2O
CO↑+ CO2↑+ H2O
小明同学设计下图所示装置来制取一氧化碳,并验证一氧化碳的性质。 
请回答下列问题:
(1)长颈漏斗a的漏斗颈没入液面下的目的是 。
(2)B中氢氧化钠溶液的作用是 。
(3)C中澄清石灰水的作用是 。
(4)通过什么现象可以判断CO能与CuO反应? 。
(5)D中反应的化学方程式是 。
化学家创造出一种物质“干水”, 其每个颗粒含水95﹪,外层是SiO2 ,干水吸收二氧化碳的能力比普通清水高三倍。下列有关说法正确的是
| A.干水和干冰是同一种物质 |
| B.干水中的水分子不再运动 |
| C.用干水吸收CO2有助于减缓温室效应 |
| D.干水吸收CO2的过程会发生化学变化 |
多彩的“碳”,多姿的生活,让我们一起走进“碳”的世界.
(1)下列含碳元素的物质中,属于有机物的是 (填字母序号)。
A.碳酸钙 B.乙醇(C2H5OH) C.二氧化碳
(2)化石燃料主要包括煤、 和天然气,他们都含有碳元素,其中天然气的主要成分是 (写化学式)。含碳物质的燃烧会导致过多的二氧化碳排放,加剧了“温室效应”,写出一条减少二氧化碳排放的建议 。
(3)2013年3月,浙江大学实验室里诞生了世界上最轻的材料——“碳海绵”。(如图所示),由碳元素组成,具有多孔结构,弹性好。它对石油有很强的吸附能力(不吸水),将吸入的石油挤出后仍可恢复原状。下列关于碳海绵的说法正确的是 (填字母序号)。
A.具有吸附性 B.可重复利用 C.可处理海上石油泄漏
(4)液态二氧化碳灭火器可用于扑救档案资料室发生的火灾,下列说法正确的有 (填标号)。
A.液态二氧化碳气化后不会污染档案资料
B.二氧化碳可覆盖在燃烧物表面,隔绝空气
C.液态二氧化碳气化时吸热,降低了可燃物的着火点
(5)二氧化碳是很重要的化工原料,科学家设想利用太阳能加热器“捕捉CO2”、“释放CO2”,实现碳循环。
①步骤1的化学方程式为 。
②为确定步骤2中的碳酸钙是否完全分解,设计的实验步骤为:取少量固体于试管中,滴加过量 溶液,若观察到试管内 。则分解不完全。
③上述设想的优点有 (填字母序号)。
a.原料易得且可循环利用 b.充分利用太阳能 c.可全地域全天候使用
④CO2是宝贵的碳氧资源。CO2和H2在一定条件下可合成甲酸(HCOOH),此反应中CO2与H2的分子个数比为 ,若要检验1%甲酸水溶液是否显酸性,能选用的有 (填字母序号)。
a.无色酚酞溶液 b.紫色石蕊溶液 c.pH试纸
(6)小刚同学对碳及其重要化合物知识进行归纳、整理,并建构了如图所示的转化关系图。请回答下列问题:
(1)写出括号内一种含有碳元素物质的化学式 ;
(2)转化关系图中由H2CO3→CO2的反应类型是 反应;
(3)CO2常用于灭火,但镁着火不能用 CO2灭火,原因是它们能发生反应生成另一种氧化物和单质,请写出该置换反应的化学方程式 。