图示四种途径都可以得到氧气:

(1)写出实验室中通过甲、乙两种途径制取氧气的化学方程式:
甲_______________________________;
乙_______________________________。
(2)“绿色化学”是21世纪化学科学发展的重要方向之一。你认为在中学化学实验室中,甲、乙、丙三种制取氧气的途径中, (填“甲”“乙”或“丙”)途径更体现化学实验的绿色化追求。
(3)某同学用如图所示的装置粗略地测定空气中氧气的体积分数,图中烧杯上方玻璃管(预先固定好)中部有一可左右滑动的活塞,活塞左端内密封有空气,活塞右端的玻璃管口跟空气连通,实验开始前活塞处在刻度5cm处。(已知:白磷着火点为40℃左右)

①向烧杯内放入适量的水与生石灰反应,目的是 ;
②可观察到玻璃管内发生反应的现象是:
白磷(足量) ;
活塞向 (选填“左”或“右”)移动;
③实验结束到常温后,活塞应停在约 cm处,据此可得出的结论是 。
水是一种重要的资源,人类的日常生活和工农业生产离不开水。请回答:
(1)图1是实验室电解水的示意图。实验中生成氧气的试管是 (填“1”或“2”),该反应的化学方程式为: 。

图1 图2
(2)图2表示自来水生产的一般过程。下列说法正确的是
| A.加入絮凝剂使水中悬浮物凝聚 | B.通过沙滤池除去水中可溶性杂质 |
| C.通过活性炭吸附有色物质和有臭味物质 | D.通入氯气杀菌消毒 |
(3)我国南海海岛众多,但淡水资源匮乏。为了解决这一问题,人们设计了太阳能海水淡化装置,原理如图3所示。
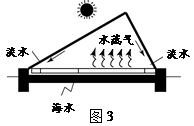
① 在相同时间内,海岛上晴好天气比阴雨天气制得淡水更多,其微观解释是 。
② 若某海水中氯化钠的质量分数为2.5%,利用该装置将1000kg的海水暴晒一段时间后,测定发现,剩余海水中氯化钠的质量分数是原来海水的十倍,则可得到的淡水为 kg;已知该温度下氯化钠的溶解度为36g,则剩余海水是 (填写“饱和溶液”、“不饱和溶液”或“不确定”)。
甲、乙、丙、丁均为常见物质,由氢、碳、氧、氯、铁、钙6种元素中的1-3种组成。在一定条件下,四种物质存在如下转化关系:甲 + 乙 → 丙 + 丁。
(1)若甲的固体俗称干冰,其化学式是 。写出符合上述转化关系的一个化学方程式 。
(2)若甲、丙均为单质,反应后溶液为浅绿色。则符合上述转化关系的反应物是 。
(3)如图所示。关闭止水夹,将装置A注射器中的液体推入瓶中,与集气瓶中收集的气体发生上述(1)的反应,待恰好反应完全后,将装置B分液漏斗中过量的液体放入瓶中(使液面没过导管下端),与瓶中适量固体接触,发生上述(2)的反应,立即关闭开关,打开止水夹,可以看到的现象有:B中的液体进入A中、 ,分析B中液体进入A中的原因是 。

如图所示,将细铁丝分别放在充满氮气、氧气的集气瓶中进行实验。

| 实验 |
Ⅰ |
Ⅱ |
| 集气瓶中的气体 |
氮气 |
氧气 |
| 接通电源加热后观察到的现象 |
铁丝红热,不燃烧 |
剧烈燃烧,火星四射 |
(1)实验Ⅱ中,反应后有 色固体生成,集气瓶中水的作用是 。
(2)接通电源后,对比Ⅰ、Ⅱ实验现象,可知可燃物燃烧的条件之一是 。
(3)在上述实验中,能证明可燃物燃烧需要温度达到着火点的依据是 。
水是重要的自然资源。
(1)节约用水是每个公民的责任和义务。下列做法属于节约用水的是_________(填编号)。
A.收集雨水用于浇灌花木 B.农业上用水漫灌农作物
C.工业上冷却水循环使用 D.用水后及时关闭水龙头
(2)可用于区分硬水和软水的物质是______________;降低水的硬度的方法是______________。
(3)自来水厂净化水的主要步骤如下图所示。有关说法错误的是______________(填编号)。

A.步骤①②可除去难溶性杂质 B.X试剂可以是活性炭
C.步骤④中可用明矾作消毒剂 D.净化后的水为纯净物
构建知识网络图是化学学习的一种重要方法。请完善网络图,并根据图示关系回答下列问题:
(1)完善上述知识网络图。图I中①_______________;
图Ⅱ中② ______________,③_______________。
(2)根据图I中所示关系填写下列空白:
④物质是由_____________组成的;
⑤构成物质的微粒有_________________;
⑥分子是由___________构成的;
⑦原子是由___________________构成的;
⑧原子得失电子转化为___________________。
(3)依据图Ⅱ完成下列问题:⑨纯净物和混合物属于________关系;(填“并列”或“包含”)
水是生命之源,政府为了解决我市人民用水难的问题,于2013年末举行了毗河供水二期工程开工动员誓师大会。
(1)河水中含有许多杂质,可利用吸附、沉淀、过滤和蒸馏等方法净化,其中净化程度最高的方法是 ;
(2)净水过程中常用漂白粉来杀菌消毒,漂白粉的有效成分是次氯酸钙,其化学式为Ca(ClO)2,次氯酸钙中氯元素的化合价为 ;
(3)硬水给生活和生产带来很多麻烦,生活中常用 来区分硬水和软水。
(4)“中水”是城市污水处理设施深度净化处理后的水,因为水质介于自来水(上水)与排入管道的污染水(下水)之间,故名为“中水”。下列关于中水的说法中不正确的是( )
| A.“中水”不能做为饮用水 |
| B.利用中水有利于节约水资源 |
| C.“中水”中水分子的构成与蒸馏水中的水分子构成不同 |
| D.将生活中的污水净化处理成“中水”的过程要用到过滤和吸附等方法。 |
(5)阿伏加德罗总结出下列定律:在同温同压下,同体积的任何气体都含有相同的分子数。右图是电解水的实验装置,如果D管产生的气体分子数为2×1023个,则C管产生的气体分子数为 个。

人类的日常生活和工农业生产离不开水.请回答:
水 人类所需的六大基本营养素之一.含有较多可溶性钙、镁化合物的水叫做 .
下列净化水的单一操作中,相对净化程度较高的是
A.静置沉淀 B.吸附沉淀 C.蒸馏
水在通电的条件下可以分解,写出该反应的化学方程式 .
高铁酸钾能作消毒剂与絮凝剂.它杀菌时会生成氢氧化铁胶状物.高铁酸钾中铁元素的化合价是 .
在点燃条件下,A和B反应生成C和D.反应前后分子种类变化的微观示意图如图所示.

请回答以下问题:
(1)1个A分子中含有 个原子.
(2)A中氮元素和氢元素的质量比为 .
(3)A、B、C、D四种物质中,属于化合物的是 (填图中字母).
(4)该反应的化学方程式为 .
草酸(C2H2O4)受热分解生成二氧化碳、一氧化碳和水。某同学为验证草酸分解产物,将产物持续通入下列装置。请回答:

①请写出草酸分解的化学反应方程式 。
②A装置中的实验现象是 ,C中发生反应的化学方程式 ,该反应的氧化剂是 。
③对该实验的分析正确的是 (选填编号)
Ⅰ.该实验中A、B装置不可以互换
Ⅱ.若C中停止加热,D中液体会倒吸入硬质玻璃管中
Ⅲ.反应结束后,C中的固体物质属于混合物
Ⅳ.若分解产物停止通入时,C中生成的铜不会被氧化。
回答下列问题.
(1)在H、H2、H+ 中表示氢离子的是__________.
(2)已知锂(Li)元素在化合物中的化合价为+1,写出氧化锂的化学式:____________.
(3)在反应4HNO3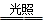 4NO2↑+2H 2 O+ X↑中,X的化学式为___________.
4NO2↑+2H 2 O+ X↑中,X的化学式为___________.
(4)清凉油的主要成分薄荷脑(C10 H10 O)是由___________种元素组成的,分子中的碳、氢、氧的原子个数比为____________.
2012年6月16日第三届亚沙会将在烟台海阳举行。它是亚洲最大的沙滩体育盛会。


(1)亚沙会采集圣火的采火棒顶部由纯棉纱构成,棉纱中添加了适量的煤油。棉纱不易点燃,而煤油容易点燃的原因是 。为保证采火棒的火焰达到所需的高度,添加煤油要适量,从而保持棉纱内有足够的孔隙,其目的是 。
(2)亚沙会火炬——“凤舞金沙”,使用丙烷(C3H8)气体为燃料,燃烧后对环境无污染。丙烷燃烧的化学方程式为__________ ______。
(3)亚沙会奖牌——“海阳之星”,采用了“金镶贝”的独特工艺。每枚奖牌由一只珍贵贝壳经多种工艺加工而成,使每枚奖牌都具备了独一无二的特性。贝壳能被盐酸、醋酸等酸性物质腐蚀,它的主要成分(CaCO3)与盐酸反应的化学方程式为___________________________________。
如图所示是初中化学的一些重要实验,请回答:

(1)实验A:通电后,乙中产生的是 ,区别硬水和软水的试剂是 ,现象是 。写出该实验反应的化学方程式 。
(2)实验B:测得空气中氧气体积分数小于五分之一的原因可能是 (只答一条)
(3)实验C:图中a的名称是 ,在操作中,它的作用是 ,浑浊的河水经过该装置过滤后得到的水是 (“纯净物”或“混合物”).
(4)实验D:集气瓶内放少量水的目的是 ,观察到_____ 现象,写出铁丝与氧气反应的化学方程式 。
(5)实验E:倾倒CO2时观察到的现象是___ _.
元素X、Y、Z、M是初中常见的四种元素,有关信息如下表:
| 元素 |
有关信息 |
| X |
可形成相对分子质量最小的气体单质 |
| Y |
形成的一种单质是天然存在的最硬的物质 |
| Z |
其单质约占空气总体积的1/5 |
| M |
人体内含量最高的金属元素 |
(1)M元素的名称是 Y形成的天然存在的最硬的物质是 。
(2)由X、Y两种元素组成的最简单的有机物是 (填化学式)由Y、Z两种元素组成的能用于人工降雨的固体物质是
(3)由Z、M 两种元素按原子个数比1:1组成的化合物俗称 ,写出它与水反应的化学方程式
如图是某同学设计的实验室制取二氧化碳并验证其性质的实验装置图。

请回答下列问题:
(1)将A、E装置连接时,应将A装置的导管a与E装置的导管 (填“b”或“c”)相连接。检验E装置中二氧化碳已收集满的方法是 。
(2)将A、B装置连接,观察到的现象是 ,可验证二氧化碳的性质是 。
(3)将A、C装置连接,可验证二氧化碳与氢氧化钙的反应,该反应的化学方程式为 。
(4)用E装置收集满一瓶二氧化碳气体,取下双孔橡胶塞,将瓶中的气体沿D装置烧杯右侧内壁缓慢倒入,观察到的现象是 ,这些现象说明二氧化碳具有的物理性质是 ,化学性质是 、 。