超氧化钾能与二氧化碳反应生成氧气(4KO2+2CO2===2K2CO3+3O2),在医院、矿井、潜水、高空飞行中用作供氧剂。要得到48 g氧气,参加反应的超氧化钾的质量是多少?
钛(Ti)是广泛应用于航空、航海等领域的一种重要金属。在一定条件下,钛由四氯化钛(TiCl4)和金属镁反应而制得:TiCl4+2Mg==Ti+2MgCl2 。现有380Kg四氯化钛,可生产金属钛多少千克?
某学生做了如下图所示的实验。
| |
第一次 |
第二次 |
| 加入氧化铜的质量 |
m |
m |
| 加入稀硫酸的质量 |
50g |
100g |
| 加入铁粉的质量 |
5.6g |
5.6g |
| 实验现象 |
黑色固体和紫红色固体 |
紫红色固体 |
若第二次所加物质恰好完全反应(滤液损失忽略不计),请回答下列问题:
(1)写出实验中发生反应的化学方程式
(2)第一次实验后的固体物质的化学式为
(3)根据已知条件列出求解第二次实验生成固体物质的质量(x)的比例式
(4)实验中加入氧化铜的质量(m)为 ;
(5)若向第二次反应后的滤液中加入92.8g水,则所得不饱和溶液中溶质的质量分数为 ;
(6)若用溶质质量分数为49%的硫酸溶液配制实验中所需的稀硫酸,则需要加水的质量
为 。
某同学为了测定一瓶过氧化氢溶液中溶质的质量分数,取该溶液20g,加入二氧化锰0.5g,完全反应后,称得烧杯内剩余物质的总质量为19.7g。请回答下列问题:
(1)二氧化锰在反应中的作用是__________________。
(2)计算该过氧化氢溶液中溶质的质量分数。
(3)利用上述溶液配制100g溶质质量分数为3%的过氧化氢消毒液,需该溶液的质量为__________g(结果保留一位小数)。
部分被氧化的铁片10g与200g的稀硫酸恰好完全反应,产生氢气0.3g,求该硫酸溶液的溶质质量分数?
造纸厂会产生含氢氧化钠的废水,需经处理呈中性后排放。为测定此废水中氢氧化钠的质量分数,工作人员取了40g废水样品加入到锥形瓶中,逐滴加入10%的稀硫酸,至恰好完全反应时,消耗稀硫酸49 g。计算废水中氢氧化钠的质量分数。
某课外活动小组加热炭粉(过量)和氧化铜的混合物,再用下图所示装置,对获得的铜粉(含炭)样品进行实验,测定铜的质量分数。图中铁架台等装置已略去。请回答下列问题: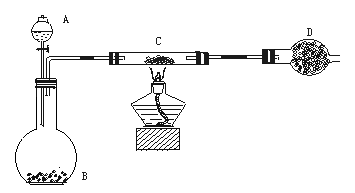
仪器:铁架台(含铁圈、铁夹)、分液漏斗、平底烧瓶、硬质玻璃管、干燥管、酒精灯、石棉网、洗气瓶等。
药品:红褐色(含炭)样品、过氧化氢溶液、二氧化锰、碱石灰(固体氢氧化钠和氧化钙的混合物,可用来吸收水和CO2)。
(1)除上述仪器外,实验中还必须用到的仪器是 ;
(2)实验操作前,首先进行 检查。在C中加入样品粉末W g,D中装入药品后并称量为m1 g,连接好仪器。打开A的上塞、活塞,慢慢滴加溶液。对C进行加热。当C中药品充分反应后,关闭A的活塞,停止加热。冷却后,称量D的质量为m2 g。 实验进行的过程中,装置C中发生的主要化学反应类型 ;充分反应后装置C中剩余的固体成分是 。
(3)问题和讨论:
实验完成后,老师评议说:按上述实验设计,即使C中反应完全,D中吸收完全,也不会得出正确的结果。经讨论,有同学提出在B与C之间加入一个装置,该装置作用是 。
(4)有学生提出直接用右图装置,在空气中直接加热进行实验。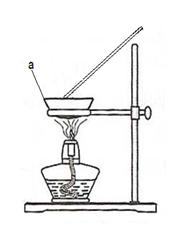
图中仪器“a”的名称为 。
若取20g铜粉(含炭)样品进行实验,充分反应后,仪器a中剩余的固体质量为24g,计算求原来混合物中铜的物质的量以及铜的质量分数。
(要求:根据化学方程式计算,并写出计算过程!)
为测定某生理盐水的溶质质量分数,现将生理盐水样品与足量的硝酸银溶液混合,相关实验数据如下表所示(不计损耗):
| |
反应前 |
反应后 |
|
| 实验 数据 |
生理盐水样品的质量 |
加入硝酸银溶液的质量 |
过滤后剩余溶液的质量 |
| 130 g |
40 g |
167.13 g |
(1)反应后生成氯化银固体的质量为 g。
(2)请计算该生理盐水中含氯化钠的物质的量(根据化学方程式列式计算) 。
(3) 。
某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁。他们为了测定水垢中碳酸钙的含量,将足量的盐酸加入到10g水垢中,产生CO2气体的情况如图所示。
(1)从图中可以看出,10g水垢反应后生成的二氧化碳最多是 g。
(2)水垢中的碳酸钙质量分数是多少?
为了测定未知浓度稀硫酸的溶质质量分数,取氢氧化钡溶液15g,逐滴加入该待测稀硫酸,同时测定并记录反应过程中混合溶液的pH变化情况(如图所示),过滤后得到滤液32.67g.
求:(1)反应后生成硫酸钡的质量是多少;
(2)该稀硫酸的溶质质量分数。
下面是工厂苛化法生产烧碱的示意图。
(1)在实验室,操作Ⅰ的名称是 ;经操作Ⅰ得到废渣的主要成份是 (写化学式)。
(2)物质X中各元素的质量比表示为 。
(3)某工厂化验员向含有1.6 g氢氧化钠的溶液中,逐滴加入20.0 g盐酸至氢氧化钠和盐酸恰好完全反应。求盐酸中溶质的质量分数为多少?(写出过程)
(4)若用1.6 g上述得到的固体烧碱产品(含杂质)代替1.6 g氢氧化钠,逐滴加入上述相同浓度盐酸至反应物恰好完全反应,则消耗盐酸的质量 20 g(填“大于”、“等于”或“小于”)。
某烧杯中加入12.5 g含杂质的石灰石,与100 g稀盐酸恰好完全反应(杂质不与盐酸反应也不溶于水),称得烧杯中物质的总质量减少了4.4 g.求:
(1)石灰石含碳酸钙的质量分数.
(2)反应后溶液中溶质的质量分数.
乙醇是一种清洁的绿色能源,可再生,俗称酒精,其化学式为C2H5OH,其在空气中完全燃烧的化学方程式为:C2H5OH+3O2 2CO2+3H2O,现有100g质量分数为92%的乙醇溶液在空气中完全燃烧产生二氧化碳的质量为多少克?
2CO2+3H2O,现有100g质量分数为92%的乙醇溶液在空气中完全燃烧产生二氧化碳的质量为多少克?
计算:
兴塘初中化学兴趣小组的同学在实验室用加热氯酸钾和二氧化锰固体混合物制取氧气时,反应前氯酸钾和二氧化锰混合物的质量为7克,加热到不再产生气体为止,剩余固体的质量为5.08克.则:
(1)反应能制得氧气质量为 克?
(2)原混合物中氯酸钾的质量分数为多少?
某化学实验小组要检测黄铜(铜、锌合金)中金属铜的纯度,同学们取20 g黄铜样品,向其中分三次共加入15 g盐酸溶液,充分反应后测得实验结果如下: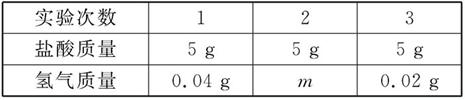
请计算:(1)第2次实验产生氢气的质量m= g。
(2)黄铜(铜、锌合金)中金属铜的纯度。
(3)该盐酸溶液中溶质的质量分数。