上海市松江区九年级下学期3月月考化学试卷
蚊子体内含有甲酸,人被叮咬后皮肤发痒,涂抹后能止痒的物质是
| A.食醋(pH≈2) | B.牛奶(pH≈6.5) | C.矿泉水(pH≈7) | D.肥皂水(pH≈10) |
向2ml氨水中滴加5〜6滴紫色石蕊试液,充分振荡后溶液颜色将变成
| A.红色 | B.紫色 | C.无色 | D.蓝色 |
一般不宜用作治疗胃酸过多的是
| A.NaOH | B.Mg(OH)2 | C.Al(OH)3 | D.墨鱼骨粉(含CaCO3) |
下面四种金属中,有一种金属能与其余三种金属的盐溶液反应,则该金属是
| A.Ag | B.Cu | C.Al | D.Zn |
已知金属锰(Mn)在金属活动性顺序中位于铝和锌之间,则不能发生置换反应的是
| A.Mn和CuSO4 溶液 | B.Mn和ZnSO4溶液 |
| C.Fe和MnSO4溶液 | D.Mn 和 稀H2SO4 |
把X、Y、Z三种金属片分别加入稀硫酸中,只有Z表面有气泡冒出,把Y投入X的硝酸盐溶液中,Y表面有X析出,则三种金属的活动性由强到弱的顺序是
| A.X>Y>Z | B.Y>X>Z | C.Z>Y>X | D.Z>X>Y |
用稀硫酸除铁锈的原理是
| A.FeO+H2SO4→FeSO4+H2O |
| B.Fe2O3+2H2SO4→2FeSO4+2H2O |
| C.Fe2O3+3H2SO4→Fe2(SO4)3+3H2↑ |
| D.Fe2O3+3H2SO4→Fe2(SO4)3+3H2O |
物质X可发生“X + 酸 → 盐 + H2O”的反应,则X可能是
| A.Fe | B.CO2 | C.H2SO4 | D.NaOH |
下列事实不能证明甲的金属活动性比乙强的是
| A.甲能与盐酸反应而乙不能 |
| B.甲能从乙的盐溶液中置换出乙 |
| C.化合物中甲元素显+2价而乙元素显+3价 |
| D.自然界中甲元素只以化合物形式存在,乙元素有单质形式存在 |
可观察到明显现象的实验是
| A.向盐酸中滴加氢氧化钠溶液 | B.向盐酸中滴加酚酞 |
| C.将铜丝放入到硝酸银溶液 | D.将铁丝放入到硫酸铝溶液中 |
类推是学习中常用的思维方法,现有以下类推结果,其中错误的是
①碱的水溶液通常呈碱性,所以碱性溶液一定是碱的溶液
②氧化物都含有氧元素,所以含氧元素的化合物一定是氧化物
③酸碱发生中和反应生成盐和水,所以生成水的反应一定是中和反应
| A.只有① | B.①② | C.①③ | D.①②③ |
下列实验方案或措施不合理的是
| A.用稀盐酸清除铁制品表面的铁锈 |
| B.用紫色石蕊鉴别稀盐酸和稀硫酸 |
| C.用CO2鉴别NaOH和Ca(OH)2溶液 |
| D.用盐酸鉴别铁粉和铜粉 |
在CuCl2和MgCl2的混合溶液中加过量锌粉,充分反应后过滤,留在滤纸上的物质是
| A.Cu | B.Cu和Zn | C.Cu和Mg | D.Zn、Mg和Cu |
某化学兴趣小组为验证Ag、Fe、Cu三种金属的活动性顺序,设计了如下图所示的实验操作。其中可以达到实验目的的组合是( )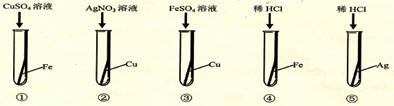
| A.②③ | B.②④ | C.④⑤ | D.①③ |
物质的量相等的铝粉和铁粉分别与质量、浓度均相同的稀硫酸充分反应,反应如图,则判断正确的是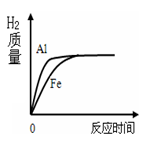
| A.铝粉、铁粉和硫酸均有剩余 |
| B.硫酸、铁粉均反应完,铝粉有剩余 |
| C.铝粉、铁粉均反应完,硫酸有剩余 |
| D.硫酸、铝粉均反应完,铁粉有剩余 |
请根据要求填空:
(1)胃液里含有的酸 (填化学式)
(2)“金银铜铁锡”俗称五金,其中金属活动性最强的是 ;在某黄金样品上滴加稀盐酸后,看到样品表面有气泡产生,说明此样品为 (选填“真”或“假”)黄金
(3)人体内最多的金属元素是 (填化学式)
(4)金属能导电,一般导线都是用金属 制成
(5)金属冶炼通常使矿石中金属元素转变为_______(填“化合”或“游离”)态。
(6)酸有多种分类方法,如下表格:
| 一元酸 |
酸根 |
二元酸 |
酸根 |
| HCl |
Cl |
H2SO4 |
SO4 |
| HNO3 |
NO3 |
H2CO3 |
CO3 |
| CH3COOH |
CH3COO |
|
|
根据以上分类信息,区分一元酸和二元酸的依据是:
将X溶液逐滴滴入Y溶液中,在滴加过程中,Y溶液的pH变化情况如图所示。
| 溶液 |
A组 |
B组 |
C组 |
D组 |
| X |
盐酸 |
盐酸 |
氢氧化钙 |
氢氧化钙 |
| Y |
氢氧化钙 |
水 |
盐酸 |
水 |
(1)表格中符合这种变化情况的是 组(填写编号),理由是
(2)处于图中m点时,溶液中的溶质为 。
有氧化铁、稀盐酸、二氧化硫、氢氧化钠、碳酸钙五种物质,其中有一种物质能与其它三种物质发生化学反应,则该物质是 ;其中属于酸性氧化物的物质是 ,写出氧化铁和稀盐酸反应的现象: ;
造纸厂会产生含氢氧化钠的废水,需经处理呈中性后排放。为测定此废水中氢氧化钠的质量分数,工作人员取了40g废水样品加入到锥形瓶中,逐滴加入10%的稀硫酸,至恰好完全反应时,消耗稀硫酸49 g。计算废水中氢氧化钠的质量分数。
现有三瓶失去标签的无色液体,它们是稀盐酸、稀硫酸和浓硫酸。为了鉴别这三种溶液,现各取少量,分别编号为A、B、C,并按下图步骤进行实验,同时观察现象。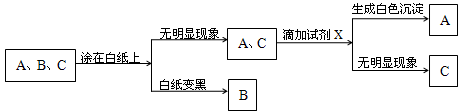
(1)B溶液是 ,由上述实验可知B具有 。
(2)A溶液是 ,试剂X是 ,写出滴加试剂X时反应的化学方程式: 。
此反应 (填“是”或“不是”)置换反应。
使用如图装置进行实验时:
(1)若锥形瓶中充满CO2气体,将滴管中的NaOH溶液滴入瓶中,稍作震荡,发现气球鼓起来,其原因是: 。该现象说明NaOH溶液与CO2发生了反应。其化学方程式为: 。
(2)片刻后,取少量锥形瓶中的液体于试管中,滴加稀盐酸,观察到 ,证明NaOH溶液与CO2发生了反应。已知碳酸钠溶液呈碱性,另取少量锥形瓶中的液体于试管中,滴加酚酞,一定能观察到 ,此现象 (填“能”或“不能”)证明NaOH溶液与CO2发生了反应,理由是 。
(3)还有其它气体和溶液的组合也能使气球鼓起来。请举出两种组合:气体是 ;溶液是 。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号