某同学为了测定黄铜屑(由锌和铜形成的合金)样品组成,取四份样品分别加入稀硫酸反应,其实验数据记录如下表。
| 样品 |
第1份 |
第2份 |
第3份 |
第4份 |
| 取样品质量(g) |
50.0 |
50.0 |
50.0 |
50.0 |
| 取稀硫酸质量(g) |
40.0 |
80.0 |
120.0 |
160.0 |
| 产生气体质量(g) |
0.4 |
0.8 |
1.0 |
m |
(1)上表中m的数值是 ;
(2)在四份样品所做实验中,稀硫酸有剩余的是 ;
(3)列式计算黄铜样品中铜的质量分数。
(4)假黄金外观与黄金相似,社会上一些不法分子用黄铜(Cu-Zn合金)假冒黄金进行诈骗活动。为了鉴别黄铜和黄金,以下方法可行的是 。
A.观察颜色 B.灼烧法 C.加稀硫酸 D.磁铁吸引 E.加硝酸银溶液
有一种石灰石样品的成分是碳酸钙和二氧化硅(SiO2是一种不溶于水,不与盐酸反应,耐高温的固体),某化学兴趣小组为测定这种石灰石样品中二氧化硅的质量分数,进行了如下实验:
①称取25.0g石灰石样品,平均分成质量相等的两份,并分别加工成块状和粉末状;
②将100mL稀盐酸平均分成体积相等的两份,并分别倒入两个锥形瓶中;
③将上述两份样品分别投入各盛有50mL稀盐酸(足量)的两个锥形瓶中,测得生成二氧化碳的质量与反应时间的关系如右图所示。请回答:
(1)由图中曲线分析得出,影响该化学反应速率的因素是: 。
(2)若实验测得该石灰石样品中二氧化硅的质量分数为20%,则m的值为多少?(要有计算过程)
(3)若再称取12.5g二氧化硅的质量分数为20%的该石灰石样品进行煅烧,一段时间后冷却至室温,称得剩余固体的质量为10.3g,则10.3g剩余固体中钙元素的质量为 。
实验室常用一定浓度的过氧化氢溶液和二氧化锰固体混合来制取氧气,现取34克过氧化氢溶液与3克二氧化锰混合,反应后剩余物质总质量为36.2克。请计算:
(1)生成氧气的质量为 克;
(2)原过氧化氢溶液中溶质的质量分数为多少?(4分,要求写出计算过程)
我国约在南北朝时就开始冶炼黄铜,黄铜是铜和锌的合金(Cu-Zn),它可用来制造电器零件及日用品。为了测定某黄铜样品中铜的质量分数,取10g该样品向其中加入一定量的稀硫酸,恰好完全反应,产生氢气的质量与加入稀硫酸的质量关系如图所示。请解答下列问题:
(1)完全反应后,生成H2的质量为 。
(2)该黄铜样品中铜的质量分数为多少?(写出计算过程)
为了测定某石灰石中碳酸钙的质量分数,准确称取12.5g石灰石样品,研碎后放入烧杯中,向其中加入足量稀盐酸,(杂质不与盐酸反应,也不溶于水),实验测得的数据如下图所示。(注:CaCO3+2HCl=CaCl2+H2O+CO2↑)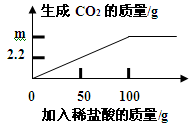
(1)将石灰石样品研碎的目的是 。
(2)12.5g样品完全反应生成二氧化碳的质量m= g。
(3)求该石灰石样品中碳酸钙的质量分数。
向一定量的碳酸钙中加入100克溶质质量分数为7.3%的稀盐酸,恰好完全反应。请计算:
(1)所用碳酸钙的质量;
(2)反应后所得溶液中溶质质量分数是多少?(结果保留到0.1%)
分某班一次社会实践活动是到碱厂参观,该厂主要产品之一是小苏打(碳酸氢钠)。参观结束,同学们带回一些化验室里废弃的小苏打样品,来测定其中碳酸氢钠的质量分数(假设该样品中只含有氯化钠一种杂质)。取样品9.3 g逐滴加入稀盐酸,生成CO2气体的质量与滴加稀盐酸的质量关系如右图所示,求:(计算结果用百分数表示,保留到小数点后一位数字)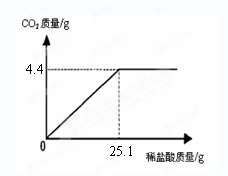
(1)样品中碳酸氢钠的质量分数。
(2)恰好完全反应时,所得溶液中溶质的质量分数。
右图是装有锂(Li)电池的儿童遥控汽车。锂电池放电时发生的化学反应为:Li+MnO2=LiMnO2,
计算3.5gLi参加反应所消耗的MnO2的质量。
已知金属钠与水在常温下反应的化学方程式为:2Na + 2H2O="=2NaOH" + H2↑。若要得到2 g氢气,需要金属钠多少克?
碳是形成化合物种类最多的元素,含碳物质是中学化学研究的主要内容:
(1)自然界CO2来源途径有 (任写一种)。
(2)任何物质都有两面性,CO2对人类的正面影响是 ,不利影响是 。
(3)人类降低空气中的CO2含量的研究有两个方向,一是减少CO2的排放,二是增加CO2的消耗,请写出一条你能做到的消耗CO2的方式或途经 。
(4)A、B、C、D四种物质是初中已学过的主要物质,B、C是组成元素完全相同的化合物;A是固体单质;在一定条件下,A燃烧可生成B或C ;D是实验室制取C的原料。它们之间有如图所示的转化关系(部分物质和反应条件已经略去)。①A在一定条件下可燃烧生成B或C,由此可得出什么结论。
②写出D转化为C的化学方程式。
(5)镁条在空气中燃烧,不仅生成氧化镁,还有少量镁与二氧化碳反应生成一种单质和镁的氧化物。
①写出镁与二氧化碳反应的化学方程式
②通过上述反应,你可以得到哪些信息
(6)称取20g石灰石样品,(假设杂质即不溶于水,也不与其他物质反应),向其中加入100g一定溶质质量分数的稀盐酸,恰好完全反应,称得剩余固液混合物的质量为113.4g。试计算石灰石样品中碳酸钙的质量分数。
某化学兴趣小组为了测定某黄铜(铜、锌合金)样品中锌的质量分数,取10克样品放入烧杯中,再取60克稀硫酸分六次加入烧杯中,俊充分反应,实验数据如下:
| |
第一次 |
第二次 |
第三次 |
第四次 |
第五次 |
第六次 |
| 加入稀硫酸的质量(g) |
10 |
10 |
10 |
10 |
10 |
10 |
| 剩余固体的质量(g) |
9.35 |
8.7 |
8.05 |
7.4 |
6.75 |
6.75 |
(1)黄铜样品中锌的质量分数为多少?(写出计算步骤,下同)
(2)所用稀硫酸的质量分数为多少?
将1.5 g混有铜粉的镁粉投入100g11.76%的稀硫酸中,至不再产生气泡为止,共收集0.1 g气体。过滤后,向所得溶液滴入质量分数为10%的氢氧化钠溶液。开始滴入时无沉淀生成,滴加一定质量的氢氧化钠溶液后开始出现白色沉淀。当滴加氢氧化钠溶液的质量为80g时,恰好得到最多的沉淀量2.9 g。试求:
(1)原混合物中镁的质量分数;
(2)最终所得溶液中溶质的质量分数。(计算结果保留至0.01%)
(3)请画出平面直角坐标图:要求以氢氧化钠溶液的质量为横坐标,产生沉淀的质量为纵坐标,并且标示出起点、折点的坐标
某铁矿石的主要成分是铁的氧化物(假设其他成分均不含铁元素和氧元素)。经测定,该铁的氧化物中氧元素的含量为30%,铁矿石中氧元素的含量为24%。
(1)这种铁的氧化物的化学式是 。
(2)若用一氧化碳还原该铁矿石冶炼生铁,1 t该矿石能生产含铁96%的生铁的质量是
多少?(要求:写出计算过程,计算结果保留小数点后1位)
以氨气(NH3)和二氧化碳为原料可生产尿素,反应的化学方程式如下:
2NH3+ CO2一定条件CO(NH2)2 + H2O
若使3.4 t氨气完全反应,至少需要二氧化碳的质量是多少?
(10分)我国著名化学家侯德榜发明的“联合制碱法”主要原理是:I.向浓氨水中通入足量的CO2,使氨气、水和CO2发生化合反应而生成NH4HCO3溶液;II.向所得溶液中加入食盐细粒,充分搅拌,会析出溶解度较小的小苏打固体并得到化肥溶液;III.加热析出的固体制取纯碱。此法经过调整并应用于化工产业,某化工企业的工艺流程示意图如下:
请完成下列填空:
(1)“联合制碱原理II”中发生反应的化学方程式为 。
(2)在如图的流程中,先加Ca(OH)2溶液的目的是 ,再加入Na2CO3溶液的目的是 。
(3)“操作1”的名称是 ,“氨化溶液”后,溶液的pH 7(填:“大于”、“小于”或“等于”),从而有利于吸收“气体A”,气体A为 (填名称)。
(4)利用“270℃以上小苏打完全分解,纯碱受热不分解”的性质,化学兴趣小组的同学对实验室所购纯碱(假设所含杂质均为小苏打)进行了如下实验:称取20.00g干燥的固体样品放入坩埚,300℃恒温加热至质量不变,在干燥器中冷却后称量残留固体质量为19.38g。
根据题目所给信息,计算该样品中纯碱的质量分数(写出计算过程)。