构建知识网络是一种重要的学习方法。右图是关于铁的化学性质的知识网络(“ → ”表示一种物质转化为另一种物质),其中B是密度最小的气体,C为红色固体单质。请回答下列问题:
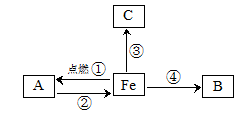
(1)B物质的化学式为 ;
(2)写出反应①的化学方程式 ;
(3)反应②的发生还需要的一种反应物是 (填化学式);
(4)写出反应③的化学方程式,并注明基本反应类型: ( )。
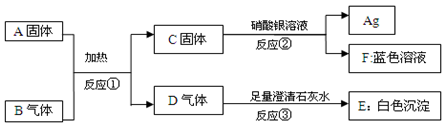
现有A、B、C、D、E、F、G七种物质,C、F是最常见的金属,B密度最小的气体,D为浅绿色溶液,G为蓝色溶液,它们之间存在如下关系:
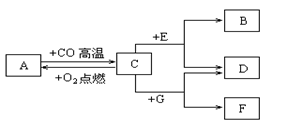
(1)写出下列物质的化学式:B 、F 。
(2)写出C→A发生的化学反应的方程式: 。
(3)写出一种与分别能D、E、G溶液发生置换反应的物质的化学式 。
为了达到收旧利废节能减排的目的,从含有金属镁、铁、铜的粉末中,分离和提取出重要化工原料MgSO4和有关金属,实验过程如下:

请回答:
(1)操作①中被磁铁吸引的金属A是 ;金属B是 。
(2)操作a的名称是 ;在蒸发过程中需要使用玻璃棒,其作用是 。
(3)步骤②所涉及的化学方程 ,该反应基本类型是 。
(4)实验步骤②中除了加入稀硫酸外,还可以选用硫酸铜溶液,请写出反应的化学方程式 。
回收利用废金属是解决废金属造成资源浪费和不同程度的环境污染的方法之一.某市一家大型化工厂处理回收含铜废料的生产流程与部分操作如下:

(注:步骤Ⅰ得到的残留物不溶于水和稀硫酸)
请回答下列问题:
(1)黑色固体
的成分是(用化学式表示)。
(2)流程图中操作①的名称是。
(3)写出步骤Ⅲ的一个反应的化学方程式。
(4)通常在步骤Ⅲ必须加入略过量的"铁屑",原因是。
已知,A、B、C、D四种物质之间存在以下转化关系。其中C是单质,D是相对分子质量最小的氧化物。试回答
(1)写出A、C、D三种物质的化学式:A________、C_________、D_________。
浅绿色溶液B中溶质的化学式_______________。
(2)写出C→D的化学方程式_________________________________。
下图是化学园地中一张表示物质间反应关系的卡片图(“——”表示相连的两种物质能够在溶液体系中发生化学反应),其中A、B、C三处的卡片尚未粘贴。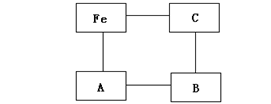
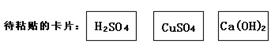
请你思考一种粘贴方案,并回答下列问题:
(1)A处贴上的卡片可以是 (写卡片中的化学式)。
(2)B处卡片中的物质是一种 (选填“酸”、“碱”或“盐”)。
(3)C处卡片中的物质与Fe反应的化学方程式为 。
(4)你认为下列物质可用来替换“Fe”位置的是 (填序号)。
①NaOH ②Zn ③Ag ④Fe2O3
一种工业废水中含有大量的硫酸亚铁、少量硫酸铜和污泥(污泥不溶于水,且不参与化学反应)。某同学设计了一个既经济又合理的实验方案,制备硫酸亚铁晶体(FeSO4·7H2O)并回收铜。方案流程如下:
【查阅资料】FeSO4·7H2O受热易分解。
回答下列问题:
(1)加入过量试剂a的目的是 。
(2)操作③中产生气体的化学方程式是 。
(3)下列说法正确的是 。
| A.溶液1中的溶质质量一定大于溶液2中的溶质质量 |
| B.溶液3中的质量分数大于或等于溶液2 |
| C.操作④中可以用蒸发溶剂结晶的方法 |
| D.操作③中所加物质一定要适量 |
含锌30%的黄铜用作弹壳的制造。现有一批使用过的、锈迹斑斑的弹壳,处理这些弹壳可以制得铜和硫酸锌,其主要过程如下图所示。
提示:弹壳上的锈主要为Cu2(OH) 2CO3,能与稀硫酸反应得到硫酸铜溶液;弹壳中其他杂质不溶于水、不参加反应。
(1)固体D为 。
(2)溶液A中加入E后发生反应的化学方程式为 。
工业废水中含有硫酸亚铁、硫酸铜和污泥。某同学设计了利用废水制备硫酸亚铁晶体(FeSO4·7H2O)并回收铜的实验方案,流程如下:
已知:硫酸亚铁晶体受热易分解。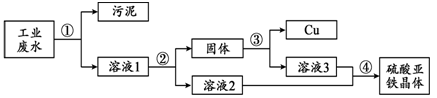
回答下列问题:
(1)步骤②中需加入的物质及目的是 。
(2)步骤③中发生反应的化学方程式为 。
(3)步骤④的操作是蒸发浓缩、降温结晶、 。
某金属冶炼厂的管道烟泥中含有某些单质,其中Cu约占10.3%、Zn约占5.0%、
S约占1.2%。现欲回收铜和锌,并对硫进行环保处理,主要步骤如下图所示: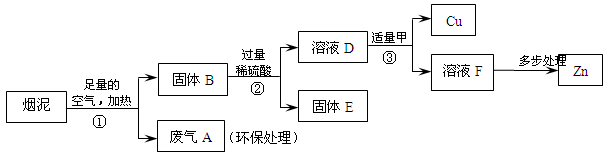
已知:加热的条件下,Zn、Cu都可以与氧气反应生成相应的金属氧化物;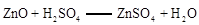 ;
;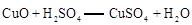
(1)步骤①产生的废气A中,一定含有的有害气体是_____。
(2)步骤③中反应的化学方程式是______________。
(3)下列说法正确的是__________。
a.②、③中的操作均包含过滤
b.溶液D和溶液F中ZnSO4的质量相等
c.溶液D中ZnSO4的质量大于CuSO4的质量
d.若步骤①中空气不足量,不会导致锌的回收率降低
已知:A、B、C、D、E、F是六种常见的物质,其中A是黑色固体,B是无色无味的剧毒气体,C是紫红色金属单质。它们之间的转化关系如图:
请回答:
(1)写出下列物质的化学式:B 、C 、E 。
(2)写出反应①的化学反应方程式: 。
(3)写出反应②的化学反应方程式: ;
该反应属于基本反应类型中的 反应。
铁是生产、生活中应用广泛的金属材料。
(1)在酱油中加入铁强化剂,可预防 (填“佝偻病”、“贫血”或“骨质疏松”)。
(2)某种含铁粉的麦片,食用后在胃酸(盐酸)作用下将铁粉转化为人体可吸收的铁元素,反应的化学方程式为 。
(3)对铁质零件进行“发蓝”处理后,其表面会形成致密氧化膜,从而有效避免腐蚀。
①致密氧化膜能有效阻止铁锈蚀的原因是________________。
②为检验“发蓝”处理的铁质零件表面是否形成致密氧化膜,将该零件浸泡于硫酸铜溶液中,发现零件表面出现红色物质,由此可知“发蓝”处理效果不好,因为________________(用化学方程式表示)。
(4)某同学对X、银、铜、铁四种金属混合物的成分进行探究,流程如下: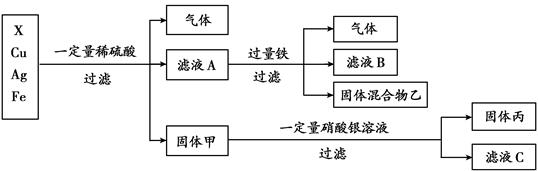
①四种金属的活动性由强到弱的顺序是 。
②固体丙的组成可能是 。
A—F表示初中化学常见的物质,A和B、B和C都能发生反应,且都只能生成两种产物,它们之间的转化关系如图所示。若B是目前世界上年产量最高的金属,D是一种红的单质,F是一种气体。
(1)写出D物质的一种用途 。
(2)反应①的基本反应类型为 。
(3)反应②的化学方程式为 。
工业上生产电路板及处理废液的工艺流程如下:
(1)由步骤①可判断FeCl3与铜反应生成的两种产物是________和________。
(2)步骤②加入过量的铁粉,除能与废液中FeCl3反应外,还可发生的化学反应方程式为______________________。
(3)步骤③加入稀盐酸,充分搅拌,当观察到________________________时,说明滤渣只剩铜。
(4)步骤②③所得FeCl2可与一种单质发生化合反应生成FeCl3,实现循环使用。根据质量守恒定律可推测该单质的化学式为___________。