将等质量的锌粉和铁粉分别与溶质质量分数相同且等质量的稀硫酸充分反应,产生氢气的质量与时间的关系如图所示。请回答下列问题: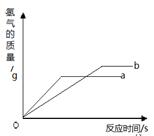
(1)表示锌粉与稀硫酸反应的曲线是: (填 a 或 b)
(2)对于曲线a表示的反应, (填化学式)有剩余。
(3)若有一种金属剩余,则剩余的金属一定是 (填化学式)
氯化铁溶液能与铜反应生成可溶性的氯化铜和氯化亚铁,工业上常用此原理生产印刷线路板。以下是印刷线路板的生产及废液的处理过程:
请回答下列问题:
(1)步骤②③中实验操作的名称是 。
步骤②中发生了两个反应:2FeCl3+Fe = 3FeCl2和 ;
(2)步骤③中适量稀盐酸的标志是 ;
发生反应的化学方程式是 。
(3)该流程中可以循环、回收利用的物质是 。
根据下列图示的探究过程,回答下列问题:

(1)操作①的名称.
(2)图中固体中含有的物质(化学式).
(3)写出步骤②发生反应的化学方程式.
铝在工业和生活中应用广泛。
(1)铝是地壳中含量最高的(填"金属"或"非金属")元素,其年产量已跃居第二位。
(2)铝可制成电线,主要是利用其有良好的延展性和性。
(3)铝制品具有很好的抗腐蚀性能,其原因是。
如图所示,将一个塑料小球放入盛有硫酸铜溶液的烧杯中,小球漂浮于液面,将足量的铁粉投入到烧杯中,充分反应后,观察到铁粉表面有红色物质析出,写出有关反应的化学方程式 ;若溶液体积变化忽略不计,则塑料小球浸入液体中的体积跟原来相比 .

运用酸、碱、盐的性质可以解决工业生产中的许多问题。
(1)工业上常选用来除去铁锈。(写出一种具体物质)
(2)某工厂向含有
、
的废水中加入一定量的锌粉(
)以回收金属,充分反应后,得到的金属组成可能有哪几种情况?。
"铁、锌、铜、镁、铝"是生活中常见的金属。请根据所学知识回答下列问题:
(1)铝块能制成铝箔是利用了铝的性;
(2)黄铜是铜锌合金,其硬度比纯铜(填"大"或"小")。
(3)将一定质量的锌粒投入含有
和
的混合溶液中,充分反应后过滤,若滤液中只含一种溶质,则滤渣中一定含有;
(4)将等质量的镁、铁、锌三种金属分别放入三份溶质质量分数相等的稀盐酸 中。生成氢气的质量与反应时间的关系如图所示。金属
是(填化学式,下同),反应后可能已经反应完的金属是,一定有剩余的金属是。

铝铁铜银是常见的金属。
(1)铝比铁活泼,但铝在空气中比铁稳定,原因是。
A.铝的密度比铁小
B.铝在地壳中含量比铁高
C.在空气中铝的表面能够形成一层致密的氧化膜
(2)用
、
和溶液可以一次性验证
、
、
三种金属的活动性顺序。
(3)写出用稀盐酸和铁锈(主要成分为
)反应的化学方程式。
阅读下面的科普短文,回答问题。
同学们一定见过晶莹剔透的水晶,你知道它的成分吗?其实水晶的主要成分是二氧化硅(SiO 2),二氧化硅是一种无色晶体,熔点很高,硬度很大,不溶于水,常温下二氧化硅能与强碱溶液缓慢反应。SiO 2在高温条件下能与CaO反应生成CaSiO 3,二氧化硅不与水反应,也不与一般的酸反应,却可以与氢氟酸反应。
二氧化硅用途十分广泛。玻璃中含有二氧化硅,此外,二氧化硅还用于制造光导纤维、电子部件等等。今后二氧化硅将更好地服务于我们的生产生活。
(1)写出二氧化硅的物理性质 (答出一点);
(2)用氢氟酸将精美的图案刻蚀在玻璃上,该过程属于 变化(填"物理"或"化学");
(3)二氧化硅与氢氧化钠反应的化学方程式为:SiO 2+2NaOH=X+H 2O,X的化学式是 ,因此实验室中储存氢氧化钠溶液的试剂瓶应用 (填"玻璃塞"或"橡胶塞")。
人类每年要提取数以亿吨计的金属,用于工农业生产和其他领域。
(1)汽车电路中一般用铜作导线,这是利用铜的 ;汽车车体表面喷漆不仅美观,而且可有效防止铁与 接触而生锈。
(2)炼铁的原理是利用一氧化碳和氧化铁的反应,化学方程式为 。
(3)某化工厂排出澄清的废水,其中可能含有的离子是Ba2+、Fe3+、Fe2+、Ag+、Cu2+、SO42-、Cl-、NO3-。[已知:白色的Fe(OH)2沉淀在空气中会迅速转化为红褐色的Fe(OH)3。]
①取少量废水,加入过量稀盐酸,产生白色沉淀的化学式为 。过滤,将滤液分成两份,一份加入稀硫酸,产生白色沉淀的化学式为 ;另一份加入过量NaOH溶液,产生蓝色沉淀,该过程中与OH-反应的离子是 (写离子符号)。
②某化学兴趣小组设计了一个处理该废水的实验方案,部分流程如下:
下列说法正确的是 (填字母)。
| A.固体A中一定含有Ag和Cu,可能含有Fe |
| B.溶液B中的溶质有Ba(NO3)2、Fe(NO3)2 |
| C.废水中含有Ba2+、Ag+、Cu2+、Fe2+、NO3 |
| D.通过该流程可以除去废水中原有的金属离子 |
化学与我们的生产、生活息息相关。请回答下列问题。
(1)①食盐、②熟石灰、③小苏打、④石墨四种物质在生产、生活中用途广泛。其中可用于制铅笔芯的是 (填数字序号,下同);可用作面点发酵剂的是 ;常用作食品加工调味的是 ;常用于改良酸性土壤的是 。
(2)农业上,碳酸钾(K2CO3)可用作 (填“磷”或“钾”)肥。已知碳酸钾溶液呈碱性,则碳酸钾 (填“能”或“不能”)与铵态氮肥混合施用。
铁是生产、生活中应用很广泛的一种金属。下列是与铁的性质有关的部分实验图,请回答下列问题。
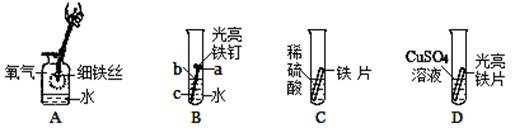
(1)A中发生反应的化学方程式是 ,集气瓶中水的作用是 。
(2)铁生锈的条件是 ,B中铁钉最易生锈的部位是 (填“a”、“b”或“c”)。
(3)C试管中刚好完全反应,得到溶液中溶质的化学式是 。
(4)D中反应一段时间后,现象是 ,试管内固体质量比反应前增大,据此推断,试管内溶液质量与反应前相比 (填“增大”、“不变”或“减小”)。
人类的生产和生活都离不开金属。
(1)生铁和钢中最主要的元素是;用铝壶烧水主要利用铝具有良好的性。
(2)铝制品有良好的抗腐蚀性,其原因是在空气中铝的表面易形成致密的。
(3)验证
、
、
的金属活动性顺序,可选择的试剂是(填字母序号)。
| A. |
、
、
溶液
|
B. | 、 、 溶液 |
| C. | 、 、 溶液 | D. | 、 、 、稀硫酸 |
化学小组探究镁、铁、铜三种金属的活动性顺序,设计了下图所示实验方案。
(1)试管乙中观察到的现象是 ,反应的化学方程式为 。
(2)同学们经讨论后认为该方案可以优化, 试管的实验是多余的。
(3)去掉多余的实验,同学们将另两只试管中反应后的物质倒入同一大烧杯中,一段时间后过滤,向滤渣中加入稀硫酸,有气泡产生,则滤渣的成分可能是 。