某工厂废液中含有氯化钠.氯化铜和氯化亚铁。某课外小组要从废液中回收铜并得到铁红(主要成分Fe2O3),要求全过程不引入其他金属元素。设计实验方案如下图所示,
回答下列问题。
(1)固体甲_______,操作a的名称是_______。
(2)工厂废液中加入过量A反应的化学方程式为 。
(3)溶液甲中的金属离子是 (写离子符号)。
(4)步骤①②③中所发生的化学反应,其中属于置换反应的是 (填序号)。
(4分)生活中有许多铜制品,如:铜暖手炉、铜雕塑、铜芯线、铜工艺品等等。
(1)其中作铜芯线是利用了铜的 (物理性质) 。
(2)东汉晚期的青铜奔马(马踏飞燕)是我国的旅游标志,但由于时间过长已经满身“绿锈”。和铁生锈类似,铜在空气中被腐蚀生成了绿色的碱式碳酸铜 ,根据它的组成判断,可能是铜和空气中的 、 、 (填化学式)共同发生了化学反应。
,根据它的组成判断,可能是铜和空气中的 、 、 (填化学式)共同发生了化学反应。
(3)孔雀石是一种主要含有绿色碱式碳酸铜的矿石。人们发现:森林火灾后,孔雀石表明往往有红色物质出现。提示:Cu2(OH)2CO3===2CuO+H2O+CO2↑试写出产生红色物质的其中一个化学方程式 。
(4)碱式碳酸铜又可以表示为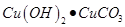 ,取少量碱式碳酸铜溶于适量稀盐酸中,得到蓝色的溶液,其溶质为 (填化学式)。
,取少量碱式碳酸铜溶于适量稀盐酸中,得到蓝色的溶液,其溶质为 (填化学式)。
阅读下列材料,回答问题。(1)﹣(4)请在答题卡选择题区域填涂作答。
新型工程结构材料一蠕墨铸铁
在高碳铁液中加入稀土合金,得到断口呈“花斑”状,石墨为蠕虫状蠕墨铸铁(又称蠕铁)。蠕铁是具有片状和球状石墨之间的过渡形态铸铁,是一种具有良好力学性能(耐高温、强度大、断面敏感性小)、导热率高和抗氧化性能的新型工程结构材料。蠕铁广泛用于制造汽车发动机、汽车制动零件、排气管等。
国产蠕铁中的蠕化剂均含有稀土元素,如稀土硅铁镁合金、稀土硅钙合金等。国产蠕铁技术冲破了国外的技术封锁,助推我国发动机制造技术迈向世界领先水平。
(1)蠕状石墨属于 (A.单质B.化合物)。
(2)片状石墨、球状石墨内部 ( A.原子种类 B.原子排列方式)不同。
(3)蠕墨铸铁从材料分类看属于 (A.有机材料 B.合金)。
(4)蠕墨铸铁作为发动机材料主要是利用其独特的 (A.物理 B.化学)性质。
(5)请简述高端材料国产化的重要性: 。
金属材料与我们的生活息息相关。
(1)下列用品所使用的主要材料,属于金属材料的是 ;
(2)人们大量使用的是合金而不是纯金属,这是因为合金具有更多优良性能,例如钢比纯铁硬度 (填“大”或“小”)。
(3)目前世界上已有50%以上的废钢铁得到回收利用,其目的是 。
A.节约金属资源 B.合理开采矿物 C.防止钢铁生锈.
(4)铜与另一种金属M的混合物(M可能是Al、Fe或Ag),在该混合物中加入足量的稀硫酸有气泡产生,则M不可能是 ,待反应完成后 (填实验操作方法),得到铜和滤液,在滤液中加入锌片,其表面有一层黑色物质,则M是 。取一定量的原混合物投入到一定量的AgNO3溶液中,充分反应后,对反应所得溶液和固体推断正确的是 。
A.溶液中一定有M的离子 B.固体中一定有Ag和Cu
C.固体中一定有Ag D.溶液中一定有Ag+
(4分)某化学兴趣小组对一包含有铜、银、锰的混合金属粉末进行了分离,获得了一种金属和一种盐的晶体。他们将三种金属随意编号为A、B、C,并设计了如下流程: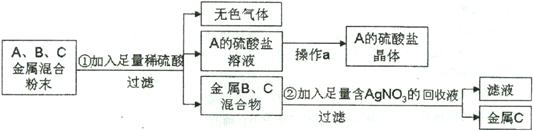
(1)金属B是 (填元素符号),操作a的名称是 。
(2)已知A的硫酸盐中A元素显+2价,请写出①、②反应的化学方程式:
① ;
② ;
应用广泛的金属。没有金属,生活是难以想象的。请你根据所学知识回答下列问题:
(1)某炼铁厂常以焦炭、赤铁矿、空气等为主要原料炼铁,反应过程如下图所示。
其中焦炭的作用是__________,写出碳与二氧化碳反应的化学方程式 。
(2)生产钛(Ti)的部分工艺流程图如下:
写出镁与四氯化钛(TiCl4)发生反应的化学方程式 ;该反应属于 反应(填基本反应类型名称)。上述反应需在氩气环境中进行,理由是 。
(3)将一定量的锌加入到稀硫酸、硫酸亚铁和硫酸铜的混合溶液中,反应停止后过滤,得到滤渣和滤液。向滤渣中滴加稀盐酸,有气泡产生。则滤渣中一定含有 (填化学式),滤液中一定含有的溶质是 (填化学式)。
(4)一定质量含杂质的铁(杂质不溶于水,也不参与反应)与100 g16%硫酸铜溶液恰好完全反应,过滤得到干燥的固体6.8 g,则含杂质的铁中的铁的质量分数是 (计算结果保留至0.1%)。
写出下列反应的化学方程式,并在括号内注明基本反应类型:
(1)硫在氧气中燃烧,()反应。
(2)锌与稀硫酸的反应。
(3)二氧化碳使澄清石灰水变浑浊。
化学实验室要从X、银、铜、锌四种金属混合物中分离某贵重金属。流程如下:(未做特别说明的“固体”,可能为纯净物或混合物)
(1)四种金属的活动性由强到弱的顺序是 ;
(2)过滤操作中用到的玻璃仪器有烧杯、漏斗和 ,其作用是 ;
(3)滤液A中共含有 种溶质,固体丙中一定含有的金属是 ;
(4)写出③中反应的化学方程式 ;
(5)为了检验滤液C中的溶质成分:向其中加入稀盐酸,有白色沉淀产生,则滤液C中一定含有的阳离子 (填离子符号)。
(6分)铁、铜等金属在我们的生活和工业生产中应用很广。某工厂利用废铁丝、硫酸铜废液(含硫酸亚铁)和废铜粉制备硫酸铜晶体。具体过程如下:
(1)将废铁丝投入到硫酸铜废液里发生反应的化学方程式为 ;反应类型为 。(填基本反应类型)
(2)操作Ⅰ的名称是 。
(3)在氧化铜(含少量铜)转化为硫酸铜溶液的过程中,下列化学反应不可能发生的是 (填序号)。
A.2Cu+ O2 2CuO 2CuO |
B.2Cu+O2+2H2SO4 2CuSO4+2H2O 2CuSO4+2H2O |
C.Cu + H2SO4  CuSO4 + H2 ↑ CuSO4 + H2 ↑ |
D.CuO + H2SO4  CuSO4 + H2O CuSO4 + H2O |
在Cu(NO3)2、A1(NO3)3和AgNO3的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤出的固体上滴加稀硫酸时有气泡产生。则反应后所得溶液中含有的金属离子有 ;反应后溶液的质量比原混合溶液的质量 (填“大”或“小”);有关反应的化学方程式为 (写出一个即可)。
木炭还原氧化铜实验后的混合粉末中含有铜、氧化铜、木炭粉,某化学实验小组设计回收铜的方案如下:
(1)过滤操作中必须用到的玻璃仪器有烧杯、玻璃棒和 ,其中玻璃棒的作用是 。
(2)反应①的化学方程式为 。
(3)滤液Ⅱ中的溶质为 。
(4)试剂A最好选用下列 溶液(填序号)。
①H2SO4 ②CuSO4 ③MgSO4
(5)为了完善实验方案,可对滤渣Ⅰ中的 进行回收。
金属在生产和生活中具有广泛的应用。
(1)下列金属制品中,利用金属导热性的是_________(填字母)。

(2)为防止铁制品锈蚀,常在铁制品表面喷漆,防锈原理是使铁制品与 和 隔绝。铝的化学性质比铁活泼,但通常铝制品比铁制品更耐腐蚀的原因是(用化学方程式表示) 。
(3)某兴趣小组欲探究Fe、Cu、Ag、R四种金属的活动性顺序(R为未知金属),进行了如下实验(提供药品:四种金属、稀硫酸、硫酸铜溶液、硫酸亚铁溶液、硝酸银溶液):

①如图A所示,将四根金属丝同时插入烧杯中。甲烧杯中可观察到的现象是铁丝表面产生 ,溶液由无色变为浅绿色。乙烧杯中铁丝表面出现红色固体,银表面无明显现象,则乙中发生反应的化学方程式是 。
②一段时间后,将烧杯中铁丝替换为R进行实验,如图B所示。若甲中出现气泡,乙中无明显现象,则烧杯乙中的溶液是 (请选用提供药品填写),可得出Fe、Cu、Ag、R的活动性顺序由强到弱为 。
通过钝化的方式使锌制品表面形成一层保护膜,可有效防止锌的腐蚀。某锌制品的钝化液含有硝酸银、硝酸铜、重铬酸等,其中重铬酸是一种可溶性的酸。
(1)该钝化液
。 (填"
"、"
"或"
")
(2)重铬酸(
)中铬元素的化合价为。
(3)反应过程中会产生含有金属单质的细微颗粒,该颗粒中一定含有的金属是。
实验是学习化学的重要途径,也是培养同学们兴趣的重要手段,结合下列实验,回答问题。
(1)为加深对燃烧条件的认识,进一步了解灭火的原理。某同学进行了探究实验:
如图1所示:将同样大小的乒乓球碎片和滤纸碎片放在薄铜片的两侧,加热铜片的中部,可以观察到__________________先燃烧,可以得出燃烧的条件之一是 ;
(2)化学兴趣小组的同学进行金属活动性的实验,如图2所示:
a.试管丙中反应的化学方程式为
b.同学们经讨论后认为该方案可以优化, 试管的实验是多余的。同学经讨论得出三种 金属的活动性由强到弱的顺序为
c.去掉多余的实验,同学们将另两只试管中反应后的物质倒入同一大烧杯中,一段时间后过滤,得到不溶物和滤液,并对不溶物的成分进行如下探究:
【提出问题】烧杯中不溶物的成分是什么?
【实验探究】向过滤得到的不溶物中加稀硫酸,若有气泡产生,则不溶物中一定含有
某兴趣小组同学为了验证铜、铁、银的金属活动性强弱,进行了如下的实验研究。
| 实验设计 |
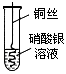 甲 |
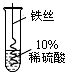 乙 |
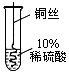 丙 |
| 实验现象 |
观察到现象 (8) |
铁丝表面有气泡产生 |
铜丝表面无气泡产生 |
| 实验结论 |
金属活动性:铁 > 铜 > 银 |
①实验前需要配制10%的稀硫酸,用到仪器有烧杯、量筒、胶头滴管,还缺少的一种仪器是(9) 。量取蒸馏水体积时,若仰视读数,则会导致硫酸溶质质量分数 (10) 10%(填“>”“<”、“=”)。
②铁丝与稀硫酸反应一段时间后剩余的溶液中,可能含有的溶质是 (11) ,为了确定可能含有的溶质,可加入 (12) (填选项序号)
A.铁 B.氯化钡溶液 C.氯化钠溶液 D.氢氧化铜
③ 拓展应用:硫酸铜溶液和熟石灰混合,可制农药波尔多液。不能用铁制容器盛放波尔多液的原因是 (13) (用化学方程式表示)