如图甲是A、B、C三种固体物质的溶解度曲线图。
(1)甲图中,t2℃时,A、B、C三种物质中,溶解度最大的是 ,P点所表示的含义为 。
(2)①将t2℃时A、B、C三种物质的饱和溶液降温到t1℃时三种物质的溶质质量分数由大到小的顺序是 ;
②如乙图所示,20℃时,把试管放入盛有X的饱和溶液的烧杯中,在试管中加入几小段镁条,再加入5mL稀盐酸,立即产生大量的气泡,同时烧杯中出现浑浊,则X可能为A、B、C三种固体物质中的哪一种? 。
水是生命的源泉,下列变化与水相关。请回答:
①二氧化碳溶于水发生反应的化学方程式是 (1) 。
②自来水厂净水过程中常用到活性炭,其作用是 (2) 。
③铁丝在氧气中燃烧时,集气瓶内放少量水的目的是 (3) 。
④除去粗盐中泥沙等难溶性杂质的实验步骤:

I. 操作a的名称是 (4) ;
II. 三个步骤都用到的玻璃仪器是 (5) 。
⑤甲和乙两种固体物质(不含结晶水)的溶解度曲线如下图所示,回答下列问题:
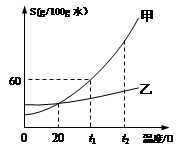
I.在 (6) ℃时,甲和乙两种物质的溶解度相等。
II.t1℃时,将50g固体甲加到50g水中,充分搅拌后所得溶液的质量为 (7) g。
III.甲的饱和溶液中含有少量的乙,由该液体得到固体甲采用的方法是 (8) 。
IV.若将甲物质的不饱和溶液变为饱和溶液,下列说法正确的是 (9) 。
A.溶剂的质量一定变小 B.溶质的质量可能不变
C.溶质的质量分数一定变大 D.溶液的质量变大
⑥下图是对20℃一定质量的丙溶液进行恒温蒸发结晶的实验过程,请回答:
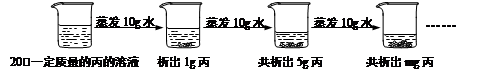
I.蒸发前原溶液是 (10) (填“饱和”或“不饱和”)溶液;m的数值是 (11) 。
II.依据上述实验,你认为丙的溶解度随温度变化的趋势是 (12) (填字母)。
A.随温度升高而增大 B.随温度升高而减小 C.无法判断
农业生产上常需要用质量分数为12%的氯化钠溶液选种。下图是小军实验操作过程示意图:

(1)图中一处明显错误的操作是 (填序号)
(2)现用质量分数为12%的氯化钠溶液(密度约为l.09g/cm3),配制50g质量分数为6%的氯化钠溶液。需要质量分数12%的氯化钠溶液 mL(计算结果精确到0.l),需要水 mL(水的密度为1g/cm3)。
(3)配制50g 6%氯化钠溶液,若用量筒量取水时俯视读数(其他操作正确),则溶液的质量分数________6%(填“>”、“<”或“=”)。
如图所示,在室温下的饱和食盐水中放了一个塑料小球。
(1)现加入少量食盐晶体,充分搅拌和静止后,在温度不变的情况下,小球在液面沉浮情况有何变化 。
(2)若要在不用外力的情况下使小球略上浮,你准备采取的具体方法是 或 。
下表为氯化钠和氯化铵在不同温度时的溶解度,回答下列问题:
| 温度/℃ |
0 |
10 |
20 |
30 |
40 |
50 |
|
溶解度 |
29.4 |
33.3 |
37.2 |
41.4 |
45.8 |
50.4 |
|
溶解度 |
35.7 |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
(1)由表中数据可知,溶解度随温度变化较大的物质是。
(2)20℃时,100
水最多只能溶解
,氯化钠与氯化铵溶解度相等的温度在℃之间。
(3)向烧杯中加100
水和50.0
氯化铵配成50℃的溶液,再冷却到20℃,烧杯中析出固体为
。
0.2%~0.5%的过氧乙酸[化学式(
)]溶液是一种杀菌能力强的高效消毒剂。
(1)过氧乙酸分子中
、
、
原子的个数比为;
(2)欲配制0.4%的过氧乙酸溶液1000g,需用20%的过氧乙酸溶液克。
现有一瓶混有少量氯化钾的硝酸钾粉末,请参照如图KCl和KNO3的溶解度曲线,回答下列问题:

(1)t℃时KCl的溶解度 KNO3的溶解度(填“大于”“小于”或“等于”).
(2)60℃时 g KNO3溶于50g水中恰好形成饱和溶液.
(3)设计实验方案提纯KNO3.
实验方案:在提纯混有少量氯化钾的硝酸钾时,先在较高温下将混合物溶于水中形成热的浓溶液,然后 ,即有大量硝酸钾晶体析出,再进行 操作,即可分离得到较为纯净的硝酸钾晶体.
(1)在H、C、O、Ca四种元素中,选择适当的元素组成符合下列要求的物质。(填写化学式)
①沼气的主要成分 ,
②最常见的溶剂
③可被人体直接吸收的糖 ,
④常用的食品干燥剂
(2)水和空气是人类赖以生存的自然资源。
①下列有关水和空气的叙述中正确的是
A.人们饮用的纯净水中不含任何化学物质
B.水是生命之源,保护水资源包括防止水体污染和节约用水两方面
C.目前计入空气质量日报的主要污染物中已包括了二氧化碳
D.充分利用太阳能、氢能等清洁能源可减少酸雨、温室效应等环境问题的发生
②铁制品在空气中易锈蚀,其实质是铁与空气中的 等接触后发生了化学反应。
③溶解了较多的可溶性钙和镁的化合物的水属于硬水,生活中一般可用 的方法来降低水的硬度。
④实验室欲将50g质量分数为6%的氯化钠溶液稀释为3%的稀溶液,需加水的体积为 _mL。
(8分)硝酸钾是初中化学常见的一种盐.请按要求填写下列有关空格:
(1)质量分数为 4.04%的硝酸钾溶液可作为番茄无土栽培的营养液.硝酸钾_______(填“属于”或“不属于”)复合肥.硝酸钾中含有的离子是____、____(填符号).
(2)黑火药爆炸的反应原理是:2KNO3+S+3C K2S+3CO2↑+N2↑.此反应的反应物和生成物中,没有涉及到下列物质类别中的_________(填序号)
K2S+3CO2↑+N2↑.此反应的反应物和生成物中,没有涉及到下列物质类别中的_________(填序号)
| A.单质 |
| B.氧化物 |
| C.酸 |
| D.碱 |
E.盐
(3)如图为硝酸钾和氯化钠两种物质的溶解度曲线示意图,其中曲线a表示 KNO3的溶解度随温度变化的趋势.恒温下欲将接近饱和的KNO3溶液变成饱和溶液,可采取的方法有__________,此过程溶液溶质质量分数一定________(“变大”、“不变”或“变小”)若KNO3固体中含有少量NaCl,可用__________的方法提纯KNO3
(4)在硝酸钾中,质量分数最大的元素是_______(填符号).
以下是氯化钠溶液的配制和粗盐中难溶性杂质的去除(需要计算粗盐的产率)实验的部分操作。

(1)仪器a的名称是 。
(2)完成粗盐提纯的实验上图中正确的操作顺序为 (填字母序号)。
(3)配制6%的氯化钠溶液和粗盐中难溶性杂质的去除都要用到的实验操作是 (填序号)。
(4)A中玻璃棒搅拌的作用是使氯化钠 。D操作中,当观察到蒸发皿中出现 时,停止加热。
(5)用托盘天平称量所需的氯化钠时,发现托盘天平的指针偏向左盘,应 。
| A.增加适量氯化钠固体 | B.减少适量氯化钠固体 |
| C.调节游码 | D.添加砝码 |
(6)用提纯得到的精盐配制了50 g 6%的氯化钠溶液。经检测,溶质质量分数偏小,其原因可能有 (填序号)。
①氯化钠固体仍然不纯 ②称量时砝码端忘垫质量相同的纸片
③量取水时,仰视读数 ④装瓶时,有少量溶液洒出
淮安市某盐化厂生产的碳酸钠粗产品中含有少量氯化钠.碳酸钠和氯化钠的溶解度与温度的关系如图所示,回答下列问题:

(1)t1℃时碳酸钠与氯化钠中溶解度较大的物质是 .
(2)t1℃时碳酸钠溶液升温至t2℃,所得溶液的溶质质量分数 .(填“变大”、“变小”或“不变”).
(3)除去碳酸钠中混有少量氯化钠的方法是 .
小明在实验室欲配制一定质量分数的食盐溶液。
(1)上面的仪器中除B、E外,她必须选用的仪器还有(填字母编号)__________;
(2)E的作用是__________。
如图为甲、乙两种固体物质在水中的溶解度曲线,据此回答下列问题:

(1)在40℃时甲、乙两种固体物质的溶解度 (填“相同”或“不同”).
(2)两种物质中 物质的溶解度随温度的升高而降低.(填“甲”或“乙”)
(3)若要从甲的60℃的饱和溶液中得到甲(固态),应该采用 的方法.(填序号)
A.升高温度到70℃
B.降低温度
C.加入一定量的水.
下表是NaCl和KNO3在不同温度时的溶解度,请根据相关信息回答下列问题。
| 温度/℃ |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
|
| 溶解度/g |
NaCl |
35.7 |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
37.3 |
| KNO3 |
13.3 |
20.9 |
31.6 |
45.8 |
63.9 |
85.5 |
110 |
(1)60℃时,在100 g水里溶解_________g KNO3时,溶液才可达到饱和状态。
(2)下图为NaCl 和KNO3的溶解度曲线,则表示NaCl的溶解度曲线是_________(填“甲”或“乙”);其中温度t的范围可能在________(填字母序号)。
A.10℃~20℃之间 B.20℃~30℃之间
C.30℃~40℃之间 D.40℃~50℃之间
(3)请根据上表或图示总结出一条具有一定规律的结论 。
(4)在0℃时,分别在100 g 水中加入30 g NaCl 和KNO3固体,再加热到60℃时(假设溶剂不损耗),NaCl溶液为______(填“饱和”或“不饱和”)溶液。加热前后,有关两种溶液的说法正确的是_____(填字母序号)。
A.0℃时,两溶液中溶质的质量分数相同
B.60℃时,两溶液中溶质的质量分数相同
C.加热前后,NaCl溶液中溶质的质量分数由小变大
D.加热前后,KNO3溶液中溶质的质量分数不变
配制50g质量分数为5%的氯化钠溶液,下图是某同学配制溶液的操作过程:
(1)写出标号①~④各仪器的名称:
①______________ ②______________ ③______________ ④______________
(2)B操作中应称氯化钠的质量是______________g,称量时若指针偏右,应进行的操作是____________________________。

(3)D操作中仪器⑨的规格应为______________(填“10mL”、“50ml”或“100mL”)读数时应使视线与____________________________保持水平。
(4)E操作的作用是____________________________。
(5)下列错误操作可能导致溶质质量分数偏低的是______________。(填序号)
①B操作中砝码和氯化钠放错托盘 ②D操作中仰视凹液面的最低处读数
⑨D操作时有少量水溅出 ④F操作中溶液洒落