.为测定某地石灰石中碳酸钙的质量分数,兴趣小组同学取一定质量的石灰石于烧杯中,向烧杯中逐渐加入较浓的盐酸,反应过程测得剩余固体质量与加入盐酸的质量关系如图所示(石灰石中的杂质不与盐酸反应,也不溶与水)。请回答下列问题:
(1)石灰石中所含杂质的质量是 g。
(2)通过计算求所用盐酸的溶质质量分数。
(3)兴趣小组同学用测定产生的气体质量来求出石灰石中碳酸钙的质量分数,假如测量准确,通过计算得到的碳酸钙的质量分数比实际数值偏大,其原因可能是: 。
(7分))课外活动时,同学们采用以下两种方法测定某氯化钠溶液的溶质质量分数。
(1)【化学方法】向一定量氯化钠溶液中加入足量硝酸银溶液,得到2.87g氯化银固体,则该氯化钠溶液中氯化钠的质量为多少?(根据化学方程式列式计算)
经多次实验测定,该溶液的溶质质量分数为10%。
(2)【物理方法】取一定量该溶液进行蒸发,测量实验数据如下:
| 蒸发皿的质量(g) |
25.0 |
| 蒸发皿+食盐溶液(g) |
45.0 |
| 蒸发皿+食盐晶体(g) |
27.4 |
| 数据处理 |
溶液的溶质质量分数为 |
若化学方法测定结果准确,则物理方法测定结果产生误差的原因是
A.蒸发时未用玻璃棒搅拌
B.所取氯化钠溶液质量较大
C.蒸发时出现少量晶体时就停止加热
D.实验后未将玻璃棒上的白色固体移入蒸发皿
在一烧杯中盛有60.2gBaCO3和BaCl2的粉末状混合物,向其中加入188.8g水使混合物中可溶物完全溶解,然后向其中逐滴加入溶质质量分数为10%的稀盐酸至146g时恰好反应完全,请根据题意回答问题:
(1)在滴加盐酸过程中观察到的明显实验现象是 。
(2)当盐酸滴加至140g时,烧杯中溶液里含有溶质的是 。(写化学式)
(3)计算恰好反应完全时烧杯中所得不饱和溶液的质量。(结果精确到0.1g)
为了测定碳酸钠样品(内含有氯化钠)的纯度,现将10克样品加入重为5克的烧杯中,再往烧杯中加入40克水搅拌至固体完全溶解,再向烧杯中加入50克稀盐酸,恰好不再产生气泡,称得烧杯总质量为102.8克。
请完成下列计算:
(1)反应产生的气体的质量是多少?
(2)碳酸钠样品中碳酸钠的质量分数是多少?
(3)盐酸溶液中溶质的质量分数是多少?
(7分) 某学生做了如下图所示的实验。
| |
第一次 |
第二次 |
| 加入硫酸铜的质量 |
m |
m |
| 加入氢氧化钠溶液的质量 |
50g(溶质质量分数16%) |
50g(溶质质量分数16%) |
| 加入稀硫酸的质量 |
50g |
100g |
| 实验现象 |
蓝色固体和蓝色溶液 |
蓝色溶液 |
若第二次所加物质恰好完全反应(溶液损失忽略不计),请回答下列问题:
(1)写出实验中发生反应的化学方程式___________________________;
(2)第一次实验后的溶液中所含溶质的化学式为___________________________;
(3)根据已知条件列出求解实验中生成沉淀的质量(x)的比例式______;
(4)实验中加入硫酸铜的质量(m)为______;
(5)在第二次实验中,若向加入氢氧化钠溶液反应后的滤液中加入43.8 g水,则所得溶液中溶质的质量分数为_____________;
(6)若用溶质质量分数为98%的硫酸溶液配制实验中所需的稀硫酸,则需要加水的质量为_________。
学过金属活动性后,秦思同学通过实验探究锌粉与硝酸亚铁和硝酸银两种盐溶液的反应。实验现象和数据如下:
| |
第一次 |
第二次 |
第三次 |
第四次 |
| 硝酸亚铁与硝酸银的混合溶液 |
100g |
100g |
100g |
100g |
| 锌粉 |
2g |
3.25g |
m |
9.75g |
| 向滤液中加入稀盐酸后的实验现象 |
产生白色沉淀 |
无明显现象 |
无明显现象 |
无明显现象 |
| 向滤渣中加入100 g稀盐酸后的实验现象 |
无明显现象 |
无明显现象 |
产生气泡,溶液变为浅绿色 |
现象与第三次相同 |
(1)第四次向滤渣中加入稀盐酸后产生气泡的化学方程式为 ;
(2)根据第一次的实验现象,你认为此次滤液中的溶质是 ;
(3)根据已知条件列出求解第二次实验中置换出金属银的质量(x)的比例式 ;
(4)若第三次实验锌与两种盐溶液恰好完全反应,则m的质量为__________________;
(5)若向第三次反应后的滤液中加入一定质量的水,所得不饱和溶液中溶质的质量分数为10%,则加入水的质量为__________________;
(6)若用溶质质量分数为36.5%的浓盐酸配制第四次实验中与滤渣恰好完全反应所需的稀盐酸,则需要浓盐酸与水的质量比为_______________。
某同学做了如下图所示的实验,在14.6%的稀盐酸中加入碳酸钙,后加入10.6%的碳酸钠溶液
| |
第一次 |
第二次 |
| 14.6%的稀盐酸的质量 |
m |
m |
| 加入碳酸钙的质量 |
10g |
20g |
| 加入10.6%的碳酸钠溶液的质量 |
100g |
200g |
| 加入碳酸钠溶液后,实验现象 |
只有气泡 |
只有白色沉淀 |
若第二次所加物质恰好完全反应(滤液损失忽略不计),请回答下列问题
写出实验一中发生化学反应的方程式
第一次实验中加入碳酸钙后溶液中溶质成分
根据已知条件列出求解第二次实验生成沉淀的质量的比例式
实验中加入稀盐酸m的质量为
若将第二次反应后的溶液蒸发191.2g水,则所得不饱和溶液中溶质的质量分数为
若用溶质质量分数29.2%的浓盐酸配置实验所需的稀盐酸,则需要加水的质量
在稀H2SO4和CuSO4的混合溶液中,加入适量铁粉,使其正好完全反应,反应后经过过滤得到固体物质的质量与所加铁粉的质量相等,则混合溶液中H2SO4与CuSO4的质量比为 。
今有氢氧化钠、碳酸氢钠和与其他物质都不反应,受热也不分解的杂质组成的固体混合物17.110g,放入密闭容器中加热至250℃,经充分反应后,将容器中的气体通入过量的澄清石灰水中得到白色沉淀2.500g;当容器中的残留固体冷却到室温后,全部溶于水制成50.00ml溶液,从中取出10.00ml,恰好可与含HCl 1.825g的盐酸溶液25.00毫升中和至中性,求原混合物中含杂质的质量分数?
(5分) 55.7 g碳酸钠溶液恰好与36.5 g某盐酸溶液完全反应,测得反应后溶液的质量为90 g,求:
(1)生成了多少克二氧化碳?
(2)反应后所得溶液的溶质质量分数是多少?
(3)所用稀盐酸中溶质的质量分数。
“过碳酸钠”(2Na2CO3·3H2O2)俗称固体双氧水,它既有碳酸盐的性质,又有双氧水的不稳定性和氧化性,是很好的消毒剂和供氧剂,广泛应用于洗涤、印染和医药等领域。“过碳酸钠”的制备流程如下:
请回答下列问题:
(1)H2O2在催化或受热条件下易分解,说明化学变化的速度和 相关;
(2)在“过碳酸钠”中加入下列物质时,不会导致“过碳酸钠”变质的是 (填序号)。
| A.二氧化锰 |
B.稀盐酸 |
C.硫酸钠 |
D.石灰水 |
(3)“过碳酸钠”极易分解,得到碳酸钠、水和氧气,其反应方程式可表示为
2(2Na2CO3.3H2O2)==4Na2CO3+6H2O+3O2↑
请通过计算说明(必须有计算的过程):
①若“过碳酸钠”分解产生氧气12g,则同时产生碳酸钠的质量是多少?
②若将上述产生的碳酸钠全部配制成溶质质量分数为10.6%的溶液,共需水多少毫升?
(8分)称取12.5g石灰石(主要成分是CaCO3,杂质不参加反应)放人烧杯中,向其中加入50g稀盐酸,二者恰好完全反应。反应结束后称量烧杯中剩余物质的总质量为58.1g(不包括烧杯的质量,且气体的溶解忽略不计)。试计算石灰石中杂质的质量分数。
实验室用大理石与稀盐酸反应制取CO2,反应后所得溶液体积为40mL.(假设大理石中的杂质不与盐酸反应,反应前后溶液体积不变).向该溶液中匀速逐滴加人Na2CO3溶液 并不断搅拌,测得溶液的pH随时间变化如图所示,该过程 共放出气体660mL(密度为2.0g/L)析出沉淀5.0g.
(1)根据图象可以看出.Na2CO3首先与溶液中的 反应.
(2)本实验制取CO2所用大理石中含CaCO3 g.
(3)已知制取CO2所用稀盐酸的密度为1.06g/Cm3求这种盐酸的质量分数.(计算结果保留1位小数,无计算过程不给分)
将氯化钠和碳酸钠组成的固体混合物18.9克完全溶解于196.8克水中,向该溶液中 加入一定质量的氯化钡溶液恰好完全反应,滤出19.7克沉淀。若将滤液蒸发100克水后,所得溶液溶质质量分数为10%。
计算:(1)蒸发水后所得溶液的质量。
(2)所用氯化钡溶液中溶质的质量分数。
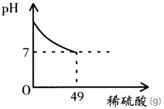
酸和碱发生中和反应,它在日常生活和农业生产中有着广泛的应用。小强同学在做中和反应实验时,向盛有40克10%氢氧化钠溶液的烧杯中逐滴加入稀硫酸,滴加过程如图所示,求所加稀硫酸的溶质质量分数。