(2)一瓶无色气体,可能含有CH4和CH2==CH2,或其中的一种,与一瓶Cl2混合后光照,观察到黄绿色逐渐褪去,瓶壁有少量无色油状小液滴。
①由上述实验现象推断出该瓶气体中一定含有CH4,你认为是否正确,为什么?
。
②上述实验可能涉及的反应类型有 。
(3)含有 的化合物与CH2==CH2一样,在一定条件下可聚合成高分子化合物。
的化合物与CH2==CH2一样,在一定条件下可聚合成高分子化合物。
①广泛用作农用薄膜的聚氯乙烯塑料,是由 聚合而成的,其化学方程式是
聚合而成的,其化学方程式是
。
②电器包装中大量使用的泡沫塑料的主要成份是聚苯乙烯 ,它是由 (写结构简式)聚合而成。
,它是由 (写结构简式)聚合而成。
有一固体化合物A(C14H12NOCl),与6mol/L盐酸回流可得到两个物质B(C7H5O2Cl)和C(C7H10NCl)。B与NaHCO3溶液反应放出CO2。C与NaOH反应后,再和HNO2作用得黄色油状物,与苯磺酰氯反应生成不溶于碱的沉淀。当C与过量CH3Cl加热反应时,得一带有芳环的季铵盐。推出A、B、C的可能结构式。
将硼酸、发烟硫酸、萤石粉共热得到无色气体A,A为平面构型分子,密度约为空气的2.3倍,A用乙醚吸收后得到液态物质B。液态乙酸中存在微弱的自偶电离,离子电导率为139μS/cm,将B加入乙酸中形成均一透明的无色溶液,发现乙酸的离子电导率显著增强,达到1300-5800μS/cm,B与乙酸的混合溶液是具有良好应用前景的非水型电解质,与传统的水溶液电解质体系相比有独特的优势,扩大了电化学反应研究的物质范围和电位研究区间。试回答下列问题:
⑴ 写出A、B的结构简式 A _____________,B______________
⑵ 写出生成A的化学反应方程式____________________________________
⑶ 用方程式表示乙酸的自偶电离过程,并分析乙酸中加入B后,电导率显著提高的原因
⑷ 红外光谱显示,纯乙酸中存在两种羧羟基吸收峰,分析这两种峰产生的原因
⑸ 为什么说非水型电解质可以扩大电化学反应研究的物质范围和电位区间?
银制器皿久置会失去光泽,这并不是仅仅由于氧气的作用,是被“流动的水和游荡的风”所侵蚀,经分析,银器失去光泽是由于其表面形成了X ,X可由以下三种方法除去,从而使银器恢复光泽。
① 将银器置于盛有苏打水的铝制器皿中煮沸
② 将银器在KSCN或NH4SCN溶液中放置几分钟
③ 将银器用A的乙醇-水溶液处理数分钟,X与A反应的物质的量比为1:8,A是 NH4SCN的同分异构体,所有原子均只有一种化学环境。
试回答如下问题:
⑴ 给出X 和 A的化学式,并写出生成X的化学方程式
⑵ 写出除去X的三种方法的化学反应方程式
⑶ 计算X 在水中的溶解度,
已知Ksp,X = 6.3×10-50, X的阴离子对应的酸Ka1=9.5×10-8, Ka2=1.0×10-14
⑷ 试判断X在浓度相同的HNO3与HCl中的溶解性大小,说明你的理由
近期大面积持续“油荒”、“电荒”,严重影响了工业生产,人民的生活,能源成了我们亟待解决的问题.目前,我国的能源结构主要是煤,还有石油、天然气、核能等,这些能源都是一次不可再生且污染环境的能源,研究和开发清洁而又用之不竭的能源是未来发展的首要任务.科学家预测“氢能”将是未来21世纪最理想的新能源.
(1)目前世界上的氢绝大部分是从石油、煤炭和天然气中制取.请写出工业上由天然气制氢气的化学反应方程式.
(2)利用硫-碘热循环法制取氢也是化学家常用的一种方法,总反应方程式为:
2H2O 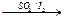 2H2+O2,其循环过程分三步进行:
2H2+O2,其循环过程分三步进行:
(a)SO2+I2+H2O→A+B (b)A→?+? (c)B→?+?+?
①完成以上三步反应,并确定哪步反应最难进行.
②请对硫-碘热循环法制取氢的优劣和前景作一分析.
(8分)下图是一些常见的物质间的转化关系图。C是紫红色金属单质,G是蓝色沉淀,X是葡萄糖溶液,H是砖红色沉淀,F是形成酸雨的无色有害气体,所有反应物、生成物中的水均未标出;反应②的条件是使用浓B溶液和加热。

(1)A是 ,E是 ;
(2)电解A溶液时阴极的反应式 ;
(3)电解A溶液的总反应化学方程式是 。
熵是由德国物理学家克劳休斯于1865年首次提出的一个重要热力学概念。统计物理学研究表明,熵是系统混乱度的量度。熵增加原理的数学表达式是:(ds)U,V≥0。其物理意义是:一个孤立系统的自发过程总是朝着熵增加的方向进行,即从有序走向无序。而生命的发生、演化及成长过程都是从低级到高级、从无序到有序的变化。这样看来把熵增加原理应用到生命科学中似乎是不可能的。
⑴熵增加原理与达尔文进化论是否矛盾?说明理由。
⑵初期的肿瘤患者可以治愈,而晚期癌症患者的肿瘤想要治愈是根本不可能的,用熵增加原理解释其原因。
20世纪60年代,化学家发现了一类酸性比100%的硫酸还要强的酸,称之为魔酸,其酸性强至可以将质子给予δ受体,CF3SO3H就是其中常见的魔酸之一。
⑴试写出CH3CH3与CF3SO3H可能的反应式。
⑵以上反应所得产物活性均很高,立即发生分解,试写出分解以后所得到的全部可能产物。
(5分)胃酸是由胃黏膜的壁细胞分泌的,实际上就是盐酸。正常人的胃液中盐酸浓度大约为0.1 mol·L-1,每日分泌胃酸2 L左右。某胃酸过多患者经测定盐酸浓度为0.126 mol·L-1。医生建议该患者服用Stomachee,按说明书要求服用即可。如图是该药品的标签,根据你所学的化学知识,通过计算回答正常服用此药物能否使该患者的胃酸恢复正常?
1941年从猫薄荷植物中分离出来的荆芥内酯可用作安眠药、抗痉挛药、退热药等。通过荆芥内酯的氢化反应可以得到二氢荆芥内酯,后者是有效的驱虫剂。为研究二氢荆芥内酯的合成和性质,进行如下反应:
写出A、B、C、D和E的结构简式(不考虑立体异构体)。
AX4四面体 (A为中心原子,如硅、锗;X为配位原子,如氧、硫) 在无机化合物中很常见。四面体T1按下图所示方式相连可形成一系列“超四面体”(T2、T3···):
⑴ 上图中T1、T2和T3的化学式分别为AX4、A4X10和A10X20,推出超四面体T4的化学式。
⑵ 分别指出超四面体T3、T4中各有几种环境不同的X原子,每种X原子各连接几个A原子?在上述两种超四面体中每种X原子的数目各是多少?
⑶ 若分别以T1、T2、T3、T4为结构单元共顶点相连(顶点X原子只连接两个A原子),形成无限三维结构,分别写出所得三维骨架的化学式。
⑷ 欲使上述T3超四面体连接所得三维骨架的化学式所带电荷分别为+4、0和-4,A选Zn2+、In3+或Ge4+,X取S2-,给出带三种不同电荷的骨架的化学式(各给出一种,结构单元中的离子数成简单整数比)。
(CN)2被称为拟卤素,它的阴离子CN-作为配体形成的配合物有重要用途。
⑴ HgCl2和Hg(CN)2反应可制得 (CN)2, 写出反应方程式。
⑵画出CN-、(CN)2的路易斯结构式。
⑶写出(CN)2 (g) 在O2 (g) 中燃烧的反应方程式。
⑷ 298 K下,(CN)2 (g) 的标准摩尔燃烧热为-1095 kJ mol-1,C2H2 (g) 的标准摩尔燃烧热为-1300 kJ mol-1,C2H2 (g) 的标准摩尔生成焓为227 kJ mol-1,H2O (l) 的标准摩尔生成焓为-286 kJ mol-1,计算 (CN)2 (g) 的标准摩尔生成焓。
⑸ (CN)2在300~500 oC形成具有一维双链结构的聚合物,画出该聚合物的结构。
⑹电镀厂向含氰化物的电镀废液中加入漂白粉以消除有毒的CN-,写出化学方程式(漂白粉用ClO-表示)。
化合物X是产量大、应用广的二元化合物,大量用作漂白剂、饮水处理剂、消毒剂等。年产量达300万吨的氯酸钠是生产X的原料,92%用于生产X—在酸性水溶液中用盐酸、二氧化硫或草酸还原。此外,将亚氯酸钠固体装柱,通入用空气稀释的氯气氧化,也可生产X。X有极性和顺磁性,不形成二聚体,在碱性溶液里可发生歧化反应。
⑴写出X的分子式和共轭π键( )。
)。
⑵分别写出上述用草酸还原和用氯气氧化生产X的反应方程式。
⑶写出上述X歧化反应的化学方程式。
EDTA是乙二胺四乙酸的英文名称的缩写,市售试剂是其二水合二钠盐。
⑴画出EDTA二钠盐水溶液中浓度最高的阴离子的结构简式。
⑵ Ca(EDTA)2-溶液可用于静脉点滴以排除体内的铅。写出这个排铅反应的化学方程式(用Pb2+ 表示铅)。
⑶能否用EDTA二钠盐溶液代替Ca(EDTA) 2-溶液排铅?为什么?氨和三氧化硫反应得到一种晶体,熔点205oC,不含结晶水。晶体中的分子有一个三重旋转轴,有极性。画出这种分子的结构式,标出正负极。
Na2[Fe(CN)5(NO)]的磁矩为零,给出铁原子的氧化态。Na2[Fe(CN)5(NO)]是鉴定S2-的试剂,二者反应得到紫色溶液,写出鉴定反应的离子方程式。
CaSO4 • 2H2O微溶于水,但在HNO3 ( 1 mol L1)、HClO4 ( 1 mol L-1)中可溶。写出能够解释CaSO4在酸中溶解的反应方程式。
取质量相等的2份PbSO4 (难溶物)粉末,分别加入HNO3 ( 3 mol L-1) 和HClO4 ( 3 mol L-1),充分混合,PbSO4在HNO3 能全溶,而在HClO4中不能全溶。简要解释PbSO4在HNO3中溶解的原因。
X和Y在周期表中相邻。CaCO3与X的单质高温反应,生成化合物B和一种气态氧化物;B与Y的单质反应生成化合物C和X的单质;B水解生成D;C水解生成E,E水解生成尿素。确定B、C、D、E、X和Y。