A、B、C是三种短周期元素,它们的原子序数依次增大。已知A是地壳中含量最多的元素;B元素原子的最外层只有一个电子;C元素的单质在常温下是黄绿色的气体。
(1)写出A、B的元素符号:A_________,B_________。
(2)写出C元素最高价氧化物对应水化物的化学式。
下图转化关系中,A、B、C、D、E都是短周期元素的单质,在常温常压下A是固体,其余都是气体,且C呈黄绿色。化合物H和I两种气体相遇时产生白烟K(NH4Cl)。化合物G的焰色反应为黄色,B为氧气。反应①和②均在溶液中进行。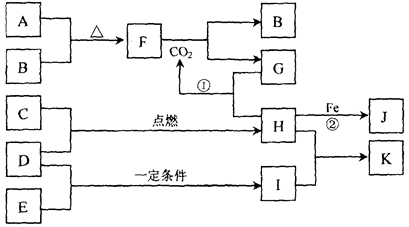
请按要求回答下列问题。
(1)写出下列物质的化学式:D、F。
(2)反应②的离子方程式为。
(3)向K溶液中加入硝酸酸化的硝酸银溶液,反应的现象为。
(4)将少量单质C通入盛有淀粉KI溶液的试管中,液体变为蓝色。这说明单质C的氧化性于单质碘(填“强”或“弱”)。
(5)向J溶液中滴入NaOH溶液时,生成的灰白色沉淀迅速变成灰绿色,最后变成
红褐色。写出红褐色沉淀的化学式:。
已知:(X代表卤素原子,R代表烃基)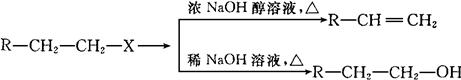
利用上述信息,按以下步骤从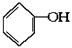 合成
合成 。(部分试剂和反应条件已略去)
。(部分试剂和反应条件已略去)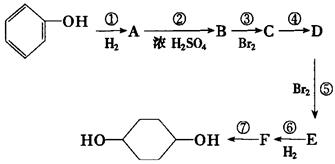
请回答下列问题:
(1)分别写出B、D的结构简式:B_________、D_________。
(2)反应①~⑦中属于消去反应的是_________。(填数字代号)
(3)如果不考虑⑥、⑦反应,对于反应⑤,得到的E可能的结构简式为:_________。
(4)试写出C D反应的化学方程式(有机物写结构简式,并注明反应条件)
D反应的化学方程式(有机物写结构简式,并注明反应条件)
。
现有前4周期中的A、B、C、D、E五种主族元素。A的最高价氧化物含A 40%,A原子中质子数等于中子数;B是同周期中除稀有气体外原子半径最大的元素;D能形成BD型离子化合物,且B、D两离子的电子层结构相同;C和D能形成CD3的化合物;C原子比E原子多1个电子;1.8g C与足量的稀硫酸反应,所产生的氢气在标准状况下的体积为2.24 L;C原子中质子数比中子数少1;D原子比A原子多1个质子。请写出A~E五种元素最高价氧化物对应水化物的化学式、、、
、。
下表是元素周期表的一部分, 针对表中的①~⑨种元素,填写下列空白:
| 主族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0族 |
| 2 |
① |
② |
③ |
|||||
| 3 |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
⑨ |
||
| 4 |
⑩ |
用化学符号回答下列问题:
(1)在这些元素中,最活泼的金属元素是,最活泼的非金属元素是,化学性质最不活泼的是:。
(2)在最高价氧化物的水化物中,酸性最强的化合物的是____ ___,碱性最强的化合物的是:____ _____ ____。
(3)最高价氧化物是两性氧化物的元素是_________;写出它的氧化物与氢氧化钠反应的离子方程式_____________________________________________。
(4)在这些元素中,原子半径最小的是,原子半径最大的是。
(5)表示①与⑧的化合物的分子式,该化合物是由(填“极性”“非极性”下同)键形成的。
(6)用电子式表示元素④与⑦的化合物的形成过程:,该化合物属于(填 “共价”或“离子”)化合物。
某氧化铝样品中含有氧化铁和二氧化硅杂质,(二氧化硅不溶于盐酸)现欲制取纯净的氧化铝,某同学设计如下的实验方案。回答下列问题:
(1)沉淀A的化学式是________________,沉淀B的化学式是________________,滤液A中含有的阳离子为 和 ,滤液B中的含铝元素的化合物化学式是_________ ____;
(2)步骤②中,加过量的氢氧化钠发生的两个反应用化学方程式表示为:
,
。
(3)步骤③的离子方程式为 。
若所加的盐酸为过量,又能发生的反应的化学方程式为:
。
(4)在操作②中要用到的玻璃仪器有 、___________、__________。
(5)步骤④的反应化学方程式为_____________________________________。
可用于提纯或分离物质的常用方法有:①过滤、②结晶、③升华、④分馏、⑤盐析、⑥渗析、⑦加热分解⑧分液等,将分离或提纯的编号填入下列各混合物后面的横线上。
(1)除去碳酸钠固体中混有的碳酸氢钠;
(2)除去石灰水中悬浮的CaCO3颗粒;
(3)除去氯化钠单质中混有的碘单质;
A、B、C、D四种元素,已知A元素是自然界中含量最多的元素;B元素为金属元素,它的原子核外K、L层上电子数之和等于M、N层电子之和;C元素是第3周期第一电离能最小的元素;D元素在第3周期中电负性最大。
(1)试推断A、B、C、D四种元素的名称和符号。
(2)写出上述元素两两化合生成的化合物的化学式。
(10分)有下图所示的反应关系,A是中学常见的无机物,A、B、C中含有同一种元素R,不含R的产物已经略去。
(1)若A与NaOH反应,既可只生成B,又可只生成C,还可生成B+C。
①写出符合上述反应关系的A的2种不同类物质的分子式_________________________,_________________________。
②任选上述一种物质,写出有关离子方程式:
生成B的离子方程式为__________________________________________________________;
生成C的离子方程式为__________________________________________________________。
(2)若A与NaOH无论以何种物质的量比反应,其产物必为B+C,则A的分子式可能是
__________(只写一种),R在A、B、C中的化合价必须满足的条件是______________________,该反应的离子方程式为
__________________________________________________________。
(12分)如图所示转化关系,判断A、B、C、D各是什么物质,写出有关的化学方程式。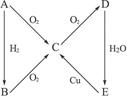
(1)当A为气体单质时,A是___________,B是___________,C是___________,D是
_____________,E是_____________。E→C化学方程式:_____________________________。
(2)当A为固体单质时,A是_________,B是__________,C是__________,D是___________,E_____________。E→C化学方程式:
_____________________________________________。
用氯气消毒的饮用水,会使水中的有机物发生氯化反应,生成有机含氯化合物,对人体有害,世界环保联盟建议推广采用高效氧化剂二氧化氯(ClO2)消毒。
(1)使用ClO2作饮用水消毒剂的优点是_____________________________。
(2)目前国外多用NaClO3与浓HCl反应制取ClO2,同时有Cl2生成,且体积为ClO2的一半,写出反应的化学方程式。__________________________________________________
(3)上述反应中产生0.1 mol Cl2,转移的电子的物质的量为_________ mol。
(4)在H2SO4酸性条件下,用Na2SO3还原NaClO3可制得ClO2,反应为:2NaClO3+Na2SO3 +H2SO4====2ClO2↑+2Na2SO4+H2O
这种方法的优点是____________________________________________________________。
在如下图的转化关系中,A、B、C为单质,其余方框内物质均为化合物,B、X、N常温下均为气体,C为黑色固体,D为白色沉淀,A、Y、Z、M、D中均含同一种元素(框图中某些生成物已略去),请填写下列空白: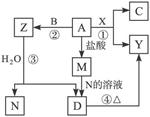
(1)完成下列化学方程式:
①_________________________________________________;
②_________________________________________________;
③_________________________________________________;
④_________________________________________________。
(2)写出下列物质的电子式:
B._________________________________________________;
X._________________________________________________;
N._________________________________________________。
(3)试拟定工业上由Y制取单质A的反应原理(用化学方程式表示)____________________,____________________。
海水占地球总储水量的97.2%。若把海水淡化和化工生产结合起来,既可以解决淡水资源缺乏的问题,又可以充分利用海洋资源。试完成下列问题:
(1)海水中含有大量的氯化钠。氯化钠中的金属元素化合价为___________价。
(2)目前国际上实用的“海水淡化”主要技术之一是蒸馏法。蒸馏法是将海水变成蒸汽,蒸汽经过冷却而得高纯度淡水,由此可判断蒸馏法是___________(填“物理变化”或“化学变化”)。
(3)工业上利用电解饱和食盐水可制得重要化工产品,反应式为:
食盐+H2O NaOH+H2+Cl2(未配平)。该反应中食盐的化学式是_____________________。利用电解所得气体制36.5%的浓盐酸100 t,最少需要消耗食盐___________t。
NaOH+H2+Cl2(未配平)。该反应中食盐的化学式是_____________________。利用电解所得气体制36.5%的浓盐酸100 t,最少需要消耗食盐___________t。
(4)近年来有人提出了一种利用氯碱工业产品及氯化钠循环治理含二氧化硫废气并回收二氧化硫的方法,该方法流程如下: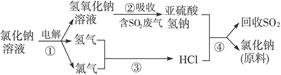
写出①③的化学反应方程式:__________________________,__________________________。
已知:①A、B、C、D四种物质均含有元素X,可能还含有元素Y或Z。元素Y、X、Z的原子序数依次递增且都不超过20。② X在A、B、C、D中的化合价分别为0、-1、+1、+5。③室温下单质A与某种常见一元强碱溶液反应,可得到B和C。④化合物D在二氧化锰催化下受热分解,可制得元素Y的单质。请完成下列问题:
(1)写出元素X、Y、Z的元素符号:X___________,Y___________,Z___________。
(2)写出A、B、C、D的化学式:A___________,B___________,C___________,D___________。
(3)写出③中反应的化学方程式:
__________________________________________________。
(4)写出④中反应的化学方程式:
___________________________________________________。