A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如下的反应关系:
⑴若A是淡黄色固体,C、D是氧化物,且C是造成酸雨的主要 物质。处理C物质可得到有价值的化学品,写出该化学品中的1种酸和1种盐的名称 、 。
⑵若B是气态氢化物,C、D是氧化物且会造成光化学烟雾污染。B与C在一定条件下反应生成的A是大气主要成分,写出该反应的化学方程式
⑶若D物质具有两性,②③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体。判断单质A的元素在周期表中的位置是___ _____。
写④反应离子方程式 。
⑷若A是应用最广泛的金属。④反应用到A,②⑤反应均用到同一种非金属单质。C的溶液用于蚀刻印刷铜电路板,写该反应的离子方程式 。
(8分)某浅绿色溶液A中加入用硝酸酸化的硝酸银酸性溶液,生成白色沉淀B和黄色溶液C,再向溶液C中加入足量的氨水生成红褐色沉淀D。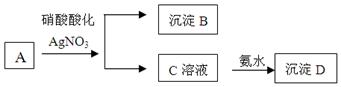
根据以上判断:
(1)A、B、C、D的化学式:A B C D
(2)写出C到D反应的离子方程式
(3)写出A和硝酸反应的化学方程式
某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的变化: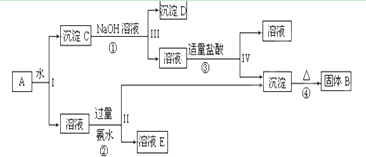
据此回答下列问题:
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是 。
(2)根据上述框图反应关系,写出下列B、C、D、E所含物质的化学式固体B ;沉淀C ;沉淀D 。
(3)写出①、②、④三个反应方程式(属于离子反应的写离子方程式)
① ;
② ;
④ 。
(4分)有一包固体粉末,由CaCO3、Na2SO4、KNO3、BaCl2、CuSO4中的三种物质组成,取样品进行如下实验:
从实验可以判断,该固体粉末中
(1)一定不含有 。
(2)写出无色气体的分子式 。
A、B、C是三种短周期元素,它们的原子序数依次增大。已知A是地壳中含量最多的元素;B元素原子的最外层只有一个电子;C元素的单质在常温下是黄绿色的气体。
(1)写出A、B的元素符号:A_________,B_________。
(2)写出C元素最高价氧化物对应水化物的化学式 。
由短周期元素组成的单质A、B、C和甲、乙、丙、丁四种化合物有下图所示的转换关系,已知C为密度最小的气体。
根据图示转化关系回答:
(1)写出下列物质的化学式:B 、丙 、丁 。
(2)组成单质A的元素在周期表中的位置是 。
(3)乙与过量CO2反应的离子反应方程式____________________________
(4)A与NaOH溶液反应的化学反应方程式____________________________
判断对错(每题1分,共5分)
1)冶炼铝时常用焦炭做还原剂。( )
2)钠的性质活泼,在空气中易发生反应,故应保存在CCl4或酒精中。 ( )
3)金属阳离子一定只具有氧化性。( )
4)碳酸氢钠在水溶液中的电离方程式为NaHCO3====Na++H++CO32-。( )
5)冰醋酸、冰水混合物、水玻璃、钢、淀粉都属于混合物( )
用“√”或“×”判断下列说法是否正确。
(1)一个D2O分子所含的中子数为8。
(2)HI、HBr、HCl、HF的稳定性依次增强。
(3)同主族元素从上到下,单质的熔点逐渐降低。
(4)常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快。
(5)从能量角度看,断开化学键要放热,形成化学键要吸热。一个化学反应是释放能量,还是吸收能量,取决于二者的相对大小。
(6)将锌片和铜片用导线连接,并平行插入稀硫酸中,由于锌片是负极,所以溶液中的H+向负极迁移。
(7)在二氧化硫与氧气的反应中,适当提高氧气浓度,可提高二氧化硫的转化率。
(8)二氯甲烷没有同分异构体,证明甲烷分子具有正四面体结构。
(9)用点燃或通入酸性高锰酸钾溶液中的方法均可以鉴别甲烷和乙烯。
(10)苯不与酸性高锰酸钾溶液、溴水发生反应,证明苯不具有类似乙烯中的双键。
判断下列说法中是否正确:(请在空格内打“√”或“×”)
①质子数相同的粒子一定属于同种元素; ( )
②电子数相同的粒子不一定是同一种元素; ( )
③一种元素只能有一种质量数; ( )
④某种元素的相对原子质量取整数,就是其质量数; ( )
⑤质子数相同,电子数也相同的粒子,不可能是一种分子和一种离子; ( )
⑥同位素的性质几乎完全相同 ( )
判断下列说法是否正确:
| A.1mol任何气体的体积都是22.4L( ) |
| B.标准状况下,1mol任何物质所占有的体积都约是22.4L( ) |
| C.标准状况下,1mol任何气体的体积都约是22.4L ( ) |
| D.标准状况下,1L H2和1L水的物质的量相同 ( ) |
E.若1mol气体的体积约为22.4L,则它一定处于标准状况下. ( )
(1)有机物A只含C、H、O三种元素,其相对分子质量为62,A经催化氧化生成D,D经催化氧化生成E,A与E在一定条件下反应可生成一种环状化合物F。
则A的分子式为 ,结构简式为 ;
A与E反应生成F的化学方程式为 。
(2)对有机物B的组成、结构、性质进行观察、分析,得实验结果如下:
①B为无色晶体,微溶于水,易溶于Na2CO3溶液;
②完全燃烧166mg有机物B,得到352mgCO2和54mgH2O;
③核磁共振氢谱显示B分子中只有2种不同结构位置的氢原子;
④B的相对分子质量在100~200之间。
B的分子式为 ,结构简式为 。
(3)A与B在一定条件下反应可生成一种常见合成纤维,该高分子化合物的结构简式为 。
(4)B的一种同分异构体(与B具有相同的官能团),在一定条件下可发生分子内脱水生成一种含有五元环和六元环的有机物G,G的结构简式为 。
(5)E可将酸性高锰酸钾溶液还原,所得还原产物为Mn2+,该反应的离子方程式为
。
某有机物X(C12H13O6Br)分子中含有多种官能团,其结构简式为
 (其中I、II为未知部分的结构)
(其中I、II为未知部分的结构)
为推测X的分子结构,进行如图的转化:

已知向E的水溶液中滴入FeCl3溶液发生显色反应;M(C2H2O4)能使蓝墨水褪色;G、M都能与NaHCO3溶液反应。请回答:
(1)M的结构简式为 ;G分子所含官能团的名称是 ;
(2)E可以发生的反应有(选填序号) ;
①加成反应 ②消去反应 ③氧化反应 ④取代反应
(3)G在一定条件下发生反应生成分子组成为C4H4O4的有机物(该有机物可使溴的四氯化碳溶液褪色),写出G发生此反应的化学方程式
;
(4)已知在X分子结构中,I结构含有能与FeCl3溶液发生显色反应的官能团,且E分子中苯环上的一氯代物只有一种,则X的结构简式是 ;
(5)F与G互为同分异构体,F的分子中只含有羧基、羟基和醛基三种官能团,且同一个碳原子上不能同时连有两个羟基。则F的分子结构可能为 。
X、Y、Z、M是元素周期表中前20号元素,其原子序数依次增大,且X、Y、Z相邻。X的核电荷数是Y的核外电子数的一半,Y与M可形成化合物M2Y。用微粒符号完成下列问题:
(1)Y、Z两种元素的最高价氧化物的水化物酸性 强于 。
(2)M、Z、Y形成的简单离子的半径的大小 。
(3)M2X2固体中阴、阳离子个数比____________, 其电子式为 .该物质中含有化学键的类型有 和 .
(4)将Z的单质通入YX2的水溶液中发生反应的离子方程式为 。
下列是芳香族化合物A、B、C、D、E的转化关系,其中A、E分子式分别是C9H8O和C9H8O2,E分子中除苯环外还含有一个六元环,且E中不含甲基。根据下列转化关系回答问题:
(1)写出A分子中所含官能团的名称________________________________。
(2)完成方程式,并分别写出反应类型
A→B___________________________________________反应类型__________________。
B→C___________________________________________反应类型__________________。
(3)写出E的结构简式______________________________。
(4)要中和16.6gD,需要2mol/LNaOH溶液的体积为_________mL。
(5)符合下列条件的D的同分异构体共有_________种,写出其中任意一种同分异构体的结构简式______________________________________。
①苯环上有两个取代基 ②能与FeCl3溶液发生显色反应 ③能发生水解反应和银镜反应