取质量为4.6g的纯净的金属钠平均分成两等份,做如下实验:
(1)第一块直接投入适量的水中,充分反应后得到了气体A和200mL溶液(甲);
(2)另一块在干燥氧气中受热后转化成3.5g固体(经检验固体中不含金属钠的单质),再将所得固体全部投入适量的水中,充分反应后得到气体B和200mL溶液(乙)。求:
①同温同压下,气体A和气体B的密度之比为 ;
②溶液甲的物质的量浓度= ;
③溶液的物质的量浓度:甲 乙(填 “>”、“=”、“<”、“无法确定”);
④3.5g固体所含成分是 。
| A.只含Na2O | B.只含Na2O2 |
| C.既含Na2O又含Na2O2 | D.无法确定 |
以丙烷为燃料制作新型燃料电池,电池的正极通入O2和CO2,负极通入丙烷,电解质是熔融碳酸盐,电池总反应方程式为:C3H8 +5O2 = 3CO2+ 4H2O。
(1)已知: 2C3H8(g) + 7O2(g) =" 6CO(g)" + 8H2O(l) ∆H1
C(s) + O2(g) = CO2 (g) ∆H2
2C(s) + O2(g) = 2CO(g) ∆H3
则C3H8(g) +5O2((g) = 3CO2(g) + 4H2O(l) ∆H= (用∆H1、∆H2、∆H3表示)
(2)写出该电池正极的电极反应式: ,电池工作时CO32-移向 ;用该电池电解1000 mL 1mol/L的AgNO3溶液,此电解池的反应方程式为 ;当电池消耗0.005 mol C3H8时,被电解溶液的pH为 (溶液体积变化忽略不计)。
氯化铜是一种广泛用于生产颜料、用木材防腐剂的化工产品。某研究性学习小组用粗铜(含杂质Fe)按下述流程制备氯化铜晶体。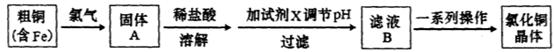
(1)固体A用稀盐酸溶解而不用水溶解的原因是________。
(2)加试剂X用于调节pH以除去杂质,X可选用下列试剂中的____(填序号)。
| A.NaOH | B.NH3.H2O | C.CuO | D.Cu(OH)2E. CuSO4 |
(3)滤液B经一系列操作可得氯化铜晶体,操作的程序依次为_________ 、_________、 过滤、自然干燥。
(4)实验室采用如下图所示装置,可使粗铜与Cl2反应转化为固体A(部分加热仪器和夹持装置已略去)。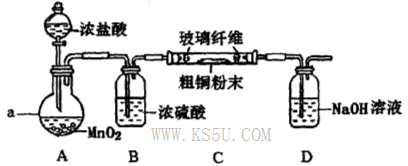
①该装置中仪器a的名称是____,其中发生反应的离子方程式是____________。
②有同学认为应在浓硫酸洗气瓶前增加吸收HCI的装置,你认为是否必要?____________(填“是”或“否”)。
③该装置存在一定的安全隐患,消除该安全隐患的措施是_______________________。
硝基苯甲酸乙酯在OH-存在下发生水解反应:
O2NC6H4COOC2H5+OH- O2NC6H4COO-+C2H5OH
O2NC6H4COO-+C2H5OH
两种反应物的初始浓度均为0.050 mol·L-1,15 ℃时测得O2NC6H4COOC2H5的浓度c随时间变化的数据如表所示。回答下列问题:
| t/s |
0 |
120 |
180 |
240 |
330 |
530 |
600 |
700 |
800 |
| c/mol·L-1 |
0 |
0.036 |
0.030 |
0.026 |
0.022 |
0.017 |
0.016 |
0.015 |
0.015 |
(1)计算该反应在120~180 s间的平均反应速率_________;比较120~180 s与180~240 s 区间的平均反应速率的大小,前者_________后者(填>,<或=),理由是____________________。
(2)计算15 ℃时该反应的平衡常数_____________。
(3)为提高O2NC6H4COOC2H5的平衡转化率,除可适当控制反应温度外,还可采取的措施有________。
A.加入O2NC6H4COOC2H5 B.增加OH-的浓度
C.移去产物 D.加入适当的催化剂
某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,实验小组利用A制备Al(OH)3的操作流程如下:
据此回答下列问题:
(1)I、II、III、IV四步中分离溶液和沉淀所采取的操作名称是 ,该实验操作所用到的玻璃仪器有 。
(2)根据上述流程,写出D、E所含物质的化学式:
沉淀D ;溶液E 、 。
(3)写出②、③反应的离子方程式:
② ;③ ;
在100 mL MgCl2和AlCl3的混和溶液中,逐滴加入1 mol/L NaOH溶液直至过量,经测定,加入NaOH的物质的量和所得沉淀的物质的量的关系如下图所示,
则:
(1)图中C点表示加入 mLNaOH,AB段发生的离子反应方程式 。
(2)c(MgCl2)= mol·L—1
(3)图中线段OA︰AB= 。
氢氧化钙俗称熟石灰,在生产和生活中有广泛的用途.
(1)熟石灰可由生石灰溶于水制得,反应的化学方程式是: .测量其溶液的pH时,可以 ,再用标准比色卡比较试纸显示的颜色,读取该溶液的pH.
(2)用石灰浆粉刷墙壁,干燥后墙面变硬,反应的化学方程式是: .
(3)用熟石灰来改良酸性土壤,反应的化学方程式是: (以土壤中含有硫酸为例).
(4)用熟石灰粉与草木灰(主要成分是K2CO3)按一定比例混合可制得高效环保农药“黑白粉”.使用时,选择有露水的早晨,把“黑白粉”撒在植物茎叶上,可消除忌碱虫体.
①“黑白粉”比熟石灰更高效,是由于生成了碱性更强的KOH,反应的化学方程式是 .
②“黑白粉”还可提供植物必需的营养素是 (填元素符号).
某大理石含有的主要杂质是氧化铁,以下是提纯该大理石的实验步骤:
(1)溶解大理石时,用硝酸而不用硫酸的原理是: 。
(2)操作Ⅰ的目的是: ,该反应的离子方程式是: 。
(3)写出加入(NH4)2CO3所发生反应的离子方程式: ,
滤液A的一种用途是 。
化学是在原子、分子的水平上研究物质及其变化规律.请回答下列关于水与过氧化氢(H2O2)的问题:
(1)H2O2中氧元素的化合价为 .
(2)1个过氧化氢分子中含有 个H, 个O.
(3)写出下列反应的化学方程式:
①水通电后分解: ;
②过氧化氢分解: .
(4)下列关于它们的说法正确的是 (填编号).
①水、过氧化氢组成元素相同,化学性质也相同
②过氧化氢溶于水得到的物质仍然属于纯净物
③水是生物体内重要的组成物质
④硬水可以使肥皂水产生更多的泡沫.
⑴按要求写出下列反应的离子方程式
①氢氧化铜溶于盐酸
②碳酸钠溶液中和足量的盐酸溶液混合
(2)现有以下物质:①NaCl晶体 ②液态HCl ③CaCO3固体 ④熔融KCl ⑤蔗糖⑥铜⑦CO2⑧H2SO4⑨KOH固体 ⑩水⑾盐酸⑿CH3COOH ⒀酒精(填序号)
①以上物质中能导电的是_________________________________。
②以上物质中属于电解质的是_____________________________。
③以上物质中属于非电解质的是___________________________。
电化学原理在化学工业中有广泛的应用.请根据如图回答问题:
(1)装置Ⅰ中的X电极的名称是 ,Y电极的电极反应式为 ,工作一段时间后,电解液的PH将 (填“增大”、“减小”、“不变”).
(2)若装置Ⅱ中a、b均为Pt电极,W为饱和食盐水(滴有几滴酚酞),实验开始后,观察到b电极周围溶液变红色,其原因是(用电极反应式表示) ,a电极上有气泡产生,该气体的电子式为 .
(3)若利用装置Ⅱ进行铜的精炼,则a电极的材料为 ,工作一段时间后装置Ⅱ电解液中c(Cu2+)将 (填“增大”、“减小”、“不变”).
(4)若装置Ⅱ中a为Ag棒,b为铜棒,W为AgNO3溶液,工作一段时间后发现铜棒增重2.1.6g,则流经电路的电子的物质的量为 .
某无色透明溶液中可能大量存在Ag+,Mg2+,Cu2+中的几种离子。






(1)不做任何实验就可以肯定原溶液中不存在的离子是_________。
(2)取少量原溶液加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,白色沉淀不消失,说明原溶液中肯定有的离子是_______,有关的离子反应式为_______。
(3)取(2)的滤液加入过量NaOH溶液,出现白色沉淀,说明原溶液中肯定存在的离子有_____。
(4)原溶液中可能大量存在的阴离子是下列A-D中的(填序号)_________。
| A.Cl- | B.NO3- | C.CO32- | D.OH- |
国际化学年的中国宣传口号是“化学-----我们的生活,我们的未来”。学习化学应该明白“从生活中来,到生活中去”道理。请填空:
①若金属钠等活泼金属着火时,应该用 来灭火。
②经火焰灼烧,焰色反应为浅紫色(透过蓝色钴玻璃)的元素是 。
③使用漂白粉Ca(ClO)2漂白衣物原理的化学方程式是 。
④在自然界中,能实现氮的固定的化学方程式是 。
⑤胃舒平(含有氢氧化铝)治疗胃酸(盐酸)过多的离子反应方程式: 。
⑥过氧化钠在太空及潜水艇中作为供氧剂的两个化学方程式是 、 。
⑦明矾(KAl(SO4)2·12H2O)是具有净水作用的复盐,请你写出其在水中的电离方程式 。
红砖是用粘土高温烧结而成,因其颜色呈红色或棕红色而得名,常用作建筑材料
(1)根据红砖的颜色、猜测其可能含有的成份是 (写化学式)
(2)为了检验猜测是否正确,请根据以下设计的实验方案,简要地完成各步操作过程以及最后的实验分析和结论,涉及化学反应的写出化学方程式(实验用品任取,不必写实验装置中的仪器安装)
实验步骤:① 用铁锤敲碎红砖,取小块磨成粉末。
② 将红砖粉末放入烧杯,加入___________
③ 将混合液倒入过滤器___________
④ 在滤液中滴入___________
实验分析及结论: 。
阅读下面科普短文。
氮氧化物(NOx)种类很多,造成大气污染的主要是一氧化氮(NO)和二氧化氮(NO2)。NO通常为无色气体。熔点为-163.6℃,沸点为-151.5℃。它的性质不稳定,在空气中易氧化成NO2。NO结合血红蛋白的能力比CO还强,更容易造成人体缺氧。NO分子作为一种传递神经信息的信使分子,在使血管扩张、增强免疫力、记忆力等方面有着极其重要的作用。NO2通常为红棕色有刺激性气味的气体,溶于水生成硝酸(HNO3)和NO,工业上利用这一原理制取HNO3。NO2能使多种织物褪色,损坏多种织物和尼龙制品,对金属和非金属材料也有腐蚀作用。城市大气中的NOx大多来自于化石燃料的燃烧。经测算,天然气、煤和石油燃烧产生NOx的量分别为:6.35 kg/t、8~9 kg/t、9.1~12.3 kg/t。以汽油、柴油为燃料的汽车,尾气中NOx的浓度相当高。在非采暖期,北京市一半以上的NOx来自机动车排放。
依据文章内容,回答下列问题:(各答1条即可)
(1)分别说明NO的“利与弊”:“利”是___________________,“弊”是
___________________。
(2)NO2溶于水发生反应的化学方程式是_________________________________。
(3)与煤和石油相比,天然气是比较清洁的燃料,结合数据解释原因:______________________。
(4)减少NOx污染的有效措施是________________________________________________。