英国国家海洋学中心于2009年8月14日发布新闻公报说,中心的研究人员及其同行利用声呐等手段探测到北极海洋中存在大量甲烷气泡,证实了全球变暖会使海底释放大量甲烷的说法。研究人员认为,这些甲烷可能会反过来加剧全球变暖。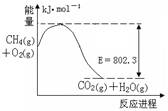
(1)右图是1molCH4和O2完全反应生成CO2气体与水蒸气过程中能量变化示意图,又已知 H2O(l)=H2O(g) △H=44.0kJ·mol-1,请写出1molCH4和O2完全反应生成CO2气体与液态水的热化学方程式 。
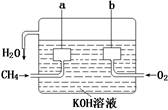
(2)美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的电池,氢气虽然使用方便,却受到价格和来源的限制。常用的燃料往往是某些碳氢化合物,如甲烷(天然气)、汽油等。电池的构造如图所示:两个电极均由多孔碳制成,通入的气体由孔隙中流出,并从电极表面放出。
①请写出甲烷燃料电池中a极的电极反应式为 。
②此时电池内的总反应方程式为 。
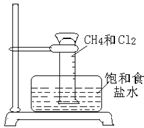
(3)某课外活动小组利用右图所示装置探究甲烷于氯气的反应。根据题意,回答下列问题:
①CH4与Cl2发生反应的条件是 ;若用日光直射,可能会引起 。
②实验中可观察的实验现象有:量筒内壁出现油状液滴,饱和食盐水中有少量固体析出, , 等。
③用饱和食盐水而不用谁的原因是 。
④实验中生成的油状液滴中的氯仿可作局部麻醉剂,常因保存不慎而被空气氧化,产生剧毒气体——光气,反应化学方程式为2CHCl3+O2→2COCl2+2HCl,上述反应 (填选项符号,下同)
A.属于取代反应 B.不属于取代反应
为防止事故发生,在使用前检验氯仿是否变质可选用的试剂是
A.氢氧化钠溶液 B.硝酸银溶液 C.稀盐酸
D.水 E.湿润的蓝色石蕊试纸 F.湿润的无色酚酞试纸
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:
(1)右图是N2和H2反应生成2molNH3过程中能量变化示意图,请计算每生成1molNH3放出热量为 。
(2)工业合成氨气需要的反应条件非常高且产量低,而一些科学家采用高质子导电性的SCY陶瓷(能传递H+)实现氨的电化学合成,从而大大提高了氮气和氢气的转化率。电化学合成氨过程的总反应式为N2+3H2 2NH3,则在电化学合成氨的过程中,阳极反应式为 ,阴极反应式为 。
2NH3,则在电化学合成氨的过程中,阳极反应式为 ,阴极反应式为 。
(3)在固定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g)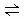 2NH3(g) △H<0,其化学平衡常数K与t的关系如下表:
2NH3(g) △H<0,其化学平衡常数K与t的关系如下表:
| t/K |
298 |
398 |
498 |
…… |
| K/(mol·L-1)-2 |
4.1×106 |
K1 |
K2 |
…… |
请完成下列问题:
①试确定K1的相对大小,K1 4.1×106(填写“>”“=”或“<”)
②下列各项能作为判断该反应达到化学平衡状态的依据的是 (填序号字母)。
A.容器内N2、H2、NH3的浓度之比为1∶3∶2
B.2v(NH3)(正) =3v(H2)(逆)
C.容器内压强保持不变
D.混合气体的密度保持不变
(4)①NH4Cl溶液呈酸性,这是由于NH4+水解的缘故。则NH4Cl溶于重水(D2O)生成一水合氨和水合氢离子的化学式是 。
②某氨水的pH=x,某盐酸的pH=y,x+y=14,且x>11,将上述氨水和盐酸等体积混合后,所得溶液中各种离子的浓度由大到小的顺序为( )
A.[Cl-]>[NH4+]>[H+]>[OH-]
B.[NH4+]>[Cl-]>[OH-]>[H+]
C.[Cl-]>[NH4+]>[OH-]>[H+]
D.[NH4+]>[Cl-]>[H+]>[OH-]
在常温下,一氯甲烷是无色气体,密度为0.9159g/cm3,熔点-97.73℃,沸点为-24.2℃;18℃时它在水中的溶解度为280mL/L水,它与乙醚、丙酮或苯互溶,能溶于乙醇。在实验室可用图所示装置制造一氯甲烷。
制备装置的分液漏斗和烧瓶中分别盛有甲醇和浓盐酸,试填写下列空白.
(1)制备一氯甲烷的化学方程式为 ;其反应类型是
(2)装置b的作用是_ ___
(3)检验气体产物CH3Cl的方法是:在e的逸出口点燃CH3Cl气体,火焰呈蓝绿色(与其他烃燃烧现象有明显区别),CH3Cl燃烧的化学方程式为__ __
(4)实验中实际按甲醇和浓盐酸1∶2(物质的量之比)进行反应的理由是___ _
(5)某学生在关闭活塞X的情况下做此实验时,发现收集到一定体积的气体产物所消耗的甲醇—浓盐酸的混合液的量比正常情况下多(装置的气密性没有问题),其原因是____
(6)实验结束时,d中收集到的液体中含有_
碳正离子[例如CH3+、CH5+、(CH3)3C+]是有机反应中重要的中间体。欧拉(G.Olah)因在此领域研究中的卓越成就而荣获1994年诺贝尔化学奖。碳正离子CH5+可以通过CH4在“超强酸”中再获得一个H+而得到,而CH5+失去H2可得CH3+。
(1)CH3+中4个原于是共平面的,三个键角相等,键角应是_______(填角度)
(2)(CH3)2CH+在NaOH的水溶液中反应将生成电中性的有机分子,其结构简式是________
(3)(CH3)3C+去掉H+后将生成电中性的有机分子,其结构简式是________
有机物A,俗名水杨酸,其结构为 。
。
(1)将A跟_____(填物质序号)的溶液反应可得到一种钠盐(其化学式为C7H5O3Na)
| A.NaOH | B.Na2S | C.NaHCO3 | D.NaClO |
(2)水杨酸的同分异构体中,属于酚类,同时还属于酯类的化合物的结构简式分别为_____
(3)水杨酸的同分异构体中,属于酚类,但不属于酯类,也不属于羧酸类的化合物中必定含有_____基(填写除了羟基以外的官能团名称)
近年来,乳酸CH3CH(OH)COOH成为人们的研究热点之一。乳酸可以用化学方法合成,也可以由淀粉通过生物发酵法制备。乳酸有许多用途,其中利用乳酸的聚合而合成的高分子材料,具有很好的生物兼容性,它无论在哺乳动物体内或自然环境中,最终都能够降解成为二氧化碳和水。请回答下列有关问题:
(1)乳酸在发生下列变化时所用的试剂是① ②

(2)乳酸可以跟精制的铁粉反应制备一种补铁的药物,反应的化学方程式为:
2CH3CH (OH) COOH+Fe→[CH3CH(OH)COO]2Fe+H2↑
该反应中氧化剂是 ,还原产物是
(3)由乳酸可以制取  ,请写出设计合成实验时所涉及的有机反应类型 。
,请写出设计合成实验时所涉及的有机反应类型 。
(4)聚乙烯、聚苯乙烯材料因难分解而给人类生存环境带来严重的“白色污染”,德国Danone公司开发了聚乳酸材料  ,它是由乳酸通过 反应制取的。聚乳酸包装材料能够在60天自行降解,降解过程分为两个阶段,首先在乳酸菌的作用下水解生成单体,然后乳酸单体在细菌的作用下与氧气反应转化为二氧化碳和水,请写出上述两个反应的化学方程式 ,
,它是由乳酸通过 反应制取的。聚乳酸包装材料能够在60天自行降解,降解过程分为两个阶段,首先在乳酸菌的作用下水解生成单体,然后乳酸单体在细菌的作用下与氧气反应转化为二氧化碳和水,请写出上述两个反应的化学方程式 ,
(5)若碳原子以单键与四个不同的原子或原子团相结合,则称该碳原子为“手性碳原子”,含有手性碳原子的分子称为“手性分子”,手性分子往往具有一定生物活性。乳酸分子是手性分子,乳酸[③CH3②CH(OH)①COOH]的手性碳原子是 号碳原子。
(6)乳酸的某种同分异构体具有下列性质:能发生银镜反应;1 mol该物质跟足量金属钠发生缓慢反应,生成2g氢气;该分子为手性分子。写出该物质的结构简式
(1)具有支链的化合物A的分子式为C4H9O2,A可以使Br2的四氯化碳溶液褪色。1 mol A和1 mol NaHCO3能完全反应,则A的结构简式是 。写出与A具有相同官能团的A的所有同分异构体的结构简式
(2)化合物B含有C、H、O三种元素,相对分子质量为60,其中碳的质量分数为60%,氢的质量分数为13.3%。B在催化剂Cu的作用下被氧气氧化成C,C能发生银镜反应,则B的结构简式是
(3)D在NaOH水溶液中加热反应,可生成A的钠盐和B,相应反应的化学方程式是
某种甜味剂A的甜度是蔗糖的200倍,由于它热值低、口感好、副作用小,已在90多个国家广泛使用。其结构简式如下: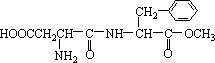
已知:①在一定条件下,羧酸酯或羧酸与含—NH2的化合物反应可以生成酰胺,如:
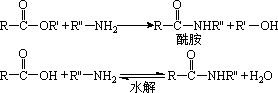
②酯比酰胺容易水解。
请填写下列空白:
(1)在稀酸条件下加热,化合物A首先生成的水解产物是_________和___________
(2)在较浓酸和长时间加热条件下,化合物A可以水解生成:_________、_________和___________
(3)化合物A分子内的官能团之间也可以发生反应,再生成一个酰胺键,产物是甲醇和________(填写结构简式,该分子中除苯环以外,还含有一个6原子组成的环。)
某温度下,在2 L的密闭容器中,X、Y、Z三种物质随时间变化的曲线如图所示。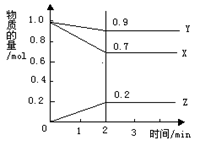
由图中数据分析:该反应的化学方程式为: 。反应开始至2 min ,Z的平均反应速率为 。
将除去氧化膜的镁条投入到盛有稀盐酸的试管中,产生H2的速率变化情况如下图所示。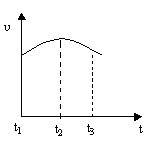
图中t1~t2速率变化的主要原因是______ ____ _,t2~t3速率变化的主要原因是 _。
已知单质铁和硫粉反应时需用酒精灯加热,反应方能开始,但在铁粉和硫粉开始反应后,把酒精灯撤去反应仍可进行完全。则此反应为 反应(填“放热”、“吸热”)。原因是 。
四种元素、
、
、
位于元素周期表的前四周期,已知它们的核电荷数依次增加,且核电荷数之和为51;
原子的
层
轨道中有2个电子;
与
原子的价层电子数相同;
原子的
层电子数与最外层电子数之比为4:1,其
轨道中的电子数与最外层电子数之比为5:1。
(1)、
可分别与
形成只含一个中心原子的共价化合物
、
,它们的分子式分别是、; 杂化轨道分别是、;
分子的立体结构是。
(2)的最高价氧化物和
的最高价氧化物的晶体类型分别是晶体、晶体:
(3)的氧化物与
的氧化物中,分子极性较小的是(填分子式);
(4)与
比较,电负性较大的, 其+2价离子的核外电子排布式是
下列实验操作或事故处理中,不正确的做法是
| A.利用气球或球胆将有毒气体收集后,另作处理,避免其逸散到空气中,污染环境。 |
| B.在粗盐的提纯实验中,溶解、过滤、蒸发都用到了玻璃棒 |
| C.酸、碱溅在眼中,立即用水反复冲洗,并不断眨眼和揉眼 |
| D.配制FeCl3溶液时,将FeCl3固体溶于较浓盐酸中,然后再用水稀释到所需的浓度 |
E.不慎将浓硫酸沾在皮肤上,立即用NaOH溶液冲洗
F.汞洒落地面,应立即撒上一层硫磺粉
G.银镜反应实验后附有银的试管,可用氨水清洗
H.为了测定某溶液的pH,将用蒸馏水润湿的pH试纸浸入到待测溶液中,过一会取出,与标准比色卡进行对比
I.误服重金属盐,可服用大量的牛奶、蛋清或豆浆解毒