固定和利用CO2能有效地利用资源,并减少空气中的温室气体。工业上有一种用CO2来生产甲醇燃料的方法:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=-49.0 kJ·mol-1
CH3OH(g)+H2O(g) △H=-49.0 kJ·mol-1
某科学实验将6molCO2和8molH2充入2L的密闭容器中,测得H2的物质的量随时间变化如下图所示(实线)。
(1)a点正反应速率___________(填大于、等于或小于)逆反应速率。
(2)下列时间段平均反应速率最大的是__________,最小的是______。
| A.0~1min | B.1~3min |
| C.3~8min | D.8~11min |
(3)求平衡时氢气的转化率和该条件下反应的平衡常数K。(写出计算过程)
(4)仅改变某一实验条件再进行两次实验,测得H2的物质的量随时间变化如图中虚线所示,曲线I对应的实验条件改变是___________,曲线II对应的实验条件改变是___________。

(1)近年来,我国储氢纳米碳管研究取得重大进展,用电弧法合成的碳纳米管中常伴有大量碳纳米颗粒(杂质),这种碳纳米颗粒可用氧化气化法提纯,其反应化学方程式为:
C+ K2Cr2O7+ H2SO4 ═ CO2↑+ K2SO4+ Cr2(SO4)3+ H2O
请完成并配平上述化学方程式.其中氧化剂是 ,氧化产物是
(2)甲醇是一种新型燃料,甲醇燃料电池即将从实验室走向工业化生产.工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:
CO(g)+2H2(g)⇌CH3OH(g) △H1=﹣116kJ•mol﹣1
①已知:2CO(g)+O2(g)=2CO2(g) △H2=﹣566kJ•mol﹣1
2H2(g)+O2(g)=2H2O(g) △H3=﹣484kJ•mol﹣1
则表示1mol气态甲醇完全燃烧生成CO2和水蒸气时的热化学方程式为 ;
②在容积为1L的恒容容器中,分别研究在230℃、250℃、270℃三种温度下合成甲醇的规律.如图是上述三种温度下不同的H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系.请回答:

A)在上述三种温度中,曲线Z对应的温度是
B)利用图中a点对应的数据,计算出曲线Z在对应温度下CO(g)+2H2(g)⇌CH3OH(g)的平衡常数K= .(写明单位)
③在某温度下,将一定量的CO和H2投入10L的密闭容器中,5min时达到平衡,各物质的物质的浓度(mol•L﹣1)变化如下表所示:
| |
0min |
5min |
10min |
| CO |
0.1 |
|
0.05 |
| H2 |
0.2 |
|
0.2 |
| CH3OH |
0 |
0.04 |
0.05 |
若5min~10min只改变了某一条件,所改变的条件是 ;且该条件所改变的量是 .
I.常温下,向25mL 0.1mol/L MOH溶液中逐滴加入0.2mol/L HA溶液,曲线如图所示(体积变化忽略不计).回答下列问题:

(1)写出MOH的电离方程式:__________________
(2)MOH与HA恰好完全反应时,溶液呈________性(填“酸”、“碱”或“中”),理由是(用离子方程式表示):________________________________________________。
(3)D点时,溶液中c(A﹣)+c(HA)__________2c(M+)(填“>”、“<”或“=”).
II.室温下,几种物质的溶度积常数见下表:
| 物质 |
Cu(OH)2 |
Fe(OH)3 |
CuI |
| Ksp |
2.2×10-20 |
2.6×10-39 |
1.3×10-12 |
(1)室温下,某酸性CuCl2溶液中含少量的FeCl3,为得纯净CuCl2溶液,宜加入__________调至溶液pH=4,使Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=__________________
(2)某学习小组用“间接碘量法”测定含有CuCl2•2H2O晶体的试样(杂质不与I―发生氧化还原反应)的纯度,过程如下:取试样溶于水,加入过量KI固体,充分反应,有白色沉淀(CuI)产生。用0.1000 mol/L Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液V mL。(已知:I2+2S2O32- S4O62-+2I―。)
S4O62-+2I―。)
①CuCl2溶液与KI反应的离子方程式为______________________________。
②可选用________作滴定指示剂,滴定终点的现象是:滴入最后一滴Na2S2O3,________________。
消除氮氧化物污染有多种方法。
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)ΔH=-574kJ·mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)ΔH=-1160kJ·mol-1
③H2O(g)=H2O(l)ΔH=-44.0kJ·mol-1
写出CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(l)的热化学方程式__________
(2)用活性炭还原法处理氮氧化物。有关反应为:C(s)+2NO(g) N2(g)+CO2(g)某研究小组向恒容密闭容器加入一定量的活性炭和NO,恒温条件下反应,反应进行到不同时间测得各物质的浓度如下
N2(g)+CO2(g)某研究小组向恒容密闭容器加入一定量的活性炭和NO,恒温条件下反应,反应进行到不同时间测得各物质的浓度如下
| 浓度/mol·L-1 时间/min |
NO |
N2 |
CO2 |
| 0 |
0.100 |
0 |
0 |
| 10 |
0.058 |
0.021 |
0.021 |
| 20 |
0.040 |
0.030 |
0.030 |
| 30 |
0.040 |
0.030 |
0.030 |
| 40 |
0.032 |
0.034 |
0.017 |
| 50 |
0.032 |
0.034 |
0.017 |
①不能作为判断反应达到化学平衡状态的依据是___ ____
A.容器内CO2的浓度保持不变 B.v正(N2)="2" v正(NO) C.容器内压强保持不变
D.混合气体的密度保持不变 E.混合气体的平均相对分子质量保持不变
②计算该温度下该反应的平衡常数为 (保留两位小数);
③在30 min,改变某一条件,反应重新达到平衡,则改变的条件是____ _ _ ___。
(3) 甲烷燃料电池可以提升能量利用率,下图是利用甲烷燃料电池电解50mL2mol/L的氯化铜溶液的装置示意图:

请回答:
①甲烷燃料电池的负极反应式是
②当A中消耗0.15mol氧气时,B中 (用a或b 表示)极增重 g.
已知下表为25℃时某些弱酸的电离平衡常数;下图表示常温时,稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化。

(1)图像中,曲线Ⅰ表示的酸是____(填化学式);
(2)a、b、c三点中,水的电离程度由大到小的顺序是___________(用编号表示)。
(3)25℃时,NaClO溶液的水解平衡常数Kh=_______________。
(4)25℃时,NaHCO3溶液存在水解平衡,写出其水解的离子方程式
(5)0.1mol/L Na2CO3溶液中c(OH-)—c(H+)=_________(用含c(HCO3-)、c(H2CO3)的关系式表示)。
(1)将0.2mol/L HA 溶液与 0.1mol/L NaOH溶液等体积混合,测得混合溶液中c(Na+)>c(A−),则(用“>”、“<”或“=”填写下列空白):①混合溶液中c(A−)______c(HA);②混合溶液中c(HA)+c(A−)______0.1mol⋅L−1;
(2)常温时,取0.1mol•L-1 HX溶液与0.1mol•L-1 NaOH溶液等体积混合(混合后溶液体积的变化不计),测得混合溶液的pH=8,试回答以下问题:
①混合溶液中由水电离出的c(OH-)与0.1mol•L-1 NaOH溶液中由水电离出的c(OH-)之比为______.
②已知NH4X溶液是中性,又知将HX溶液加入到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的pH______7(选填“>”、“<”或“=”).
氨气是一种重要工业原料,在工农业生产中具有重要的应用.
(1)已知:N2(g)+O2(g)═2NO(g);△H=+180.5kJ•mol-1
4NH3(g)+5O2(g)═4NO(g)+6H2O(g);△H=-905kJ•mol-1
2H2(g)+O2(g)═2H2O(g);△H=-483.6kJ•mol-1
则N2(g)+3H2(g)═2NH3(g);△H=______
(2)工业合成氨气的反应为N2(g)+3H2(g) 2NH3(g);在一定温度下,将一定量的N2和H2通入到初始体积为1L的密闭容器中达到平衡后,单独改变下列条件,能使平衡向正反应方向移动且平衡常数不变的是______.(填序号)
2NH3(g);在一定温度下,将一定量的N2和H2通入到初始体积为1L的密闭容器中达到平衡后,单独改变下列条件,能使平衡向正反应方向移动且平衡常数不变的是______.(填序号)
①增大压强 ②增大反应物的浓度 ③使用催化剂 ④降低温度
(3)将相同体积、pH之和为14的氨水和盐酸混合后,溶液中离子浓度由大到小的顺序为______.
(4)氢气是合成氨的原料之一,下图是以SO2、I2、H2O为原料,利用核能使水分解制氢气的一种流程。

反应X的化学方程式为SO2+I2+2H2O=2HI+H2SO4该流程中循环使用的原料除了SO2外,还有 。从理论上讲,该流程中,1mol原料水制得 molH2。
(1)已知在氨水中存在下列平衡: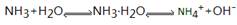
①向氨水中加入NaOH固体时,平衡向 (填“正反应”“逆反应”或“不”)移动,OH-的浓度 (填“减小”“增大”或“不变”)
②向氨水中加入浓盐酸,平衡向 (填“正反应”“逆反应”或“不”)移动,此时溶液中浓度增大的离子有NH4+(Cl-除外)和
(2)已知某溶液中只存在OH−、H+、NH4+、Cl−四种离子,某同学推测其离子浓度大小顺序有以下几种:
A.c(Cl−)>c(NH4+)>c(H+)>c(OH−) B.c(Cl−)>c(NH4+)>c(OH−)>c(H+)
C.c(NH4+)>c(Cl−)>c(OH−)>c(H+) D.c(Cl−)>c(H+)>c(NH4+)>c(OH−)
①上述关系一定不正确的是______(填序号).
②若溶液中只有一种溶质,则该溶液中离子浓度的大小关系为______(填序号).
③若四种离子浓度关系有c(NH4+)=c(Cl−),则该溶液显______(填“酸性”、“碱性”或“中性”).
(3)常温下,有A、B、C、D四种无色溶液,它们分别是CH3COONa溶液、NH4Cl溶液、盐酸和NaNO3溶液中的一种。已知A、B的水溶液中水的电离程度相同,A、C溶液的pH相同。
①则:B是______溶液,C是______.
②常温下若B溶液中c(OH-)与C溶液中的c(H+)相同,B溶液的pH用pHb表示,C溶液的pH用pHc表示.则pHb+pHc= (填某个数)
答案:(1)①逆反应 增大 ②正反应 H+ (2)促进 不变
(3)①B ②A ③中性 (4)①CH3COONa 盐酸 ②14
亚磷酸(H3PO3)与足量NaOH溶液反应生成Na2HPO3
(1) 亚磷酸是________元酸。
(2)PCl3水解可制取亚磷酸,反应的化学方程式是______________;
(3)H3PO3溶液中存在电离平衡:H3PO3 H++H2PO3-
H++H2PO3-
①某温度下,0.10mol•L-1的 H3PO3溶液 pH=1.6,即溶液中 c(H+)=2.5×10-2mol•L-1.求该温度下上述电离平衡的平衡常数K= ________;(只考虑H3PO3的第一步电离,结果保留两位有效数字)
②根据H3PO3的性质可推测Na2HPO3稀溶液的pH ______7 (填“>”、“=”或“<”);
(4)亚磷酸具有强还原性,可使碘水褪色.该反应的化学方程式为______________。
现有浓度均为0.1mol•L-1的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸铵、⑦硫酸氢铵、⑧氨水,请回答下列问题:
(1)①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号)_________;
(2)④、⑤、⑥、⑦、⑧四种溶液中NH4+浓度由大到小的顺序是(填序号)_________;
(3)将③和④等体积混合后,混合液中各离子浓度由大到小的顺序是_________;
(4)已知t℃时,Kw=1×10-13,则t℃(填“>”“<”或“=”)_______25℃;在t℃时将pH=11的NaOH溶液aL与pH=1的H2SO4溶液bL混合(忽略混合后溶液体积的变化),若所得混合液的pH=2,则a:b=____。
CO和NO对环境影响较大,属于当今社会热点问题。请回答下列问题
(1)降低汽车尾气的反应:2NO(g)+2CO(g) N2(g)+2CO2(g)若NO中的键能是632kJ/mol,CO中的键能是1072 kJ/mol,CO2中C=O的键的键能为750 kJ/mol,N2中的键能是946kJ/mol,则该反应的△H=___________
N2(g)+2CO2(g)若NO中的键能是632kJ/mol,CO中的键能是1072 kJ/mol,CO2中C=O的键的键能为750 kJ/mol,N2中的键能是946kJ/mol,则该反应的△H=___________
(2)若在一定温度下,将1.4molNO、1.2molCO充入1L固定容积的容器中,反应过程中各物质的浓度变化如图所示

①该反应的平衡常数K=___________
②若保持温度不变,20min时再向容器中冲入CO、N2各0.8mol,平衡将向_______移动(填“向左”“向右”或“不”)
③20min时,若改变反应条件,导致CO浓度发生如图所示的变化,则改变的条件可能 是_______(填序号)
a.缩小容器体积 b.增加CO2的量 c.升高温度 d.加入催化剂
(3)固氮是科学家致力研究的重要课题,自然界中存在天然的大气固氮过程:N2(g)+O2(g)→2NO (g)-180.8kJ,工业合成氨则是人工固氮.
分析两种固氮反应的平衡常数,下列结论正确的是______________。
| 反应 |
大气固氮 |
工业固氮 |
||||
| 温度/℃ |
27 |
2000 |
25 |
350 |
400 |
450 |
| K |
3.84×10-31 |
0.1 |
5×108 |
1.847 |
0.507 |
0.152 |
A.常温下,大气固氮很难进行,而工业固氮却能非常容易进行
B.K越大说明合成氨反应的速率越大
C.工业固氮时温度越低,氮气与氢气反应越完全
D.模拟大气固氮应用于工业上的意义不大
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,工业上合成氨反应通常用铁触媒作催化剂,反应方程式为:N2+3H2 2NH3 △H<0。
2NH3 △H<0。
(1)已知N2(g)+3H2(g)  2NH3(g) ΔH=-92kJ·mol-1,拆开1mol H-H键,1molN≡N键分别需要的能量是436kJ、、946kJ,则拆开1molN-H键需要的能量是__________。
2NH3(g) ΔH=-92kJ·mol-1,拆开1mol H-H键,1molN≡N键分别需要的能量是436kJ、、946kJ,则拆开1molN-H键需要的能量是__________。
(2)合成氨反应达到平衡后将容器的容积压缩到原来的1/2,其他条件不变,对平衡体系产生的影响是 (填字母序号)。
| A.c(H2)减小 | B.正反应速率加快,逆反应速率减慢 |
| C.NH3的物质的量增加 | D.平衡常数K增大 |
E.平衡向正方向移动
(3) 如图2所示,在甲、乙两容器中分别充入1molN2和3molH2,使甲、乙两容器初始容积相等。在相同温度下发生反应N2(g)+3H2(g)  2NH3(g) ,并维持反应过程中温度不变。已知甲容器中H2的转化率随时间变化的图像如图3所示,请在图3中画出乙容器中H2的转化率随时间变化的图像。
2NH3(g) ,并维持反应过程中温度不变。已知甲容器中H2的转化率随时间变化的图像如图3所示,请在图3中画出乙容器中H2的转化率随时间变化的图像。


(4)若反应N2(g)+3H2(g)  2NH3(g)在一容积固定不变的容器内进行,并维持反应过程中温度不变。若平衡从正向建立,且起始时N2与H2的物质的量分别为amol、bmol,当a:b=______时,达到平衡后NH3的体积分数最大。
2NH3(g)在一容积固定不变的容器内进行,并维持反应过程中温度不变。若平衡从正向建立,且起始时N2与H2的物质的量分别为amol、bmol,当a:b=______时,达到平衡后NH3的体积分数最大。
高温下CuO(s)+CO(g) Cu(s)+CO2(g)已知该反应在不同温度下的平衡常数如下:1000℃ K=4.0 1150℃ K=3.7 1300℃ K=3.5 ;请回答下列问题:
Cu(s)+CO2(g)已知该反应在不同温度下的平衡常数如下:1000℃ K=4.0 1150℃ K=3.7 1300℃ K=3.5 ;请回答下列问题:
(1)该反应的平衡常数表达式___________.
(2)在一个容积为2L的密闭容器中,1000℃时加入Cu、 CuO、CO、CO2各0.2 mol,反应经过10min后达平衡。求该时间范围内反应的平均反应速率v(CO2)﹦ 。
(3)以下措施中,能使反应(2)中的正反应速率显著加快同时不影响CO的平衡转化率的是 (填字母序号)。
A、增加CO的浓度 B、增加CuO的量 C、移出部分CO2 D、提高反应温度 E、减小容器的容积
(4)1000℃时测得在2L的密闭容器中反应体系中某时刻各物质的物质的量见下表:
| CuO |
CO |
Cu |
CO2 |
| 0.8mol |
0.4mol |
0.6mol |
0.6mol |
此时反应中正、逆反应速率的关系式是 (填代号)。
A.v(正)>v(逆) B.v(正)<v(逆) C.v(正)=v(逆) D.无法判断
合成氨是人类科学技术上的一项重大突破,其反应原理为:
N2(g)+3H2(g) 2NH3(g) ∆H= —92.4kJ•mol‾1一种工业合成氨的简易流程图如下:
2NH3(g) ∆H= —92.4kJ•mol‾1一种工业合成氨的简易流程图如下:

(1)天然气中的H2S杂质常用氨水吸收,写出氨水的电离方程式 。吸收产物为NH4HS。一定条件下向NH4HS溶液中通入空气,得到单质硫并使吸收液再生,写出吸收液再生反应的化学方程式 。
(2)步骤II中制氢气原理如下:
①CH4(g)+H2O(g)  CO(g)+3H2(g) △H=+206.4 kJ·mol-1
CO(g)+3H2(g) △H=+206.4 kJ·mol-1
②CO(g)+ H2O(g)  CO2(g)+H2(g) △H=-41.2 kJ·mol-1
CO2(g)+H2(g) △H=-41.2 kJ·mol-1
则反应CH4(g)+2H2O(g)  CO2(g)+4H2(g) △H= kJ·mol-1。
CO2(g)+4H2(g) △H= kJ·mol-1。
对于反应①,一定可以提高平衡体系中H2百分含量,又能加快反应速率的措施是(填编号) 。
a.升高温度 b.增大水蒸气浓度 c.加入催化剂 d.降低压强
(3)利用反应②,将CO进一步转化,可提高H2产量。若1mol CO和H2的混合气体(CO的体积分数为20%)与H2O蒸气反应,得到1.18mol CO、CO2和H2的混合气体,则CO转化率为 。
(4)下图1表示500℃、60.0MPa条件下,H2和N2为原料气的投料比与平衡时NH3体积分数的关系。根 据图中a点数据计算N2的平衡体积分数为 。
(5)依据温度对合成氨反应的影响,在下图2坐标系中,画出一定条件下的密闭容器内,从通入起始原料气开始,随温度不断升高,NH3物质的量变化的曲线示意图。

图1 图2
(6)简述本流程中提高合成氨原料总转化率的方法 。
(Ⅰ)浓硝酸与浓盐酸混合过程中会产生少量的黄绿色气体单质X、化合物M和无色液体,化合物M中所有原子均达到8电子的稳定结构。2mol M加热分解生成1mol氧化产物X和2mol无色气体Y,Y遇到空气呈现红棕色。
(1)镁与气体X反应产物的电子式 。
(2)浓硝酸与浓盐酸反应的化学方程式为 。
(3)化合物M水解生成两种酸,为非氧化还原反应,该反应的化学方程式为 。
(Ⅱ)石油铁储罐久置未清洗易引发火灾,经分析研究,事故是由罐体内壁附着的氧化物甲与溶于石油中的气态氢化物乙按1︰3反应生成的物质丙自燃引起的。某研究小组将一定量的丙粉末投入足量的浓盐酸中发生反应,得到4.8g淡黄色固体和气体乙,乙在标准状况下的密度为1.52g·L-1。过滤后向滤液(假设乙全部逸出)中加入足量的NaOH溶液,先出现白色沉淀,最终转变为红褐色沉淀,过滤、洗涤、灼烧后的固体质量为24g。已知气体乙可溶于水。请回答下列问题:
(4)甲的化学式为 。
(5)丙在盐酸中反应的化学方程式为 。
(6)丙与盐酸反应后的滤液暴露在空气中一段时间颜色加深,其原因是(用离子方程式表示) 。
(7)为消除石油铁储罐的火灾隐患,下列措施可行的是(填编号) 。
| A.石油入罐前脱硫 | B.定期用酸清洗罐体 |
| C.罐体内壁涂刷油漆 | D.罐体中充入氮气 |