取一定质量NaHCO3和Na2O2的固体混合物放入一密闭容器中加热至250℃,充分反应后排出所有气体。将反应后的固体分成完全相同的两份,将其中一份投入到足量的BaCl2溶液中,最后可得到3.94g沉淀。另一份溶于适量的水,无气体放出,再向水溶液中缓慢逐滴加入某物质的量浓度的盐酸,产生气体与所加盐酸体积之间的关系如下图所示。试回答下列问题:
(1)反应后的固体的成分(填化学式)___________ ;
(2)加入盐酸后产生的气体在标准状况下的体积为_________L;
(3)盐酸中HCl的物质的量浓度____________;
(4)原固体混合物中n(NaHCO3) =_____________、n(Na2O2) =_____________。
质量为10g的镁铝合金,与200mL 0.5mol•L﹣1的氢氧化钠溶液恰好完全反应.已知铝与氢氧化钠溶液反应的化学方程式为:2Al+2NaOH+6H2O═2Na[Al(OH)4]+3H2↑求:
(1)合金中铝的质量分数
(2)生成气体在标准状况下的体积.
某K2CO3与KHCO3的混合物共6.14 g,加热分解后质量减少为5.52 g。
(1)求原混合物中K2CO3的质量分数。(写出计算过程,计算结果精确到0.1%)
(2)若将原混合物溶于200 mL水配成溶液,向溶液中逐滴加入1.0 mol·L-1的稀盐酸。当加入的稀盐酸的体积为 mL时开始产生气体;当加入50 mL稀盐酸时,产生的气体在标准状况下的体积为 mL。
将6.50g锌投入200mL某浓度的盐酸中,锌和盐酸恰好完全反应.求:
(1)6.50g锌的物质的量;
(2)反应中生成的H2在标准状况下的体积.
(3)所用盐酸中HCl中的物质的量浓度;
在标准状况下,由CO和CO2组成的混合气体11.2L,质量为18.8g,则混合气体中n(CO):n(CO2)=______________;CO的物质的量分数为_____________;CO2的质量分数为_____________;混合气体的密度为_____________g/L.
现有m g某气体X2,它的摩尔质量为M g·mol-1.若阿伏加德罗常数用NA表示,则:
(1)该气体的物质的量为____________________mol.
(2)该气体所含原子总数为_______________________个.
(3)该气体在标准状况下的体积为____________________L.
(4)该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为__________________.
(5)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为__________________mol·L-1.
(1)N原子的摩尔质量是_________,1mol HNO3的质量是____________,1mol HNO3约含有_________________个氧原子.
(2)标准状况下11.2L HCl气体的物质的量是______________,将此HCl气体 溶于水中配成1L溶液,所得盐酸溶液的物质的量浓度是____________________.
(3)2mol OH-约含有___________________个电子.
常温下,在35.5g水中溶解12.5g CuSO4·5H2O,恰好达到饱和,该溶液密度为1.20g /cm3,求:(1)该溶液中阴阳离子的总物质的量;
(2)该溶液中CuSO4的物质的量浓度;
有一瓶(约100mL)硫酸和硝酸的混合溶液,取出10.00mL该混合溶液,加入足量氯化钡溶液,充分反应后过滤、洗涤、烘干,可得到4.66g沉淀。滤液跟2.00mol·L-1NaOH溶液反应,共用去35.00mL碱液时恰好中和。请分别计算混合液中H2SO4和HNO3的物质的量浓度(请分步计算,写出计算过程)
准确称取22.7g某矿石样品(含Al2O3、Fe2O3和不溶于水和酸的杂质),放入盛有100mL某浓度的硫酸的烧杯中,充分反应后过滤,向滤液中加入10mol/L的NaOH溶液,产生的沉淀的质量m与加入NaOH溶液的体积V的关系如下图所示。请回答:
(1)硫酸的物质的量浓度是多少?
(2)若a=10,矿石样品中Fe2O3的质量是多少?
(3)试计算a的取值范围。
常温下,稀硝酸可以将铜溶解,反应方程式为3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O。生成的NO在标准状况时的体积为5.6L,计算
(1)需要参加反应的铜的质量是多少?
(2)被氧化的硝酸的物质的量是多少?
(3)反应过程中转移的电子数?
过氧化钙是一种安全无毒的物质,带有数量不等的结晶水,通常还含有部分CaO。
(1)称取0.542g过氧化钙样品,灼热时发生如下反应: 2CaO2·XH2O  2CaO + O2↑ + 2XH2O,得到的O2在标准状况下体积为67.2mL,该样品中CaO2的物质的量为 。
2CaO + O2↑ + 2XH2O,得到的O2在标准状况下体积为67.2mL,该样品中CaO2的物质的量为 。
(2)另取同一样品0.542g,溶于适量的稀盐酸中,然后加入足量的Na2CO3溶液,将溶液中Ca2+全部转化为CaCO3沉淀,得到干燥的CaCO3 0.70g。
① 试计算样品中CaO的质量。
② 试计算样品中CaO2·XH2O的X值。
将等物质的量的A、B混合于2L的密闭容器中,发生如下反应:3A(g)+B(g)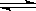 xC(g)+2D(g),经5min后,测得D的浓度为0.5mol/L,c(A):c(B)=3:5,C的平均反应速率是0.1mol·L-1·min-1。求:
xC(g)+2D(g),经5min后,测得D的浓度为0.5mol/L,c(A):c(B)=3:5,C的平均反应速率是0.1mol·L-1·min-1。求:
(1)x值;
(2)B的平均反应速率;
(3)此时A的浓度及反应开始前放入容器中的A、B的物质的量。