短周期元素X、Y、Z、W的原子序数依次增大,X 原子的最外层电子数是其内层电子总数的3 倍,Y 原子的最外层只有2 个电子,Z 单质可制成半导体材料,W与X属于同一主族。下列叙述正确的是
| A.化合物YX、ZX2、WX3都是酸性氧化物 |
| B.元素W 的最高价氧化物对应水化物的酸性比Z 的弱 |
| C.原子半径的大小顺序: rY >rZ >rW >rX |
| D.元素X 的简单气态氢化物的热稳定性比W 的弱 |
一定条件下A、B、C有如图所示的转化关系,且△H=△H1+△H2 符合上述转化关系的A、C可能是

①Fe、FeCl3 ②C、CO2 ③AlCl3、NaAlO2 ④NaOH、NaHCO3 ⑤S、SO3 ⑥Na2CO3、CO2
A.只有②③④⑥ B.除①外 C.除⑤外 D.全部
实验室用标准盐酸溶液测定某NaOH溶液的浓度,用甲基橙作指示剂,下列操作中可能使测定结果偏低的是
| A.锥形瓶内溶液颜色变化由黄色变橙色,立即记下滴定管液面所在刻度 |
| B.开始实验时酸式滴定管尖嘴部分有气泡,在滴定过程中气泡消失 |
| C.酸式滴定管在装酸液前未用标准盐酸溶液润洗2~3次 |
| D.盛NaOH溶液的锥形瓶滴定前用NaOH溶液润洗2~3次 |
已知:2H2(g)+O2(g)=2H2O(l)ΔH=-571.6kJ·mol-1
2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)ΔH=-1452kJ·mol-1
H+(aq)+OH-(aq)=H2O(l)ΔH=-57.3kJ·mol-1
下列说法正确的是
| A.H2(g)的燃烧热ΔH=-571.6 kJ·mol-1 |
| B.H2SO4(aq)+Ba(OH)2(aq)= BaSO4(s)+2H2O(l) ΔH=-57.3 kJ·mol-1 |
| C.同质量的H2(g)和CH3OH(l)完全燃烧生成液态水,H2(g)放出的热量多 |
| D.3H2(g)+CO2(g)= CH3OH(l)+H2O(l) ΔH=+131.4 kJ·mol-1 |
能正确表示下列反应的离子方程式是
| A.用过量氨水吸收工业尾气中的SO2:2NH3·H2O+SO2=2NH4++SO32-+H2O |
| B.NaHSO3溶液中通入少量Cl2:HSO3- + Cl2+ H2O=3H+ +SO42- +2Cl- |
C.氯化钠与浓硫酸混合加热:H2SO4+2Cl- SO2↑+Cl2↑+H2O SO2↑+Cl2↑+H2O |
| D.磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3-=3Fe3++NO↑+3H2O |
据悉,奥运会上使用的发令枪所用的“火药”成分是氯酸钾和红磷,经撞击发出响声,同时产生白色烟雾,撞击时发生反应的化学方程式为:5KClO3+6P=3P2O5+5KCl,则下列有关叙述错误的是
| A.上述反应是放热反应 |
| B.产生白色烟雾的原因是生成的P2O5白色固体小颗粒(烟)吸水性很强,吸收空气中的水分,生成磷酸小液滴(雾) |
| C.上述反应中消耗3molP时,转移电子的物质的量为15mol |
| D.该反应氧化剂与还原剂物质的量之比为6:5 |
NA为阿伏加德罗常数的值,下列说法正确的是
| A.18gD2O和18gH2O中含有的质子数均为10NA |
| B.2L0.5mol/L亚硫酸溶液中含有的氢离子数为2NA |
| C.过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA |
| D.密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA |
下列各组离子在特定条件下一定能够大量共存的是
| A.含有较多Fe3+的溶液:Na+、SO42-、HS-、NH4+ |
| B.pH=1的溶液:K+、Fe2+、NO3-、Na+ |
| C.c(OH-)=1mol·L-1的溶液:AlO2-、CH3COO-、K+、Ba2+ |
| D.遇Al能放出H2的溶液:HCO3-、K+、Mg2+、Cl- |
一定温度下,取pH=12的NaOH溶液和氨水各10 mL,分别用蒸馏水冲稀至1 L。关于稀释后的溶液的pH的说法正确的是
| A.NaOH溶液的pH小于氨水的pH | B.NaOH溶液的pH大于氨水的pH |
| C.两溶液的pH相等 | D.无法判别两溶液pH的相对大小 |
2015年8月12日天津港瑞海公司危险化学品仓库发生特大火灾爆炸事故,事故警示我们,化学药品的安全存放是非常重要的。下列有关化学药品的存放说法不正确的是
| A.液溴易挥发,应用少量的水液封并放在冷暗处保存 |
| B.碳酸钠虽然属于盐,但是其水溶液呈碱性,应用带橡胶塞的试剂瓶保存 |
| C.金属钠遇到氧气和水均立即反应,应保存在煤油里 |
| D.硝酸见光易分解、易挥发,应用棕色广口试剂瓶密封保存 |
一定温度下,水溶液中H+和OH-的浓度变化曲线如图,下列说法正确的是( )
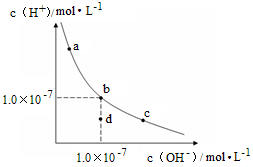
| A.升高温度,可能引起由c向b的变化 |
| B.该温度下,水的离子积常数为1.0×10-13 |
| C.该温度下,加入FeCl3可能引起由b向a的变化 |
| D.该温度下,稀释溶液可能引起由c向d的变化 |
下列溶液中有关物质的量浓度关系正确的是( )
| A.碳酸氢钠溶液:c(Na+)+ c(H+)= c(CO32-)+ c(OH-)+ c(HCO3-) |
| B.物质的量浓度相等的CH3COOH和CH3COO Na 溶液等体积混合:c(CH3COOH)+ c(CH3COO-)="2" c(Na+) |
| C.硫酸铜溶液与过量浓氨水反应的离子方程式为:Cu2++ 2NH3•H2O= Cu(OH)2↓ +2 NH4+ |
| D.一定浓度的盐酸和氨水混合可能出现c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
新型NaBH4/H2O2燃料电池(DBFC)的结构如图所示,该电池总反应方程式:NaBH4+4H2O2═NaBO2+6H2O,有关的说法不正确的是( )

A.电极B为正极,纳米MnO2层的作用是提高原电池的工作效率
B.放电过程中,Na+从正极区向负极区迁移
C.电池负极的电极反应为:BH4-+8OH--8e-═BO2-+6H2O
D.在电池反应中,每消耗1L 6mol/L H2O2溶液,理论上流过电路中的电子为12mol