按图甲装置进行实验,若图乙中横坐标x表示通过电极的电子的物质的量,下列叙述正确的是 ( )
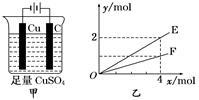
| A.电解过程中,Cu2+浓度不变 |
| B.E表示反应生成O2的物质的量 |
| C.电解过程中,石墨棒附近溶液的pH有所增大 |
| D.若向烧杯中加入2 mol CuO可以使电解质恢复到电解前的浓度,则电解过程中共转移了4mol电子。 |
室温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A.pH=2的溶液中:Na+、Al3+、NO3-、Cl- |
| B.惰性电极电解的Cu SO4溶液:Na+、Fe2+、NO3-、Cl- |
| C.1.0 mol/L的NaAlO2溶液中:K+、Ca2+、NO3-、HCO3- |
| D.由水电离的c(H +) = 1.0×10-13mol/L的溶液中:K+、NH4+、SO42-、NO3- |
对于已达到平衡状态的可逆反应:A+B C+D,若t1时增大压强,正、逆反应速率变化如图所示,下列有关A、B、C、D四种物质的状态叙述中正确的是( )
C+D,若t1时增大压强,正、逆反应速率变化如图所示,下列有关A、B、C、D四种物质的状态叙述中正确的是( )

A.A、B、C、D一定都是气体
B.A、B一定都是气体,C、D只有一种是气体
C.C、D一定都是气体,A、B只有一种是气体
D.C、D至少有一种是气体,A、B也至少有一种是气体
在一体积固定的密闭容器中通入2mol A和1mol B,一定条件下发生如下反应:
2A(g)+B(g)  3C(g) ΔH<0,反应达到平衡后,改变一个条件(x),下列量(y)一定符合图中曲线的是( )
3C(g) ΔH<0,反应达到平衡后,改变一个条件(x),下列量(y)一定符合图中曲线的是( )

下列有关说法正确的是( )
| A.燃料电池工作时,燃料在负极被还原 |
| B.氯碱工业采用的是以铜为电极,阳离子交换膜来电解饱和食盐水 |
C. 有Mg、Al和NaOH溶液组成的原电池,其负极为铝,电极反应为Al-3e- = Al3+ 有Mg、Al和NaOH溶液组成的原电池,其负极为铝,电极反应为Al-3e- = Al3+ |
| D.二次电池充电时,电池负极连接到外接电源的负极 |
已知:H2(g)+Cl2(g)==="2HCl(g)" ΔH=-Q kJ·mol-1(Q>0),下列说法正确的是( )
| A.在一定条件下,1个氢气与1个氯气反应生成2个氯化氢放出Q kJ热量 |
| B.在一定条件下,1 mol氢气与1 mol氯气反应生成2 mol液态氯化氢放出Q kJ热量 |
| C.在相同条件下,1 mol氢气与1 mol氯气的能量总和大于2 mol氯化氢气体的能量 |
| D.在标准状况下,1L氢气和1 L氯气完全反应生成2L氯化氢气体放出QkJ热量 |
化合物Z由如下反应得到: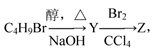 Z的结构简式不可能是( )
Z的结构简式不可能是( )
| A.CH3CH2CHBrCH2Br | B.CH3CH(CH2Br)2 |
| C.CH3CHBrCHBrCH3 | D.CH2BrCBr(CH3)2 |
设NA为阿伏加德罗常数的值,下列有关叙述不正确的是( )
| A.标准状况下,1 L庚烷所含有的分子数为NA/22.4 |
| B.1 mol甲基(—CH3)所含电子数为9NA |
| C.标准状况下,B2H6(g)和C2H4的混合气体22.4 L,所含的电子数约为16NA |
| D.26 g C2H2和苯蒸气的混合气体中所含的C原子数为2NA |
已知分子式为C12H12的物质A的结构简式为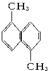 ,其苯环上的二溴代物有9种同分异构体,由此推断A苯环上的四溴代物的同分异构体的数目有( )
,其苯环上的二溴代物有9种同分异构体,由此推断A苯环上的四溴代物的同分异构体的数目有( )
| A.9种 | B.10种 | C.11种 | D.12种 |
一次性饭盒中石蜡(高级烷烃)和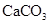 在食物中的溶出量是评价饭盒质量的指标之一,测定溶出量的主要实验步骤设计如下: 剪碎、称重→浸泡溶解→过滤→残渣烘干→冷却、称重→恒重,为了将石蜡溶出,应选用的试剂是( )
在食物中的溶出量是评价饭盒质量的指标之一,测定溶出量的主要实验步骤设计如下: 剪碎、称重→浸泡溶解→过滤→残渣烘干→冷却、称重→恒重,为了将石蜡溶出,应选用的试剂是( )
| A.氢氧化钠溶液 | B.盐酸 | C.稀硫酸 | D.正己烷 |
用a、b两个质量相等的Pt电极电解AlCl3和CuSO4的混合溶液[ n(AlCl3) : n(CuSO4) = 1:9 ]。 t1时刻a电极得到混合气体,其中Cl2在标准状况下为224 mL(忽略气体的溶解);t2时刻Cu全部在电极上析出。下列判断正确的是
| A.a电极与电源的负极相连 |
| B.t2时,两电极的质量相差3.84g |
| C.电解过程中,溶液的pH不断增大 |
| D.t2时,b的电极反应是4OH――4e-=2H2O+O2↑ |
甲醇燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成.电池的总反应式为2CH3OH+3O2+4OH-═2CO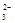 +6H2O.则下列说法正确的是
+6H2O.则下列说法正确的是
| A.电池放电时通入空气的电极为负极 |
| B.电池放电时负极的电极反应式为CH3OH-6e-+H2O═CO2↑+6H+ |
C.由于CO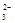 水解显碱性,电池放电时,电解质溶液的pH逐渐增大 水解显碱性,电池放电时,电解质溶液的pH逐渐增大 |
| D.电池放电时每消耗1molCH3OH转移6mol电子 |
下列有关金属腐蚀与防护的说法正确的是
| A.黄铜(铜锌合金)制作的铜锣易产生铜绿 |
| B.镀锡铁制品和镀锌铁制品的镀层破损时,镀锡铁中铁的腐蚀速率更快 |
| C.在轮船船体四周镶嵌锌块保护船体不受腐蚀的方法叫阳极电化学保护法 |
| D.不锈钢有较强的抗腐蚀能力是因为在钢铁表面上镀上了铬 |
常温时,Ksp[Mg(OH)2] = 1.1×10-11,Ksp(AgCl) = 1.8×10-10,Ksp(Ag2CrO4) = 1.9×10-12 Ksp(CH3COOAg) = 2.3×10-3,下列叙述不正确的是
| A.浓度均为0.2mol·L-1AgNO3溶液和CH3COONa溶液等体积混合一定产生CH3COOAg沉淀 |
| B.将0.001mol·L-1的AgNO3溶液滴入0.001mol·L-1的KCl和0.001mol·L-1的K2CrO4的混合溶液中,先产生Ag2CrO4沉淀 |
| C.c(Mg2+)为0.11mol·L-1的溶液中要产生Mg(OH)2沉淀,溶液的pH要控制在9以上 |
| D.在其他条件不变的情况下,向饱和AgCl水溶液中加入NaCl溶液,Ksp(AgCl)不变 |
向体积为Va的0.05 mol·L-1CH3COOH溶液中加入体积为Vb的0.05 mol·L-1KOH溶液,下列关系错误的是
| A.Va>Vb时:c(CH3COOH)+c(CH3COO-)>c(K+) |
| B.Va=Vb时:c(CH3COOH)+c(H+)=c(OH-) |
| C.Va<Vb时:c(CH3COO-)>c(K+)>c(OH-)>c(H+) |
| D.Va与Vb任意比时:c(K+)+c(H+)=c(OH-)+c(CH3COO-) |