燃烧含硫高的煤和石油是形成酸雨的重要原因,现取放置一段时间的雨水,经分析测得除H+外的各离子浓度为:c(NH4+)=2×10-5mol/L,c(Cl-)=6×10-5mol/L ,c(Na+)=1.9×10-5mol/L ,c(NO3-)=2.3×10-5mol/L, c(SO42-)=2.8×10-5mol/L,则此次酸雨的pH为
| A.3 | B.4 | C.5 | D.6 |
下列说法正确的是:
| A.工业上常使用电解精炼法将粗铜提纯,在电解精练时,阳极减少的质量等于阴极增加的质量 |
| B.心脏起搏器中使用的新型Li-I2电池的寿命已超过10年,其反应可简单表示为2Li+I2=2LiI,阴极反应为:2Li-2e-=2Li+ |
| C.为了降低某水库的铁闸门被腐蚀的速率,其中焊接在铁闸门上的金属材料可以是锌 |
| D.某物质的溶解度为难溶,则该物质不溶于水 |
下列各组离子,在所给的条件下,一定能够大量共存的是
| A.在pH=0的溶液中:Fe2+、Mg2+、CO32-、NO3- |
| B.在由水电离出的c(H+)=1×10-12mol/L的溶液中:HCO3-、Al3+、NH4+、ClO- |
| C.在滴加酸碱指示剂酚酞试液后呈现红色的溶液中:Na+、Cl-、AlO2-、CO32- |
| D.在AlCl3溶液中:K+、NO3-、OH-、Na+ |
如图是表示:2X(g)+Y(g)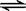 Z(g)+R(s)+Q(g)的气体反应速率(υ)与时间(t)的关系,
Z(g)+R(s)+Q(g)的气体反应速率(υ)与时间(t)的关系,
t1时开始改变条件,则所改变的条件符合曲线的是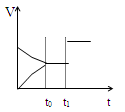
| A.减少Z物质 | B.使用催化剂 | C.升高温度 | D.加大压强 |
常温下,下列混合溶液的pH一定大于7的是
| A.0.01mol/L的盐酸和0.01mol/L的NaOH溶液等体积混合 |
| B.pH=3的盐酸和pH=11的氨水溶液等体积混合 |
| C.0.01mol/L的盐酸和0.01mol/L的氨水溶液等体积混合 |
| D.pH=3的醋酸和pH=11的NaOH溶液等体积混合 |
下列离子方程式方程式中正确的是
A.NaHCO3溶液中HCO3-水解:HCO3-+ H2O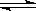 H2CO3+OH- H2CO3+OH- |
| B.AlCl3溶液中Al3+水解:Al3++3H2O = Al(OH)3↓+3H+ |
C.NaHS溶液中HS-水解:HS-+H2O 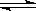 H3O++S2- H3O++S2- |
D.碳酸溶液中H2CO3的电离:H2CO3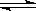 2H++ CO32- 2H++ CO32- |
可逆反应2SO2 (g)+ O2 (g)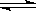 2SO3(g)达到平衡的标志是
2SO3(g)达到平衡的标志是
① 消耗2 mol SO2的同时生成2 mol SO3
②SO2、O2与SO3的物质的量之比为2∶1∶2
③ 反应混合物中,SO3的质量分数不再改变
| A.①② | B.①③ | C.只有③ | D.只有① |
下列事实,可以证明氨水是弱碱的是
| A.氨水能跟氯化亚铁溶液反应生成氢氧化亚铁 |
| B.铵盐受热易分解 |
| C.0.1mol/L的氨水可以使酚酞试液变红 |
| D.0.1mol/L的NH4Cl溶液的pH约为5 |
某学生的实验报告所列出的下列数据中合理的是
| A.用10mL量筒量取7.13mL稀盐酸 |
| B.用pH计测得某稀盐酸的pH为1.54 |
| C.广泛pH试纸润湿后,测得某溶液的pH为2.3 |
| D.用标准的盐酸滴定待测的NaOH溶液时,滴定完毕后,酸式滴定管中盐酸的读数为17.1mL |
甲、乙两个电解池均以Pt为电极,且互相串联。甲池盛有CuSO4溶液,乙池中盛有一定量的某盐溶液。通电一段时间后,测得甲池电极质量增加0.64g,乙池电极上析出0.24 g金属,则乙池中的溶质可能是
| A.MgSO4 | B.Al(NO3)3 | C.CuSO4 | D.Na2SO4 |
25℃、101 kPa下,2g氢气燃烧生成液态水,放出285.8kJ热量,表示该反应的热化学方程式正确的是
A.2H2(g)+O2(g) ="=" 2H2O(1)△H= ―285.8kJ/mol |
| B.2H2(g)+ O2(g) ="=" 2H2O(1)△H= +571.6 kJ/mol |
| C.2H2(g)+O2(g) ="=" 2H2O(g)△H= ―571.6 kJ/mol |
D.H2(g)+ O2(g) ="=" H2O(1)△H= ―285.8kJ/mol O2(g) ="=" H2O(1)△H= ―285.8kJ/mol |
下列说法正确的是
| A.可逆反应的化学平衡常数K值的大小和反应的温度、各组分的浓度以及体系的压强都有关 |
| B.任何条件下,只要c(H+)>c(OH-),水溶液就一定显酸性 |
| C.盐酸中无OH-,烧碱溶液中无H+ |
| D.水的离子积常数Kw和水的电离平衡常数K电离是两个没有任何关系的物理量 |
有关如右图所示原电池的叙述,正确的是(盐桥中装有含琼胶的KCl饱和溶液)
| A.铜片上有气泡逸出 |
| B.反应中,盐桥中的K+会移向CuSO4溶液 |
| C.取出盐桥后,电流计依然发生偏转 |
| D.反应前后铜片质量不改变 |
下列事实不能用勒夏特利原理来解释的是
| A.增大压强,有利于SO2和O2反应生成SO3 |
| B.热的纯碱溶液去油污能力较强 |
| C.加催化剂使N2和H2在一定条件下转化为NH3 |
| D.常温下pH=3的H2SO4溶液中水的电离程度小于pH=3的NH4Cl溶液中水的电离程度 |