下列事实中,与电化学腐蚀无关的是
| A.在空气中,光亮的银表面逐渐变暗 |
| B.为保护海轮的船壳,常在船壳上镶入锌块 |
| C.埋在潮湿土壤里的铁管比埋在干燥土壤里的铁管更易被腐蚀 |
| D.镀锡的铁制品,镀层部分受损后,露出的铁表面易被腐蚀 |
下列关于金属腐蚀的叙述正确的是
| A.金属(M表示金属) 被腐蚀的本质是: M n+ + ne- = M |
| B.金属不可能在碱性环境中发生电化学腐蚀 |
| C.镀锌铁的镀层破损后,镀层仍能对铁起保护作用 |
| D.钢管与外加直流电源的正极相连,以保护它不受腐蚀 |
将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆周中心区(a)已被腐蚀而变暗,在液滴外沿棕色铁锈环(b),如图所示.导致该现象的主要原因是液滴之下氧气含量比边缘少.下列说法正确的是( )
| A.液滴中的Cl﹣由a区向b区迁移 |
| B.液滴边缘是正极区,发生的电极反应为:O2+2H2O+4e﹣═4OH﹣ |
| C.液滴下的Fe因发生还原反应而被腐蚀,生成的Fe2+由a区向b区迁移,与b区的OH﹣形成Fe(OH)2,进一步氧化、脱水形成铁锈 |
| D.若改用嵌有一铜螺丝钉的铁板,在铜铁接触处滴加NaCl溶液,则负极发生的电极反应为Cu﹣2e﹣═Cu2+ |
下列各容器中盛有海水,铁在其中被腐蚀时由快到慢的顺序是
| A.②>①>③>④ | B.④>②>①>③ | C.④>②>③>① | D.③>②>④>① |
【改编】下列叙述的原因不是由于原电池造成的是
| A.铁与酸反应滴加硫酸铜后反应加快 |
| B.金属在潮湿空气中更容易腐蚀 |
| C.镀锡铁镀层破损后腐蚀加快 |
| D.浓硝酸比稀硝酸更能氧化金属铜 |
埋在地下的铸铁输油管道,在下列各种情况下,腐蚀最慢的是( )
| A.在含铁元素较多的酸性土壤中 |
| B.在潮湿疏松透气的土壤中 |
| C.在干燥致密不透气的土壤中 |
| D.在含碳粒较多的潮湿透气的中性土壤中 |
有关下列图像的说法正确的是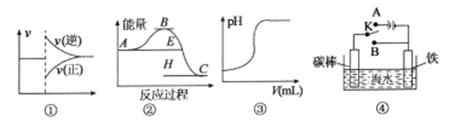
| A.图①可以表示,某化学平衡体系改变温度后反应速率随时间的变化 |
| B.根据图②判断,物质A反应生成物质C的△H>O |
| C.图③表示向一定量的硫酸溶液中滴加一定浓度氢氧化钠溶液时的pH变化 |
| D.图④中开关K置丁A或B处均可减缓铁的腐蚀 |
下列有关原电池和金属腐蚀的说法错误的是
| A.普通锌锰干电池碳棒是负极,锌片是正极 |
| B.盛水的铁器,在空气与水交界处更容易锈蚀 |
| C.为防止金属的腐蚀可在金属表面涂油漆、油脂 |
| D.用盐酸与锌反应制取氢气,含有杂质的锌比纯锌产生氢气速度快 |
下列现象或反应的原理解释正确的是
| |
现象或反应 |
原理解释 |
| A. |
铝箔在酒精灯火焰上加热熔化但不滴落 |
铝箔对熔化的铝有较强的吸附作用 |
| B. |
合成氨反应需在高温条件下进行 |
该反应为吸热反应 |
| C. |
镀层破损后,镀锡铁比镀锌铁易腐蚀 |
锡比锌活泼 |
| D. |
2CO=C+O2在任何条件下均不能自发进行 |
该反应△H>0,△S<0 |
下列有关说法错误的是
| A.为保护海轮的船壳,常在船壳上镶入锌块 |
| B.纯碱溶于热水中,去污效果增强,说明纯碱的水解反应是吸热反应 |
| C.已知工业合成氨气△H<0,达平衡后,升高温度,正反应速率减小,逆反应速率增大,平衡向逆反应方向移动 |
| D.NH3(g) + HCl(g)="=" NH4Cl(s)较低温度下能自发进行,说明该反应的△H<0 |
下列叙述错误的是()
| A. | 生铁中含有碳,抗腐蚀能力比纯铁弱 |
| B. | 用锡焊接的铁质器件,焊接处易生锈 |
| C. | 在铁制品上镀铜时,镀件为阳极,铜盐为电镀液 |
| D. | 铁管上镶嵌锌块,铁管不易被腐蚀 |
钢铁在腐蚀过程中,下列变化可能发生的是( )
①铁元素由+2价转化为+3价
②氧气被还原
③产生氢气
④Fe(OH)3失水生成Fe2O3·xH2O
⑤杂质碳被氧化而除去
| A.①② | B.③④ | C.①②③④ | D.①②③④⑤ |