期中备考总动员高一化学模拟测试卷基础版【人教版】3
化学家及其突出贡献为:①波义耳(化学元素概念);②道尔顿(原子学说);③门捷列夫(元素周期律);④玻尔(玻尔原子模型)。这些突出贡献提出的年代顺序是
| A.①②③④ | B.②④①③ | C.③①④② | D.③④①② |
第IA族元素具有相似的化学性质,是由于它们的原子具有相同的
| A.原子半径 | B.电子层数 | C.核外电子数 | D.最外层电子数 |
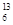 C-NMR(核磁共振)可以用于含碳化合物的结构分析有关
C-NMR(核磁共振)可以用于含碳化合物的结构分析有关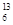 C的说法正确的是
C的说法正确的是
| A.质子数为6 | B.电子数为13 | C.中子数为6 | D.质量数为6 |
美国夏威夷联合天文中心的科学家发现了新的氢微粒,该微粒是由3个氢原子核(只含质子)和2个电子构成的,关于这种微粒的下列说法中正确的是
| A.是氢元素的一种新的同素异形体 |
| B.是氢元素的一种新的同位素 |
| C.该微粒比普通氢分子多一个氢原子核 |
| D.该微粒的组成可用H3表示 |
【原创】以下分子中,不是所有原子都满足最外层为8电子结构的是
| A.N2 | B.CO2 | C.HCl | D.PCl3 |
【改编】下列叙述的原因不是由于原电池造成的是
| A.铁与酸反应滴加硫酸铜后反应加快 |
| B.金属在潮湿空气中更容易腐蚀 |
| C.镀锡铁镀层破损后腐蚀加快 |
| D.浓硝酸比稀硝酸更能氧化金属铜 |
下列关于反应速率的说法中,错误的是
| A.反应速率可衡量化学反应的快慢 |
| B.决定反应速率的主要因素是反应物的性质 |
| C.可逆反应达到化学平衡时,正、逆反应速率都为0 |
| D.增大反应物浓度、提高反应物温度都能增大反应速率 |
在下图所示的柠檬电池中,外电路上的电子从电极Y流向电极X。若X为铁,则Y可能是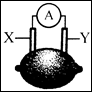
| A.锌 | B.石墨 | C.银 | D.铜 |
如图为某反应的焓变示意图,下列有关该反应的说法中正确的是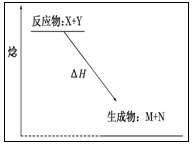
| A.ΔH>0 |
| B.X能量一定高于M |
| C.该反应为放热反应 |
| D.该反应一定不必加热就可以发生 |
下列措施不能够使化学反应速率加快的是
| A.升高温度 | B.降低温度 |
| C.使用催化剂 | D.增大固体反应物面积 |
【改编】对于锌、铜和硫酸铜组成的原电池(如图),下列有关说法不正确的是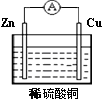
| A.电子从铜经过导线流向锌 |
| B.Cu片发生还原反应 |
| C.负极质量减少 |
| D.正极电极反应为: Cu2++2e-=Cu |
2010年4月中旬全球核安全峰会在华盛顿举行,发展核电、制裁核武器发展是会议主题,各式各样电池的发展是化学对人类的一项重大贡献,下列有关电池的叙述正确的是
| A.手机上用的锂离子电池属于一次电池 |
| B.锌锰干电池中,锌电极是负极 |
| C.氢氧燃料电池工作时氢气在负极被还原 |
| D.太阳能电池的主要材料为二氧化硅 |
下列关于铷的叙述不正确的是
| A.金属铷投入水中会引起爆炸 |
| B.铷是一种强还原剂,铷离子很稳定 |
| C.铷受热后,能在空气中剧烈燃烧,生成比过氧化物更复杂的氧化物 |
| D.铷原子的核电荷数比钾原子的核电荷数多,因此铷原子失电子的能力小于钾原子 |
元素周期表中位于金属元素和非金属元素交界处可找到的材料是
| A.制催化剂的材料 | B.耐高温、耐腐蚀的合金材料 |
| C.制农药的材料 | D.半导体材料 |
【改编】下列化合物只含有离子键的是
| A.H2O | B.NaOH | C.MgCl2 | D.NH4Cl |
在温度不变的条件下,在恒容的容器中进行下列反应: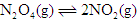 。若
。若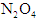 的浓度由
的浓度由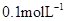 降到
降到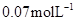 需要15s,那么
需要15s,那么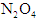 的浓度由
的浓度由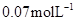 降到
降到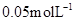 所需的反应时间
所需的反应时间
| A.等于5s | B.等于10s | C.大于10s | D.小于10s |
某探究性学习小组用相同质量的锌和相同浓度的足量的稀盐酸反应得到实验数据如下表所示:
| 实验编号 |
锌的状态 |
反应温度/℃ |
收集100 mL氢气所需时间/s |
| Ⅰ |
薄片 |
15 |
200 |
| Ⅱ |
薄片 |
25 |
90 |
| Ⅲ |
粉末 |
25 |
10 |
(1)该实验的目的是探究________、________对锌和稀盐酸反应速率的影响;
(2)实验Ⅰ和Ⅱ表明________,化学反应速率越大;
(3)能表明固体的表面积对反应速率有影响的实验编号是________和________;
(4)请设计一个实验方案证明盐酸的浓度对该反应的速率的影响:____________________。
某温度时,在2 L容器中A、B两种物质间的转化反应中,A、B物质的量随时间变化的曲线如图所示,由图中数据分析得: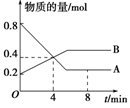
(1)该反应的化学方程式为_________________________________________。
(2)反应开始至4 min时,A的平均反应速率为________________________________。
(3)4 min时,反应是否达到平衡状态?________(填“是”或“否”),8 min时,v(正)________v(逆)(填“>”、“<”或“=”)。
【改编】部分中学化学常见元素原子结构及性质如表所示:
| 序号 |
元素 |
结构及性质 |
| ① |
A |
A单质是中学化学常见金属,在空气中燃烧生成淡黄色固体 |
| ② |
B |
B与A在同一周期,电子层数等于最外层电子数 |
| ③ |
C |
C是常见化肥的主要元素,单质常温下呈气态 |
| ④ |
D |
D单质被誉为“信息革命的催化剂”,是常用的半导体材料 |
| ⑤ |
E |
通常情况下,E没有正化合价,A、B、C、D、F都能与E形成化合物 |
| ⑥ |
F |
F在周期表中可以排在ⅠA族,也有人提出排在ⅦA族 |
(1)A原子在周期表中的位置为________。
(2)B与E形成的化合物的化学式为______,它属于_____化合物(填“酸性”或“碱性”或“两性”)。
(3)F与E可以形成10电子和18电子的两种化合物X和Y,区别X与Y的水溶液的实验方法是__________________________________________________________。
(4)C与E都是较活泼的非金属元素,用化学方程式表明这两种单质的氧化性强弱____________。
(5)A和B的最高价氧化物对应的水化物之间反应的离子方程式为:_________________________。
(共10分)某研究性学习小组设计了一组实验验证元素周期律。
(Ⅰ)为了用实验的方法验证镁和铝的金属性强弱,学生甲和学生乙分别设计了两种不同的方法:
方案一:学生甲用水作试剂,比较镁和铝与水反应的情况
方案二:学生乙用稀盐酸作试剂,比较镁和铝与稀盐酸反应的情况
回答下列问题:
(1)以上两实验方案实验现象较为明显的是方案 。
(2)学生乙在实验中取了一段黑色的镁带,投入稀盐酸中,现象不十分明显,请分析原因 。
(3)学生丙另辟蹊径,不用镁、铝的单质,而用镁、铝的可溶盐及一些其它化学试剂,进行实验也得出正确的结论,简述学生丙用的是什么方法?
(Ⅱ)学生丁设计了下图装置以验证氮、碳、硅元素的非金属性强弱。他设计的实验可直接证明三种酸的酸性强弱,已知A是强酸,常温下可与铜反应;B是块状固体;打开分液漏斗的活塞后,C中可观察到白色沉淀生成。

(1)A写出所选用物质的化学式:
A: ,
B: 。
(2)写出烧杯中发生反应的离子方程式: 。
把在空气中久置的铝片5.0 g投入盛有 500mL0.5 mol·L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间可用如右的坐标曲线来表示,回答下列问题:
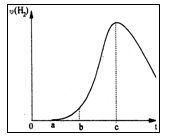
(1)曲线由0→a段不产生氢气的原因___________,有关反应的离子方程式为____________ ;
(2)曲线由a→b段产生氢气的速率较慢的原因___________
有关的化学方程式__________________________;
(3)曲线由b→c段,产生氢气的速率增加较快的主要原因_________________________;
(4)曲线由c以后,产生氢气的速率逐渐下降的主要原因_________________________。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号