浙江省温州市高三上学期返校联考化学试卷
2015年7月31日,中国获得2022年冬奥会主办权,这将促进中国冰雪运动。以下关于冰的说法正确的是
| A.冰与水共存物属于混合物 | B.冰的密度比水大 |
| C.冰与二氧化硅的晶体类型相似 | D.氢键在冰晶体结构中起关键作用 |
下列化学用语中,正确的是
| A.乙炔的结构简式 CHCH |
B.乙醇的比例模型 |
C.NaCl的电子式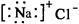 |
D.S原子结构示意图  |
下列说法正确的是
| A.煤的主要组成为苯以及苯的同系物 |
| B.“可燃冰”为水可能变成油提供了有力的证据 |
| C.油脂、淀粉、纤维素、蛋白质都是高分子化合物 |
| D.石油的裂解是使石油分馏产物中的长链烃断裂成乙烯、丙烯等气态短链烃 |
用14C标记的一种C60羧酸衍生物,在特定条件下会断裂DNA抑制艾滋病毒的繁殖。以下有关14C的叙述正确的是
A.与12C60的碳原子化学性质不同 B.与15N含的中子数相同
C.与12C60互为同素异形体 D.与12C、13C互为同系物
用NA表示阿伏加德罗常数,下列叙述正确的是
| A.l mol甲基(-CH3)含有9 NA个电子 |
| B.标准状况下,22.4 L SO3含有的原子数为4NA |
| C.0.10 mol·L-1NaOH溶液中含有OH-离子数是0.1NA |
| D.5.6 g Fe与2.24 L Cl2充分反应转移电子数为0.2NA |
下列关于金属腐蚀的叙述正确的是
| A.金属(M表示金属) 被腐蚀的本质是: M n+ + ne- = M |
| B.金属不可能在碱性环境中发生电化学腐蚀 |
| C.镀锌铁的镀层破损后,镀层仍能对铁起保护作用 |
| D.钢管与外加直流电源的正极相连,以保护它不受腐蚀 |
用0.1000mol·L-1标准NaOH溶液测定食醋中醋酸的含量,下列说法正确的是
| A.酸式滴定管、碱式滴定管及锥形瓶均需洗净后再润洗内壁2~3次 |
| B.可使用酚酞或甲基橙作指示剂 |
| C.滴定过程中眼睛应始终注视滴定管内液面变化 |
| D.读取标准液的刻度时,滴定前平视,滴定后仰视,测定结果偏高 |
下列说法中正确的是
| A.苯使溴水层褪色属于加成反应 |
| B.乙烯与水反应生成乙醇属于水解反应 |
| C.间二甲苯只有一种结构说明苯分子中不存在单双键交替 |
| D.等质量环丁烷(C4H8)和乙烯(C2H4)完全燃烧,消耗的氧气量相等 |
下列褪色现象中,其中一项与其他三项褪色原理不同的是
| A.二氧化硫能使酸性高锰酸钾溶液褪色 |
| B.氯水能使甲基橙褪色 |
| C.浓硝酸能使石蕊试液褪色 |
| D.臭氧能使品红溶液褪色 |
下列用水能鉴别的一组物质是
| A.乙酸乙酯、甘油、硝基苯 | B.乙醇、甘油、四氯化碳 |
| C.乙酸乙酯、苯、乙醇 | D.苯、四氯化碳、硝基苯 |
下列说法正确的是
| A.Cu与石墨都能导电,但都属于非电解质 |
| B.AgCl与BaSO4都是难溶性盐,但都属于强电解质 |
| C.SO2与CaO都是氧化物,因此SO2、CaO都是非电解质 |
| D.NaCl与HCl都是电解质,因此熔融NaCl、液态HCl都能导电 |
原子序数依次增大的四种短周期元素X、Y、Z、M。其中Z是金属元素,X的原子半径小于Y ,Y与M同主族,Y的质子数为M的1/2。下列说法一定正确的是
| A.X与M的原子序数之差为31 |
| B.Y的离子半径小于Z的离子半径 |
| C.由X与Z组成的化合物,可与水反应放出X2 |
| D.由M与Y组成的化合物,其水化物是强酸 |
一定条件下,反应:C(s)+CO2(g) 2CO(g),ΔH>0在2L恒容密闭容器中进行,反应进行20s时,CO的物质的量增加了0.40 mol,则下列说法正确的是
2CO(g),ΔH>0在2L恒容密闭容器中进行,反应进行20s时,CO的物质的量增加了0.40 mol,则下列说法正确的是
A.反应20s,C的平均反应速率v (C) ="0." 005 mol·L-1·s-1
B.反应平衡时,v (CO2): v (CO) =1:2
C.升高温度时,正反应速率增大,逆反应速率减小
D.充入N2使体系压强增大,能提高反应速率
H2O2(l)在有MnO2条件下和无MnO2条件下分解的能量变化如图所示。下列说法正确是
| A.有MnO2条件下的反应曲线是a曲线 |
| B.a曲线变为b曲线,反应的活化分子百分数增大 |
| C.a曲线变为b曲线,平衡时H2O2的转化率增大 |
| D.b曲线的热化学方程式为:H2O2(l) =H2O(l) +1/2O2(g) ΔH= - ( E1 - E2 )KJ•mol-1 |
用pH传感器测得0.10mol·L-1Na2CO3溶液从55℃升高至85℃的pH如图所示。在55℃升高至85℃升温过程中,下列说法正确的是
| A.c(H+)增大,c(OH-)减小 |
| B.c(CO32-)/c(HCO3-)比值不断增大 |
C.c(CO )+c(HCO3-) +c(H2CO3)=0.10 )+c(HCO3-) +c(H2CO3)=0.10 |
| D.c(OH-) - c(HCO3-) - c(H2CO3)=10-11.1 |
为完成相应实验,实验器材(规格和数量不限)足够的一项是
| |
相应实验 |
实验器材(省略夹持装置) |
| A |
氯化钠溶液的浓缩结晶 |
烧杯、玻璃棒、酒精灯 |
| B |
用盐酸除去硫酸钡中的少量碳酸钡 |
烧杯、漏斗、胶头滴管、滤纸 |
| C |
用浓硫酸配制0.5mol·L-1的溶液 |
烧杯、玻璃棒、胶头滴管、容量瓶 |
| D |
用溴水和CCl4除去NaBr溶液中的少量NaI |
烧杯、玻璃棒、胶头滴管、分液漏斗 |
装置(Ⅰ)为铁镍(Fe-Ni)可充电电池:Fe+NiO2+2H2O 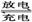 Fe(OH)2+Ni(OH)2;装置(Ⅱ)为电解示意图。当闭合开关K时,Y附近溶液先变红。下列说法正确的是
Fe(OH)2+Ni(OH)2;装置(Ⅱ)为电解示意图。当闭合开关K时,Y附近溶液先变红。下列说法正确的是
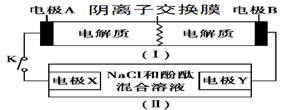
| A.闭合K时,X的电极反应式为:2H++2e-= H2↑ |
| B.闭合K时,A电极反应式为:NiO2+2e-+2H+= Ni(OH)2 |
| C.给装置(Ⅰ)充电时,B极参与反应的物质被氧化 |
| D.给装置(Ⅰ)充电时,OH- 通过阴离子交换膜,移向A电极 |
已知部分弱酸的电离平衡常数如下表:
| 弱酸 |
醋酸 |
次氯酸 |
碳酸 |
亚硫酸 |
| 电离平衡常数(25℃) |
Ka=1.75×10-5 |
Ka=2.98×10-8 |
Ka1=4.30×10-7 Ka2=5.61×10-11 |
Ka1=1.54×10-2 Ka2=1.02×10-7 |
下列离子方程式正确的是
A.少量CO2通入NaClO溶液中:CO2+H2O+2ClO-=CO +2HClO
+2HClO
B.少量的SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO
C.少量的SO2通入Na2CO3溶液中:SO2+H2O+2 CO =SO
=SO +2HCO3-
+2HCO3-
D.相同浓度NaHCO3溶液与NaHSO3溶液等体积混合:H++HCO3-=CO2↑+H2O
某种溶液只含下表离子中的几种(不考虑水的电离与离子水解),且各种离子的物质的量浓度均为0.1 mol·L-1。
| 阳离子 |
K+ NH4+Fe2+Mg2+ Al3+Cu2+ |
| 阴离子 |
OH- Cl- AlO CO CO SO SO SiO SiO |
某同学进行了如下实验(必要时可加热):

下列说法正确的是
A.原溶液中只含有NH4+、Fe2+、Cl-、SO
B.由沉淀A推断原溶液中一定含有SO
C.滤液A中可能含有K+、Al3+、Cl-
D.沉淀B中一定含有Mg(OH)2
(10分)某合成树脂E的单体A(C3H4O2),存在如下转化关系:

已知:①A能使溴的CCl4溶液褪色,又能与碳酸钠溶液反应放出CO2
② ③
③ (X指卤素原子)
(X指卤素原子)
回答下列问题:
(1)A中官能团的名称是 。
(2)A+C→D的化学方程式 。
(3)E的结构简式 。
(4)下列化合物中属于B的同分异构体的是 。
A. B.
B.
C. D.
D.
(5)对于化合物D,下列说法正确的是 。
A.能发生水解反应 B.能与乙酸发生酯化反应
C.不能使酸性KMnO4溶液褪色 D.不能与金属钠反应放出气体
I.请回答:
(1)CO2的电子式 。
(2)钠燃烧不能用CO2灭火,用化学方程式表示其理由 。
(3)重晶石(BaSO4)不溶于酸,用饱和Na2CO3处理转化为易溶于酸的BaCO3,写出反应的离子方程式 。
(4)完成以下氧化还原反应的离子方程式:
( )Cr2O + ( )H2O2+ _____ =( ) Cr3++ ( ) O2 ↑+ ________
+ ( )H2O2+ _____ =( ) Cr3++ ( ) O2 ↑+ ________
II.化合物K3Fe(A2B4)3·3H2O是重要的催化剂。将化合物K3Fe(A2B4)3·3H2O受热完全分解,只得到气体产物和固体产物。经分析,气体产物只有甲、乙和水蒸气。已知甲、乙均由A、B两元素组成,且摩尔质量:M(甲)<M(乙)。A元素的最外层电子数是次外层电子数2倍,B元素的主族序数是其所在周期数的3倍。经分析,固体产物只有Fe、FeO 和K2AB3。某同学再进行以下定量分析。

(1)甲的化学式: 。
(2)溶液②与KMnO4发生氧化还原的离子方程式: 。
(3)由以上实验数据的分析可知n(Fe):n(FeO) :n(K2AB3) = : : 。
(4)某同学认为:溶液②由紫红色变为无色,振荡试样半分钟内不变色,即可证明溶液②与KMnO4溶液反应到达滴定终点。判断该同学设想的合理性并说明理由 。
(14分) 二氧化碳与氢气催化合成甲醇,发生的反应为:CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
(1)已知:
| 化学键 |
H-H |
C-O |
C=O |
H-O |
C-H |
| 键能/kJ·mol-1 |
436 |
326 |
803 |
464 |
414 |
计算上述反应的△H= kJ.mol-1。
(2)一定条件下,将n(CO2):n(H2)=1:1的混合气充入恒温恒容密闭容器中,下列事实可以说明该反应已达平衡的是 (填选项字母)。
A.容器内气体密度保持不变
B.CO2的体积分数保持不变
C.H2O(g)与CO2(g)的生成速率之比为1∶1
D.该反应的平衡常数保持不变
E.混合气体的平均相对分子质量不变
F.容器中压强保持不变
(3)一定条件下,往2L恒容密闭容器中充入1.2molCO2和3.6molH2,在不同催化剂作用下的反应I、反应II与反应III,相同时间内CO2转化率随温度变化的数据如表所示,据表中数据绘制“图1”:
| 相同时间内CO2转化率 |
T1 |
T2 |
T3 |
T4 |
T5 |
| 反应Ⅰ |
65% |
77% |
80% |
80% |
66.67% |
| 反应Ⅱ |
56% |
67% |
76% |
80% |
66.67% |
| 反应Ⅲ |
48% |
62% |
72% |
80% |
66.67% |

(T5时,图1中C点转化率为66.67%,即转化了2/3)
①催化剂效果最佳的反应是 (填“反应I”,“反应II”,“反应III”)。
②T3的b点v(正) v(逆)(填 “>”, “<”, “="”" )。
③T4的a点转化率比T5的c点高的原因是 。
④在温度为T5时,该反应的平衡常数K= 。
⑤在温度为T5时,CH3OH的浓度随时间变化的趋势如“图2”所示。
当时间到达t1时,将生成的甲醇和水同时除去,并维持该温度,在 t2时达新平衡。
请在“图2”中画出t1时刻后CH3OH的浓度变化总趋势曲线。
以下为工业从海水中提取液溴的流程图:

已知:溴的沸点为59℃,微溶于水,有毒性。请回答:
(1)某同学利用“图1”装置进行步骤①至步骤④的实验,当进行步骤①时,应关闭活塞 ,打开活塞 。

(2)步骤②中可根据 现象,简单判断热空气的流速
(3)步骤③中简单判断反应完全的依据是 。
(4)从“溴水混合物Ⅰ”到“溴水混合物Ⅱ”的目的是 。
(5)步骤⑤用“图2”装置进行蒸馏,蒸馏烧瓶中尚未安装温度计,安装其位置时应注意 装置C中直接加热不合理,应改为 ,蒸馏时冷凝水应从 端进入(填“e”或“f”),图中E、F的作用是 、 。

 粤公网安备 44130202000953号
粤公网安备 44130202000953号