硫化汞(HgS)难溶于水,在自然界中呈红褐色,常用于油画颜料、印泥及朱红雕刻漆器等。某温度时HgS在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是( )
| A.向硫化汞的浊液中加入硫化钠溶液,硫化汞的Ksp减小 |
| B.图中a点对应的是饱和溶液 |
| C.向c点的溶液中加入0.1mol/LHg(NO3)2,则c(S2-)减小 |
| D.升高温度可以实现c点到b点的转化 |
常温下,Ksp(CaSO4)=9×10-6,常温下CaSO4在水中的沉淀溶解平衡曲线见图。下列叙述正确的是( )
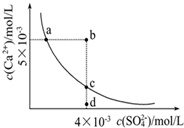
①a、c两点均可以表示CaSO4溶于水所形成的饱和溶液;②a点对应的Ksp不等于c点对应的Ksp;③b点对应的溶液将有沉淀生成;④向d点溶液加入适量的CaCl2固体可以变到c点;⑤d点溶液通过蒸发溶剂可以变到c点;⑥常温下CaSO4溶于水的饱和溶液中,c(Ca2+)与c(SO42-)的乘积对应曲线上任意一点;⑦常温下,向100mL饱和CaSO4溶液中加入400mL0.01mol/L Na2SO4溶液,能使溶液由a点变为b点
| A.2句 | B.3句 | C.4句 | D.5句 |
下列说法正确的是
①用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小;②对于Al(OH)3(s)  Al(OH)3(aq)
Al(OH)3(aq) Al3++3OH-,前者为溶解平衡,后者为电离平衡;③物质的溶解度随温度的升高而增加,物质的溶解都是吸热的;④除去溶液中的Mg2+,用OH-沉淀Mg2+比用CO32-效果好,说明Mg(OH)2的溶解度比MgCO3小;⑤沉淀反应中常加过量的沉淀剂,其目的是使沉淀完全。
Al3++3OH-,前者为溶解平衡,后者为电离平衡;③物质的溶解度随温度的升高而增加,物质的溶解都是吸热的;④除去溶液中的Mg2+,用OH-沉淀Mg2+比用CO32-效果好,说明Mg(OH)2的溶解度比MgCO3小;⑤沉淀反应中常加过量的沉淀剂,其目的是使沉淀完全。
| A.①②④⑤ | B.② | C.①③④⑤ | D.①②⑤ |
向AgCl沉淀中加入过量的KI溶液,白色沉淀转化为黄色沉淀。下列叙述错误的是( )
| A.加入过量的KI溶液充分反应后,Kw(AgCl)减小 |
| B.加入过量的KI溶液充分反应后,溶液中Ag+和I-的浓度之积等于Ksp(AgI) |
| C.加入过量的KI溶液充分反应后,溶液中Ag+和Cl-的浓度之积小于Ksp(AgCl) |
| D.Ksp(AgI)<Ksp(AgCl) |
已知25℃时,几种难溶电解质的溶度积常数Ksp如下表所示:
下列叙述不正确的是
| A.由溶度积常数不能判断相应物质的溶解性大小 |
| B.将等体积的4×10-3 mol/L的AgNO3溶液和4×10-3mol/L K2CrO4溶液混合,有Ag2CrO4沉淀产生 |
| C.向AgCl的悬浊液中滴加饱和NaBr溶液不能得到黄色AgBr |
| D.向100 mL 0.02mol/L的NaSO4溶液中加入100mL0.02mol/L的AgNO3溶液,有白色沉淀生成 |
下列说法正确的是 ( )
| A.某物质的溶解性为难溶,则该物质不溶于水 |
| B.不溶于水的物质的溶解度为0 |
| C.绝对不溶解的物质是不存在的 |
| D.某离子被沉淀完全是指该离子在溶液中的浓度为0 |
已知:Ksp(AgCl)=1.8×10-10;Ksp(Ag2S)=6.3×10-50。向盛0.1mol/L AgNO3溶液的试管中滴加0.1mol/L Na2S溶液至沉淀完全,再滴加足量NaCl溶液,产生的现象或生成的物质是
| A.黑色沉淀完全转化为白色沉淀 | B.既有氯化银也有硫化银 |
| C.只产生黑色硫化银沉淀 | D.只有氯化银白色沉淀 |
某溶液可能含有Clˉ、SO42ˉ、CO32ˉ、NH4+、Fe3+、Al3+和K+。取该溶液200mL,加入过量浓NaOH溶液,加热,得到448mL气体(标准状况下测定),同时产生红褐色沉淀;过滤,洗涤,灼烧,得到3.2g固体;向上述滤液中加足量BaCl2溶液,得到9.32g不溶于盐酸的沉淀。由此可知原溶液中
| A.至少存在5种离子 |
| B.SO42ˉ、NH4+一定存在,Clˉ可能不存在 |
| C.Clˉ一定存在,且c(Clˉ)≥0.3mol/L |
| D.CO32ˉ、Al3+一定不存在,K+可能存在 |
下列溶液均处于 25℃,有关叙述正确的是
| A.AgCl 在同浓度的CaCl2 和NaCl溶液中的溶解度相同 |
| B.0.1 mol∙L-1的Na2S溶液中,c(OH-)=c(H+)+c(HS-)+c(H2S) |
| C.含有 NH4+、Cl-、H+、OH-的溶液中,其离子浓度一定是:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| D.pH=4.5的番茄汁中 c(H+) 是 pH=6.5 的牛奶中 c(H+)的 100 倍 |
向盛有0.1mol/LAgNO3溶液的试管中滴加 0.05mol/LNa2S溶液至沉淀完全,再向上层清液中滴加足量 NaCl,产生的现象及发生的反应是
| A.黑色沉淀完全转化为白色沉淀 | B.既有Ag2S也有 AgCl |
| C.不能由黑色沉淀转变为白色沉淀 | D.只有 AgCl白色沉淀 |
下图表示的是难溶氢氧化物在不同pH下的溶解度(S/mol·L-1),下列说法中正确的是( )

| A.pH=3时溶液中铁元素的主要存在形式是Fe3+ |
| B.若Ni(NO3)2溶液中含有少量的Co2+杂质,可通过调节溶液pH的方法来除去 |
| C.若分离溶液中的Fe3+和Cu2+,可调节溶液的pH在4左右 |
| D.若在含有Cu2+和Ni2+的溶液中加入烧碱,Ni(OH)2优先沉淀 |
某溶液中含有KCl、KBr、K2CrO4,浓度均为0.01mol/L,已知Ksp(AgCl)=1.77×10-10,Ksp(AgBr)=5.35×10-13,Ksp(Ag2CrO4)=1.12×10-12,向溶液中逐滴加入0.01mol/LAgNO3溶液时,最先产生沉淀的是( )
| A.AgCl | B.AgBr | C.Ag2CrO4 | D.同时沉淀 |
饱和石灰水中存在溶解平衡:Ca(OH)2(s)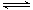 Ca2+(aq)+2OH-(aq),向其中加入少量生石灰,充分反应后恢复至原温度,则下列说法中不正确的是( )
Ca2+(aq)+2OH-(aq),向其中加入少量生石灰,充分反应后恢复至原温度,则下列说法中不正确的是( )
| A.溶液的pH不变 | B.溶液中Ca2+的浓度减小 |
| C.溶液中OH-的数目减小 | D.容器中固体的质量增加 |
常温下,Ksp(CaSO4)=9×10-6,常温下CaSO4在水溶液中的沉淀溶解平衡曲线见右图。下列说法不正确的是
| A.CaSO4溶解在水中,c(Ca2+)=c(SO42-) = 3×10-3mol/L |
| B.在d点溶液中加入一定量的CaCl2可能会有沉淀析出 |
| C.a点对应的Ksp等于c点对应的Ksp |
| D.b点将有沉淀生成,平衡后溶液中c(SO42-)等于3×10-3mol/L |