反应A+3B==2C+D在某段时间内以A的浓度变化表示的反应速率为1 mol·L-1·min-1,则此段时间内以C的浓度变化表示的化学反应速率为( )
| A.0.5 mol·L-1·min-1 | B.1 mol·L-1·min-1 |
| C.2 mol·L-1·min-1 | D.3 mol·L-1·min-1 |
用纯净的碳酸钙与稀盐酸反应制取二氧化碳气体,请回答:
(1)实验过程如下图所示,分析判断:________段化学反应速率最快,_____段收集的二氧化碳气体最多。
(2)试分析三个时间段里,反应速率不同的可能原因(该反应是放热反应)。
(3)为了减缓上述反应的速率,欲向溶液中加入下列物质,你认为可行的是
| A.蒸馏水 | B.氯化钠固体 | C.氯化钠溶液 | D.浓盐酸 |
COCl2(g)  CO(g)+Cl2(g) △H>0,当反应达到平衡时,下列措施①升温②恒容通入惰性气体③增加CO的浓度④减压⑤加催化剂⑥恒压时通入惰性气体,能提高COCl2转化率的是( )
CO(g)+Cl2(g) △H>0,当反应达到平衡时,下列措施①升温②恒容通入惰性气体③增加CO的浓度④减压⑤加催化剂⑥恒压时通入惰性气体,能提高COCl2转化率的是( )
| A.①②④ | B.①④⑥ | C.②③⑥ | D.③⑤⑥ |
下列四个数据是在不同条件下测出的合成氨反应的速率,其中最快是
| A.v(H2)="=0.1" mol/(L·min) | B.v(N2)==0.1mol/(L·min) |
| C.v(NH3)==0.15mol/(L·min) | D.v(N2)==0.02mol/(L·s) |
(1)反应A(g)+B(s) C(g);△H<0,在其他条件不变时,改变其中一个条件,则生成C的速率:
C(g);△H<0,在其他条件不变时,改变其中一个条件,则生成C的速率:
①升温___ ;②增大压强____ ;③增大容器容积____ ;
④加入A___ ; ⑤加入B____ ; ⑥加正催化剂____ 。
(2)在25℃、101kPa下,1g甲烷燃烧生成CO2和液态水时放热55.6kJ。则表示甲烷燃烧热的热化学方程式为___________________________________________。
(3)北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6),丙烷脱氢可得丙烯。
已知:C3H8(g) CH4(g)+HC
CH4(g)+HC CH(g)+H2(g) △H1="156.6" kJ·mol-1
CH(g)+H2(g) △H1="156.6" kJ·mol-1
CH3CH CH2(g)
CH2(g) CH4(g)+HC
CH4(g)+HC CH(g ) △H2="32.4" kJ·mol-1
CH(g ) △H2="32.4" kJ·mol-1
则相同条件下,反应C3H8(g) CH3CH
CH3CH CH2(g)+H2(g) 的△H= kJ·mol-1。
CH2(g)+H2(g) 的△H= kJ·mol-1。
(4)下表中的数据表示破坏1 mol化学键需消耗的能量(即键能,单位为kJ·mol-1):
| 化学键 |
C—H |
C—F |
H—F |
F—F |
| 键能 |
414 |
489 |
565 |
158 |
根据键能数据计算以下反应的反应热△H:
CH4(g)+4F2(g)﹦CF4(g)+4HF(g) △H=______________________
在2L密闭容器内,某气体反应物在2s内由8mol变为7.2mol,则该反应的平均反应速率为()
| A.0.4mol/(L·s) | B.0.3mol/(L·s) | C.0.2mol/(L·s) | D.0.1mol/(L·s) |
在N2+3H2 2NH3的反应中,在5s中NH3的浓度变化了8mol/L。则NH3的平均反应速率
2NH3的反应中,在5s中NH3的浓度变化了8mol/L。则NH3的平均反应速率
| A.2.4 mol/(L·s) | B.0.8mol/(L·s) |
| C.1.6 mol/(L·s) | D.0.08 mol/(L·s) |
在一个容积为2L的密闭容器中,发生如下反应:3A + B  2C (A、B、C均为气体),若最初加入的A、B都是4 mol,A的平均反应速率为0.12 mol/(L·s),则10s后容器中的B是
2C (A、B、C均为气体),若最初加入的A、B都是4 mol,A的平均反应速率为0.12 mol/(L·s),则10s后容器中的B是
A、2.8 mol B、3.2mol C、1.6 mol D、3.6 mol
反应4NH3(g) + 5O2(g) 4NO(g) + 6H2O(g)在5L密闭容器中进行,半分钟后,NO的物质的量增加了0.3mol,则表示此反应的速率正确的是( )
4NO(g) + 6H2O(g)在5L密闭容器中进行,半分钟后,NO的物质的量增加了0.3mol,则表示此反应的速率正确的是( )
| A.v (O2) = 0.01mol·(L·s) –1 | B.v (NO) =" 0.008mol·(L·s)" –1 |
| C.v (H2O) =" 0.003mol·(L·s)" –1 | D.v (NH3) =" 0.02mol·(L·s)" –1 |
将5.6 g铁粉投入盛有100 mL 2 mol/L稀硫酸的烧杯中,2 min时铁粉刚好溶解完全。如果反应前后溶液的体积不变,则该反应的平均速率可表示为
| A.v(Fe)="0.05" mol/(L·min) | B.v(H2SO4)="1" mol/(L·min) |
| C.v(H2)="0.5" mol/(L·min) | D.v(FeSO4)="0.5" mol/(L·min) |
随着世界粮食需求量的增长,农业对化学肥料的需求量越来越大,其中氮肥是需求量最大的一种化肥。而氨的合成为氮肥的生产工业奠定了基础,其原理为:N2+3H2 2NH3
2NH3
(1)在N2+3H2 2NH3的反应中,一段时间后,NH3的浓度增加了0.9mol·L-1。用N2表示其反应速率为0.15 mol·L-1·s-1,则所经过的时间为 ;
2NH3的反应中,一段时间后,NH3的浓度增加了0.9mol·L-1。用N2表示其反应速率为0.15 mol·L-1·s-1,则所经过的时间为 ;
A.2 s B.3 s C.4 s D.6 s
(2)下列4个数据是在不同条件下测得的合成氨反应的速率,其中反应最快的是 ;
A.v(H2)=0.1 mol·L-1·min-1 B.v(N2)=0.1 mol·L-1·min-1
C.v(NH3)=0.15 mol·L-1·min-1 D.v(N2)=0.002mol·L-1·min-1
(3)在一个绝热、容积不变的密闭容器中发生可逆反应:N2(g)+3H2(g) 2NH3(g) △H<0。下列各项能说明该反应已经达到平衡状态的是 。
2NH3(g) △H<0。下列各项能说明该反应已经达到平衡状态的是 。
A.容器内气体密度保持不变
B.容器内温度不再变化
C.断裂1mol N≡N键的同时,断裂6 mol N—H键
D.反应消耗N2、H2与产生NH3的速率之比1︰3︰2
把0.6molX气体和0.4molY气体混合于2L容器中,使它们发生如下反应:
3X(气) + Y(气) = nZ(气) + 2W(气) 5min末已生成0.2molW,若测知以Z浓度变化来表示的反应平均速率为0.01mol/(L·min)求:
(1)反应中Z气体的计量数n;
(2)反应在5分钟末时,Y的转化率。
把在空气中久置的铝片5.0 g投入盛有500 mL 0.5 mol·L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间的关系可用如图曲线来表示,回答下列问题: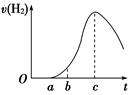
(1)曲线由O →a段不产生氢气的原因是____________________________________________________________;
有关反应的化学方程式为
__________________________________________________;
(2)曲线a→c段,产生氢气的速率增加较快的主要原因是
________________________________________________________________________
________________________________________________________________________;
(3)曲线由c以后,产生氢气的速率逐渐下降的主要原因是_________________________;
(4)该反应若使用催化剂,可使H2产量增多吗?______(填“会”或“不会”)。
某温度时,在5 L的容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。请通过计算回答下列问题。
(1)反应开始至2 min,Y的平均反应速率为 ;
(2)分析有关数据,写出X、Y、Z的反应方程式:
;
(3)反应达到最大限度时,Y的转化率为 。