用NA表示阿伏加德罗数的值。下列叙述正确的是
| A.电解饱和食盐水,当阴极产生2.24L H2时,转移的电子数一定为0.2NA |
| B.0.1mol Fe在0.1mol Cl2中充分燃烧,转移的电子数为0.3NA |
| C.室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA |
| D.常温下,1 L 0.1 mol·L-1的NH4NO3溶液中氧原子数为0.3 NA |
氯气是一种重要的工业原料。
Ⅰ.实验室可用二氧化锰和浓盐酸反应制取氯气,反应的化学方程式是 。
Ⅱ.某研究性学习小组查阅资料得知,漂白粉与硫酸反应可制取氯气,化学方程式为:
Ca(ClO)2+CaCl2+2H2SO4  2CaSO4+2Cl2↑+2H2O
2CaSO4+2Cl2↑+2H2O
他们利用该反应设计如下制取氯气并验证其性质的实验。
(1)回答下列问题:(1)该实验中A部分的装置是 (填标号) 。
(2)请你帮助他们设计一个实验,证明洗气瓶C中的Na2SO3已被氧化(简述实验步骤): 。
(3)写出D装置中发生反应的离子方程式 (4)该实验存在明显的缺陷,请你提出改进的方法 。
(5)该小组又进行了如下实验:称取漂白粉2.0 g,研磨后溶解,配制成250 mL溶液,取出25 mL加入到锥形瓶中,再加入过量的KI溶液和过量的H2SO4溶液,静置。待完全反应后,用0.1 mol·L−1的Na2S2O3溶液作标准液滴定反应生成的碘,已知反应方程式为:2Na2S2O3+I2 === Na2S4O6+2NaI,共用去Na2S2O3溶液20.0 mL。则该漂白粉中Ca(ClO)2的质量分数为 。
CuCO3和Cu2(OH)2CO3的混合物34.6 g,可恰好完全溶解于300mL、
2 mol·L-1的盐酸溶液中,若加热分解等量的这种混合物可得CuO固体质量为( )
| A.16.0 g | B.19.2 g | C.24.0 g | D.30.6 g |
设NA为阿伏伽德罗常数的值。下列叙述正确的是( )
| A.18gNH+4中含有的电子数为10NA |
| B.78gNa2O2固体中含有的阴离子数为2NA |
| C.1L0.1 mol/L醋酸溶液中含有的氢离子数为0.1NA |
| D.标准状况下,2.24L苯含有分子的数目为0.1NA |
把7.4 g Na2CO3·10H2O和NaHCO3组成的固体混合物溶于水配成100 mL溶液,其中c(Na+)="0.6" mol·L-1。若把等质量的固体混合物加热至恒重,残留固体的质量是( )。
| A.3.18 g | B.2.12 g | C.4.22 g | D.5.28 g |
用向下排气法在容积为VmL的集气瓶中收集氨气。由于空气未排完,最后瓶内气体的平均相对分子质量为19。将此盛满气体的集气瓶倒置于水中,瓶内水面上升到一定高度后即停止上升。则在同温同压下,瓶内剩余气体的体积为( )
| A.V/4mL | B.1/5mL | C.V/6mL | D.无法判断 |
下列叙述正确的是
A.1 mol N 参加氧化还原反应时电子转移数为3×6.02×10 参加氧化还原反应时电子转移数为3×6.02×10 |
B.16g O 所含氧原子个数为6.02×10 所含氧原子个数为6.02×10 |
C.物质的量浓度为0.5 mol·L 的MgCl 的MgCl 溶液,含有的Cl 溶液,含有的Cl 数为6.02×10 数为6.02×10 |
D.常温常压下,22.4L SO 含分子的个数为6.02×10 含分子的个数为6.02×10 |
有体积相同的两份营养液,其配方如下:
| |
KCl |
K2SO4 |
ZnSO4 |
ZnCl2 |
| 第一份 |
0.3 mol |
0.2 mol |
0.1 mol |
—— |
| 第二份 |
0.1 mol |
0.3 mol |
—— |
0.1 mol |
两份营养液中各离子浓度
A. 完全不同 B. 完全相同 C. 仅c(K )相同 D. 仅c(Cl
)相同 D. 仅c(Cl )相同
)相同
下列条件下,两种气体分子数一定不相等的是
A.相同质量、不同密度的N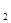 O和CO O和CO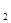 |
B.相同体积、相同密度的CO和C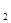 H H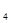 |
C.相同温度、相同压强、相同体积的O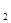 和O 和O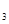 |
D.相同压强、相同体积、相同质量的NO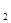 和N 和N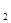 O O |
有Al、CuO、Fe2O3组成的混合物共10.0 g,放入1000 mL某浓度的盐酸溶液中,混合物完全溶解,当再加入250 mL 2.0 mol/L的NaOH溶液时,得到的沉淀最多。上述盐酸溶液的液度为( )
| A.0.5 mol/L | B.1.0 mol/L | C.2.0 mol/L | D.3.0 mol/L |
设NA代表阿伏加德罗常数的数值,下列说法正确的是( )
| A.钠在氧气中燃烧生成1mol 物质时转移电子数为4 NA |
| B.标准状况 下22.4升的SO3中所含分子数为NA |
| C.16 g O2和O3的混合气体在常温下所含的氧原子数为NA |
| D.1mol·L-1 CuCl2溶液中含氯离子数为0.2 NA |
某风景区被称为天然氧吧,其原因是空气中的自由电子附着在分子或原子上形成空气负离子,被称为“空气维生素”。  就是一种空气负离子,其摩尔质量为 ( )
就是一种空气负离子,其摩尔质量为 ( )
| A.32 g | B.33 g | C.32 g·mol-1 | D.33 g·mol-1 |
3.84 g Fe和Fe2O3的混合物溶于过量盐酸中,生成0.03 mol H2,反应后的溶液中加入KSCN溶液检验,溶液不显红色。求原混合物中Fe2O3的质量。
向m g镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体b L。向反应后的溶液中加入c mol/L氢氧化钾溶液V mL,使金属离子刚好沉淀完全,得到的沉淀质量为n g。再将得到的沉淀灼烧至质量不再改变为止,得到固体p g。则下列关系不正确的是( )