在化学学习中使用数轴的表示方法可收到直观、形象的效果,下列表达中正确的是
A.分散质微粒的大小与分散系种类的关系: |
B.常温下溶液的pH其酸碱性的关系: |
C.硫的化合物中化合价与其氧化性、还原性的关系: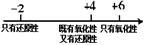 |
D.Fe在Cl2中燃烧的产物与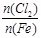 的关系: 的关系: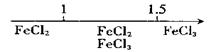 |
把由NaOH、AlCl3、MgCl2三种固体组成的混合物溶于足量水中,有0.58克白色沉淀,在所得的浊液中逐渐加入0.5mol/L盐酸,加入盐酸的体积与生成沉淀的质量关系如下图所示 。
回答下列问题:
①混合物中NaOH质量为 ; ②混合物中AlCl3的物质的量为 ;
③混合物中MgCl2的物质的量为 ;④P点所示的盐酸体积为 。
下图为一定量AlCl3溶液中加入NaOH溶液后,产生Al(OH)3白色沉淀的质量与NaOH的物质的量之间的关系曲线。试回答:
(1)B点时已参加反应的AlCl3和NaOH的物质的量之比为_______。
(2)写出下列曲线代表的离子反应方程式:
OA段 ____________________________,
AB段 ____________________________。
(3)向B处生成的溶液中通入二氧化碳,可见到的现象是_________________。
实验室用18.4 mol·L-1的浓硫酸来配制500mL 0.2 mol·L-1的稀硫酸。
(1)所需仪器除了玻璃棒、烧杯、胶头滴管、量筒外,还需要哪个仪器才能完成该实验,请写出: 。
(2)计算所需浓硫酸的体积为________ mL 。现有①10mL ②50mL ③100mL三种规格的量筒,应当选用___________。(填序号)
(3)实验中两次用到玻璃棒,其作用分别是:___________、__________。
(4)下列对容量瓶及其使用方法的描述中正确的是_____。
| A.容量瓶上标有容积、温度和浓度 |
| B.容量瓶用蒸馏水洗净后,必须烘干 |
| C.配制溶液时,把量好的浓硫酸小心倒入容量瓶中,加入蒸馏水到接近刻度线 1~2 cm处,改用胶头滴管加蒸馏水至刻度线 |
| D.使用前要检查容量瓶是否漏水 |
(5)在配制过程中,下列操作可引起所配溶液浓度偏低的有_______。(填序号)
①未洗涤稀释浓硫酸时用过的烧杯和玻璃棒。
②未等稀释后的硫酸溶液冷却至室温就转移到容量瓶中。
③转移前,容量瓶中含有少量蒸馏水。
④定容时,仰视刻度线。
某溶液中只含有K+, Fe3+, Cl-,SO42-四种离子,已知K+, Fe3+, Cl-的个数比为3:2:1。则溶液中Fe3+与SO42-离子的个数比为( )
| A.1:2 | B.1:4 | C.3:4 | D.3:2 |
设 NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A.NA个CH4分子的质量为16g/mol |
| B.1mol/LNaCl溶液含有NA个Na+ |
| C.等物质的量的N2和CO所含分子数、原子个数、电子总数均相同 |
| D.22.4LCO2中含有 NA个CO2分子 |
下列溶液中含Cl-物质的量浓度最大的是( )
| A.10mL 0.1mol·L-1的氯化钙溶液 | B.5mL 0.1mol·L-1的氯化铝溶液 |
| C.30mL 0.2mol·L-1的氯化钾溶液 | D.40mL 0.25mol·L-1的氯化钠溶液 |
设NA为阿伏加德罗常数,下面叙述正确的是 ( )
| A.标准状况下,11.2L SO3所含分子数为0.5 NA |
| B.1L 1mol/L的氯化钠溶液中,所含离子数为NA |
| C.常温下,4.4g CO2和N2O(不反应)混合物中所含有的原子数为0.3 NA |
| D.一定量的铜与足量的浓硫酸反应,放出2.24L气体时,转移电子数为0.2 NA |
(9分)填写下列表格:
| 物质 |
分子数 |
质量/g |
物质的量/mol |
摩尔质量/ g·mol -1 |
| 氮气 |
|
14 |
|
|
| H2SO4 |
3.01×1023 |
|
|
|
| H2O |
|
|
2 |
|
下列溶液中的Cl-浓度与50 mL 1 mol / L MgCl2溶液中的Cl-浓度相等的是
| A.100 mL 1 mol / L NaCl溶液 | B.75 mL 1 mol / LCaCl2溶液 |
| C.150 mL 3 mol / LKCl溶液 | D.50 mL 2 mol / L AlCl3溶液 |
用固体NaOH配制一定物质的量浓度的NaOH溶液,下列操作正确的是
| A.称量时,将固体NaOH直接放在天平左盘上 |
| B.将称量好的固体NaOH放入容量瓶中,加蒸馏水溶解 |
| C.定容时如果加水超过了刻度线,用胶头滴管直接吸出多余部分 |
| D.将烧杯中溶解固体NaOH所得溶液,冷却到室温后转移至容量瓶中 |
下列说法正确的是
| A.摩尔质量就等于物质的相对分子质量 |
| B.摩尔质量就是物质相对分子质量的6.02×1023倍 |
| C.HNO3的摩尔质量是63g |
| D.硫酸和磷酸(H3PO4)的摩尔质量相等 |
某人体检结果中显示其甘油三酯指标为0.52 mmol/L,这里表示甘油三酯指标的物理量是
| A.物质的量 | B.物质的量浓度 | C.质量分数 | D.摩尔质量 |