用6.02×1023表示阿伏加德罗常数的值,下列说法中正确的是
| A.常温常压下,1.6 g臭氧中含有6.02×1022个氧原子 |
| B.标准状况下,2.24 L水中含有6.02×1022个水分子 |
| C.2.24 L氨气分子中含6.02×1023个电子 |
| D.2.4 g金属镁变为镁离子时失去6.02×1022个电子 |
设阿伏加德罗常数的值为NA,下列说法中正确的是:
| A.标准状况下,2.24LCHCl3含有的分子数为0.1NA |
| B.2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA |
| C.0.1molCnH2n+2中含有的C-C键数为0.1nNA |
| D.1mol苯乙烯中含有的C=C数为4NA |
在标准状况下,将a L NH3完全溶于水得到V mL氨水,溶液的密度为ρ g/cm3,溶质的质量分数为w,溶质的物质的量浓度为c mol/L。下列叙述中正确的是( )
①w=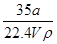 ×100%
×100%
②c=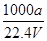
③向上述溶液中再加入V mL水后,所得溶液的质量分数大于0.5 w
④向上述溶液中再加入1.5V mL同浓度稀盐酸,充分反应后溶液中离子浓度大小关系为:
c(Cl-)> c(NH )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
| A.①③ | B.②③ | C.②④ | D.①④ |
现有下列化学仪器与用品:①玻璃棒 ②烧杯 ③托盘天平 ④量筒 ⑤药匙 ⑥胶头滴管 ⑦容量瓶 ⑧标签纸 ⑨细口试剂瓶
Ⅰ.称量:若需要配制500 mL 0.622 moL / L NaOH溶液,则应称取固体NaOH g;
Ⅱ.用以上称量后的NaOH固体配制溶液并备用:按配制溶液的过程顺序,从上述所给仪器和用品中选取需要的仪器(重复的不计),其编号排列是 ;
Ⅲ.配制过程中,应将固体NaOH溶解后并冷却至室温的溶液转移到 中,在转移时玻璃棒起 作用;在液面接近容量瓶刻度线 处,改用 定容。
Ⅳ.若实验中遇到下列情况,可能导致溶液浓度偏高的是 (填字母):
| A.固体氢氧化钠溶解时未冷却至室温,就开始转移、洗涤以及定容; |
| B.转移时不小心有少量溶液流到了容量瓶外; |
| C.定容时仰视容量瓶刻度线; |
| D.定容时加水超过了刻度线,马上用胶头滴管吸去多余的水。 |
E、配制好后,发现称量时所用的托盘天平的砝码生锈了
Ⅰ.H2SO4的摩尔质量为 ;0.3mol的CO(NH2)2中含有 个电子(用NA表示);
Ⅱ.①标准状况下22.4 L CH4 ②1.5 mol NH3 ③1.806 x1024个H2O④标准状况下73g HCl所含H原子个数由多到少的顺序为 (填序号);在含0.4 mol Al2(SO4)3的溶液中SO42—的物质的量为 ;
Ⅲ.某常见气体在标准状况下的密度为1.25g/L,若该气体的分子式为A2型,则其名称是 ;该气体在一定条件下可与氢气反应生成氨气,试写出该反应的化学方程式 ;
Ⅳ.取100 mL a mol / L HCl溶液与300 mL n mol / L H2SO4溶液均注入到500 mL的容量瓶中,加水稀释到刻度线,则该混合溶液中H+ 的物质的量浓度为 mol / L;
配制250mL 0.1mol/L 的盐酸溶液时,下列实验操作使配制溶液的浓度偏小的是( )
| A.用量筒量取所需的浓盐酸时俯视刻度线 |
| B.定容时,俯视刻度线 |
| C.用量筒量取所需浓盐酸倒入烧杯后,用水洗涤量筒2~~3次,洗涤液倒入烧杯中 |
| D.定容后倒转容量瓶几次,发现凹液面最低点低于刻度线,可以不管它。 |
标准状况下,10 g由CO和CO2组成的混合气体的体积为 6.72 L,则混合气体中CO和CO2的物质的量之比是
| A.2:1 | B.2:3 | C.4:3 | D.1:1 |
用NA表示阿伏加德罗常数的值,下列说法正确的是
| A.常温常压下,5.6 L一氧化碳和5.6 L氧气混合后的分子总数为0.5NA |
| B.标准状况下,5.6 L N2和16.8L NO混合气体中的原子数为2NA |
| C.标准状况下,22.4L H2O中分子数为NA |
| D.常温常压下,1 mol氦气含有的原子数为2NA |
下列溶液中,c( Cl— )与50mL 1mol/L AlCl3溶液中c(Cl— )相等的是
| A.150mL 1mol/L 的NaCl溶液 | B.75mL 2mol/L的NH4Cl溶液 |
| C.100mL 1.5mol/L的KCl溶液 | D.75mL 1mol/L的FeCl3溶液 |
NA表示阿伏加德罗常数,下列判断错误的是
| A.常温下,22 g CO2中含有NA个氧原子 |
| B.1 mol/L CaCl2溶液中Cl— 的数目等于2NA |
| C.标准状况下,33.6LCH4中含H原子数为6NA |
| D.1 mol Na 完全反应时,失去NA个电子 |
下列说法中正确的是
| A.摩尔既是物质的数量单位又是物质的质量单位 |
| B.阿伏加德罗常数是12 kg 12C中含有的碳原子数 |
| C.1 mol H2O分子中含有10 mol电子 |
| D.一个NO分子的质量是a g,一个NO2分子的质量b g,氧原子的摩尔质量是(b-a) g•mol-1 |
NA为阿伏加德罗常数的值。下列说法中,正确的是
| A.标准状况下,22.4L庚烷的分子数约为NA |
| B.密闭容器中23gNO2与N2O4的混合气体中氮原子数为0.5NA |
| C.过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.4NA |
| D.1L0.1mol·L-1的NaHCO3溶液中HCO3-和CO32-离子数之和为0.1NA |
有某温度下KCl饱和溶液m1 g,溶质质量分数为ω1%。对其蒸发结晶或降温结晶,若析出KCl的质量、所得母液质量及溶质质量分数用m g、m2 g和ω2%表示,分析正确的是
| A.原条件下KCl的溶解度小于ω1 g | B. m1∙ω1%- m = m2∙ω2% |
| C.ω1一定大于ω2 | D. m1 - m2 ≤ m |