1mol/L NaOH溶液的含义是
| A.1L溶液中含有1mol NaOH | B.溶液中含有1mol NaOH |
| C.1L水中含有1mol NaOH | D.将40克NaOH溶于1L水中所得的溶液 |
已知Ksp(AB2)=4.2×10-8,Ksp(AC)=3.0×10-15。在AB2、AC均为饱和的混合液中,测得c(B-)=1.6×10-3 mol·L-1,则溶液中c(C2-)为
A. 7.3×10-13 mol·L-1 B. 1.8×10-13 mol·L-1
C.2.3 mol·L-1 D.3.7 mol·L-1
设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.1mol FeI2与足量氯气反应时转移的电子数为2NA |
B.室温下,14.0g分子通式为CnH2n烯烃中含有的碳碳双键数目为 |
| C.标准状况下,5.6L O2与适量Na加热反应,转移的电子数一定为NA |
| D.氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA |
常温常压下二氧化碳和过氧化钠反应后得到碳酸钠和氧气,若反应中固体质量增加了28g,反应中有关物质的物理量正确的是(NA表示阿伏加德罗常数)
| A.参与反应的过氧化钠中含阴离子2 mol |
| B.参与反应的二氧化碳的体积为22.4 L |
| C.反应中电子转移的数目为NA个 |
| D.将生成的碳酸钠溶解在1L水中,能得到1mol/L的碳酸钠溶液 |
实验室中配制250mL 0.5mo1/L盐酸时,不需要用到的仪器是( )




| A.酒精灯 | B.玻璃棒 | C.容量瓶 | D.胶头滴管 |
下列叙述正确的是 ( )
| A.1 mol任何气体的气体摩尔体积都约为22.4 L/mol |
| B.常温常压下,11.2LO3中所含氧原子个数等于1.5NA |
| C.标准状况下,1mol CCl4所占的体积约为22.4L |
| D.同温、同压下,相同体积的一氧化碳和二氧化碳的质量比为7:11 |
下列说法正确的是( )
| A.硫酸的摩尔质量是98g |
| B.铁原子的摩尔质量等于铁的相对原子质量 |
| C.标准状况下,任何物质的摩尔体积都约是22.4L |
| D.1mol氧气的质量为32g |
小明体检的血液化验单中,葡萄糖为5.9×10﹣3mol/L.表示该体检指标的物理量是( )
| A.溶解度(s) | B.物质的量浓度(c) |
| C.质量分数(w) | D.摩尔质量(M) |
实验室中需要配制1mol/L的NaCl溶液970mL,配制时应选用的容量瓶的规格是
| A.950mL 容量瓶 | B.500mL容量瓶 |
| C.1000mL 容量瓶 | D.任意规格的容量瓶 |
4 mol·L-1的KOH溶液100mL,取出5mL,这5mL溶液中K+浓度为:
| A.4 mol·L-1 | B.0.2mol·L-1 | C.2 mol·L-1 | D.0.4 mol·L-1 |
下列说法正确的是
| A.1 mol氧为32 g |
| B.标准状况下,1 mol H2和O2的混合气体的体积约为22.4 L |
| C.CO2的摩尔质量为44 |
| D.2 mol·L-1的BaCl2溶液中含Cl-的个数为2.408×1024 |
镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系
如右图。反应中镁和铝的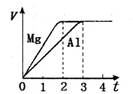
| A.物质的量之比为3:2 | B.质量之比为2:3 |
| C.摩尔质量之比为2:3 | D.反应速率之比为3:2 |