(1)在一定条件下,容积为 10L密闭容器中发生反应:CH4(g)+H2O(g)  CO(g)+3H2(g);ΔH>0,将1.0 mol CH4和2.0 mol H2O(g)通入该密闭容器10 min时有0.1 mol CO生成,则10 min内该反应的平均速率υ(H2) 。
CO(g)+3H2(g);ΔH>0,将1.0 mol CH4和2.0 mol H2O(g)通入该密闭容器10 min时有0.1 mol CO生成,则10 min内该反应的平均速率υ(H2) 。
(2)在压强为0.1 MPa条件下,容积为V L某密闭容器中a mol CO与2a mol H2在催化剂作用下反应生成甲醇: CO(g)+2H2(g)  CH3OH(g) 平衡时CO的转化率与温度、压强的关系如图。
CH3OH(g) 平衡时CO的转化率与温度、压强的关系如图。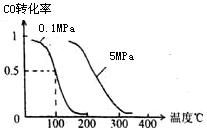
①该反应的△H 0 (填“<”、“>”或“=”)。
②100℃时该反应的平衡常数K= (用含a、V的代数式表示)。
③在温度容积不变的情况下,向该密闭容器再增加a mol CO与 2a mol H2,达到新平衡时,CO的转化率 (填“增大”、“减小”或“不变”)。平衡常数 (填“增大”、“减小”或“不变”)
④在某温度下,向一个容积不变的密闭容器中通入2.5mol CO和7.5mol H2反应生成CH3OH(g),达到平衡时CO的转化率为80%,此时容器内的压强为开始时的 倍。
1000℃时,硫酸钠可与氢气发生反应: Na2SO4(s)+4H2(g)  Na2S(s)+4H2O(g)。请回答下列问题:
Na2S(s)+4H2O(g)。请回答下列问题:
(1)上述反应的平衡常数表达式为: 。
(2)上述反应在三个不同条件下进行,与曲线a比较,b和c分别仅改变一种反应条件,其中H2的浓度随时间的变化如图所示。
①则曲线b改变的条件为
②该反应的△H___0(填“>”、“<”或“=”)。
(3)该温度下,向2 L盛有1.42 g Na2SO4的密闭恒容容器中通入H2,5 min
后测得固体质量为1.10 g。
①则该时间范围内的平均反应速率v(H2)= 。
②能说明该反应已达到平衡状态的是 (填字母,下同)。
| A.容器内压强保持不变 | B.容器内气体密度保持不变 |
| C.c(H2)=c(H2O) | D.v正(H2)=v逆(H2O) |
已知一定温度和压强下,在容积为VL的密闭容器中充入1mol A和1mol B,保持恒温恒压下反应:A(g) + B(g)  C(g),△H<0。达到平衡时,C的体积分数为40%。试回答有关问题:
C(g),△H<0。达到平衡时,C的体积分数为40%。试回答有关问题:
(1)升温时,C的反应速率_______(填“加快”、“减慢”或“不变”)
(2)若平衡时,保持容器容积不变,使容器内压强增大,则平衡_______
| A.一定向正反应方向移动 | B.一定向逆反应方向移动 |
| C.一定不移动 | D.不一定移动 |
(3)若使温度、压强在上述条件下恒定不变,在密闭容器中充入2mol A和2 mol B,则反应达到平衡时,C的体积分数为_____ ;容器的容积为____ (请写出计算过程)
(12分)现有反应:mA(g)+nB(g) pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
(1)该反应的逆反应为_________热反应,且m +n ________ p(填“>”“=”“<”)。
(2)减压时,A的质量分数_________。(填“增大”“减小”或“不变”,下同)
(3)若加入B(体积不变),则A的转化率__________。
(4)若升高温度,则平衡时B、C的浓度之比 将_________。
将_________。
(5)若B是有色物质,A、C均无色,则加入C(体积不变)时混合物颜色_______ (填“变深”“变浅”或“不变”)。
在密闭容器中,将1.0molCO与1.0molH2O混合加热到800℃,发生下列反应:CO(g)+H2O(g) CO2(g)+H2(g),一段时间后该反应达到平衡,测得CO的物质的量为0.5mol.求:
CO2(g)+H2(g),一段时间后该反应达到平衡,测得CO的物质的量为0.5mol.求:
(1)达到平衡时CO2的物质的量分数为 ,该反应的化学平衡常数为 ;
(2)向该平衡体系中通入1.0mol水蒸气,达到新的平衡状态时,水蒸气的物质的量为
CO的转化率为 。
工业上用CO生产燃料甲醇.一定条件下发生反应:CO(g)+2H2(g) ⇌CH3OH(g)
(1)下图表示该反应进行过程中能量的变化,曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化。该反应是 (填“吸热”或“放热”)反应,写出反应的热化学方程式 ;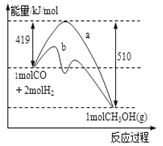
选择适宜的催化剂, (填“能”或“不能”)改变该反应的反应热。
(2)该反应平衡常数K的表达式为K= ,温度升高,平衡常数K (填“增大”、“不变”或“减小”);
(3)恒容条件下,下列措施中能使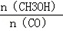 增大的有 。
增大的有 。
a.升高温度 b.充入He气 c.再充入1molCO和2molH2 d.使用催化剂.
化学反应 2A+B⇌2C;△H<0达到化学平衡时,根据以下条件改变填空:
(1)若A、B、C都是气体,且C为有色气体
①及时分离出C,平衡 移动;(填正向、逆向、不)
②使密闭容器体积增大,A的转化率 ;(填增大、减小、不变)
③如果升高温度,平衡混合物的颜色 ;(填加深、变浅、不变)
(2)若A、C为气体,B为固体;
①加压,则A的体积分数 ; ②增加B的量,A的转化率 。(填增大、减小、不变)
甲醇是一种重要的化工原料。
(1)已知:①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) △H= -1275.6 kJ·mol—1
②H2O(l)= H2O(g) △H="+" 44.0 kJ·mol—1
写出表示甲醇燃烧热的热化学方程式 。
(2)甲醇与水蒸气催化重整可获得清洁能源,具有广泛的应用前景。其反应为:
CH3OH (g)+ H2O (g) CO2(g) +3H2 (g) △H=-72.0kJ/mol
CO2(g) +3H2 (g) △H=-72.0kJ/mol
①该反应的平衡常数表达式为__________________。
②下列措施中能使平衡时n(CH3OH)/n(CO2)减小的是(双选)___________。
| A.加入催化剂 | B.恒容充入He(g),使体系压强增大 |
| C.将H2(g)从体系中分离 | D.恒容再充入1molH2O(g) |
(3)甲醇可以氧化成甲酸,在常温下用0.1000 mol/L NaOH溶液滴定20. 00 mL 0.1000 mol/L 甲酸溶液过程中,当混合液的pH=7时,所消耗的V(NaOH) _________ (填“<”或“>”或“=”) 20. 00 mL。
(8分)在一定体积的密闭容器中,进行如下化学反应:
CO2(g)+H2(g)  CO(g)+H2O(g),其化学平衡常数K和温度T的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度T的关系如下表:
| T/℃ |
700 |
800 |
830 |
1 000 |
1 200 |
| K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
回答下列问题:
(1)该反应为________反应(填“吸热”“放热”).
(2)能判断该反应是否已达化学平衡状态的依据是________.
a.容器中压强不变 b.混合气体中c(CO)不变
c.v正(H2)=v逆(H2O) d.c(CO2)=c(CO)
(3)某温度下,在2 L的密闭容器中,加入1 mol CO2和1 mol H2充分反应达平衡时,CO平衡浓度为0.25 mol/L,试判断此时的温度为________℃.
(4)若在(3)所处的温度下,在1 L的密闭容器中,加入2 mol CO2和3 mol H2充分反应达平衡时,H2的物质的量为________.
a.等于1.0 mol
b.大于1.0 mol
c.大于0.5 mol,小于1.0 mol
d.无法确定
(14分)
(1)与OH-电子数和质子数均相同的单核微粒的离子结构示意图为____________
(2)250C时,2.3 g酒精在血液中被氧气完全氧化放出66.8 kJ热量,该反应的热化学方程式为________________(3)汽车安全气囊中含MYn和红棕色金属氧化 物。M、Y为短周期元素,其最外层电子数之和等于氧原子的最外层电子数,且可发生下图的转化。
①写出元素符号:M______;Y_______.
②在2L密闭容器中,起始投入2 mol Y2和3.5 mol H2发生反应II,测得平衡时的数据如表。
若该反应ΔH <0,则T1______T2(填“ >”、“ <”或“=”);在温度T2下,若经过10 min反应达到平衡,则平均速率v(YH3)= ______,平衡常数为______ (保留两位有效数字)
③反应III的化学方程式为___________________。
设反应①Fe(s)+CO2(g)  FeO(s)+CO(g) ΔH=Q1的平衡常数为K1,反应②Fe(s)+H2O(g)
FeO(s)+CO(g) ΔH=Q1的平衡常数为K1,反应②Fe(s)+H2O(g) FeO(s)+H2(g) ΔH=Q2的平衡常数为K2,在不同温度下,K1、K2的值如下:
FeO(s)+H2(g) ΔH=Q2的平衡常数为K2,在不同温度下,K1、K2的值如下:
| 温度(T) |
K1 |
K2 |
| 973 |
1.47 |
2.38 |
| 1 173 |
2.15 |
1.67 |
(1)从上表可推断,反应①是________(填“放”或“吸”)热反应。
(2)现有反应③H2(g)+CO2(g) CO(g)+H2O(g) ΔH=Q的平衡常数为K3。
CO(g)+H2O(g) ΔH=Q的平衡常数为K3。
Ⅰ.根据反应①与②推导出K1、K2、K3的关系式K3=___ _____;可推断反应③是________(填“放”或“吸”)热反应。要使反应③在一定条件下建立的平衡右移,可采取的措施有________。
A.缩小容器体积 B.降低温度
C.使用合适的催化剂 D.设法减少CO的量
E.升高温度
Ⅱ.根据反应①与②推导出Q1、Q2、Q3的关系式Q3=________。
如下图,甲、乙、丙分别表示在不同条件下可逆反应:A(g)+B(g)  xC(g)的生成物 C在反应混合物中的百分含量(C%)和反应时间(t)的关系。
xC(g)的生成物 C在反应混合物中的百分含量(C%)和反应时间(t)的关系。
(1)若甲图中两条曲线分别代表有催化剂和无催化剂的情况,则 曲线表示无催化剂时的情况,速率:a b(填:大于、小于或等于)
(2)若乙图表示反应达到平衡后,分别在恒温恒压条件下和恒温恒容条件下向平衡混合气体中充入He气后的情况,则 曲线表示恒温恒容的情况,此时该恒温恒容中C% (填:变大、变小或不变)
(3)根据丙图可以判断该可逆反应的正反应是 反应(填:放热、吸热),计量数x的值是 ;
(4)丁图表示在某固定容器的密闭容器中,上述可逆反应达到平衡后,某物理量随着温度(T)的变化情况,根据你的理解,丁图的纵坐标可以是 ,[填:①C% ②A的转化率 ③B的转化率 ④压强 ⑤c(A) ⑥c(B)];升温平衡移动的方向为 。(填:左移或右移)
(4分)某温度下,在2 L密闭容器中,x、y、z三种物质的物质的量随时间变化曲线如图所示,
由图分析:
(1)该反应的化学方程式是_________________。
(2)3 min末,用y的浓度变化表示的反应速率V(y)为___________。
(3)反应是由_____________开始的反应。
A.正反应 B.逆反应 C.正、逆反应同时
某温度时,A+B 2C反应达到平衡状态,如果A为气体,且压强增大时,A的平衡浓度增大,则B为_________态或__________态,C为________态;如果减少或增加B的量,平衡不移动,则B是__________态;如果降温,C的平衡浓度降低,此反应的逆反应是___________热反应。
2C反应达到平衡状态,如果A为气体,且压强增大时,A的平衡浓度增大,则B为_________态或__________态,C为________态;如果减少或增加B的量,平衡不移动,则B是__________态;如果降温,C的平衡浓度降低,此反应的逆反应是___________热反应。
(1)G.H.盖斯,根据一系列事实于1840年提出“不管化学过程是一步或分数步完成,这一过程热效应相同”。换言之,若一个反应可分成几步反应完成,则各步反应的反应热总和与该反应一次发生时反应热相同。应用这个原理,解决下列问题:
已知:①C(s)+O2(g)==CO2(g) ∆H=" -393.5kJ/mol②CO(g)+1/2" O2(g)==CO2(g) ∆H= -283kJ/mol
写出C(s)与O2(g)反应生成CO(g)的热化学方程式:___________________________________
(2)反应:2A(气) B(气)+xC(气),在一定的条件下达到平衡状态,密闭容器中的压强增大P%,测得A的转化率为P%,,则x的值为_____.
B(气)+xC(气),在一定的条件下达到平衡状态,密闭容器中的压强增大P%,测得A的转化率为P%,,则x的值为_____.