下列气体中能用排水法收集的无色气体是
| A.SO2 | B.Cl2 | C.NO2 | D.NO |
某研究性学习小组同学设计了如下图制取氯气(药品:MnO2和浓盐酸)并验证其性质的实验装置。

请回答下列问题:(1)该实验中A部分的装置是 (填写装置的序号)

(2)A中发生反应一段时间后,B中的现象是 ;
整套实验装置存在的明显缺陷是 。
(3)写出D装置中发生反应的离子方程式: 。
(4)请你帮该小组同学设计一个实验,证明洗气瓶C中的 已被氧化(简述实验步骤): 。
已被氧化(简述实验步骤): 。
实验室用下图所示装置进行氨气实验。

(1)试管中发生反应的化学方程式是_________________。
(2)干燥管中盛放的干燥剂是_______________(填名称)。
(3)请在方框中画出收集一烧瓶氨气的装置。
(4)检验氨气是否收集满,可选用_________试纸,实验现象是_______________。
(5)用右图装置做喷泉实验。轻轻挤压滴管,使少量水进入烧瓶,打开止水夹,观察到的现象是 ,出现这一现象的原因是 。
下列有关物质制取或性质探究实验设计不能达到实验目的的是( )

| A.利用图1制取并收集干燥的氨气 |
| B.利用图2制取Fe(OH)2,使用煤油的目的是防止生成的Fe(OH)2被空气氧化 |
| C.利用图3制取并收集NO气体 |
| D.利用图4以医用酒精为原料制取无水乙醇 |
已知:CH3CH2OH+NaBr+H2SO4(浓) CH3CH2Br+NaHSO4+H2O.
CH3CH2Br+NaHSO4+H2O.
实验室制备溴乙烷(沸点为38.4℃)的装置和步骤如下:

①按图所示连接仪器,检查装置的气密性,然后向U形管和大烧杯里加入冰水;②在圆底烧瓶中加入10mL95%乙醇、28mL浓硫酸,然后加入研细的13g溴化钠和几粒碎瓷片;③小火加热,使其充分反应.
试回答下列问题:
(1)反应时若温度过高可看到有红棕色气体产生,该气体的化学式为 .
(2)为了更好的控制反应温度,除用图示的小火加热,更好的加热方式是 .
(3)反应结束后,U形管中粗制的溴乙烷呈棕黄色.将U形管中的混合物倒入分液漏斗中,静置,待液体分层后,分液,取 (填“上层”或“下层”)液体.为了除去其中的杂质,可选择下列试剂中的 (填序号).
| A.Na2SO3溶液 | B.H2O | C.NaOH溶液 | D.CCl4 |
(4)要进一步制得纯净的C2H5Br,可再用水洗,然后加入无水CaCl2干燥,再进行 (填操作名称).
(5)下列几项实验步骤,可用于检验溴乙烷中的溴元素,其正确的操作顺序是:取少量溴乙烷,然后 (填序号).
①加热 ②加入AgNO3溶液 ③加入稀HNO3酸化 ④加入NaOH溶液 ⑤冷却.
某化学兴趣小组利用MnO2和浓HCl 及如图装置制备Cl2。下列分析中不正确的是( )

| A.A 中可用分液漏斗代替长颈漏斗 | B.A 中缺少加热装置 |
| C.B 中盛放的NaOH 溶液可以净化Cl2 | D.D 中盛放的NaOH 溶液可以吸收尾气 |
实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )

| 选项 |
a中物质 |
b中物质 |
c中物质 |
d中物质 |
| A |
浓氨水 |
CaO |
NH3 |
H2O |
| B |
浓NaOH |
铝屑 |
H2 |
H2O |
| C |
浓盐酸 |
MnO2 |
Cl2 |
NaOH溶液 |
| D |
浓硝酸 |
Cu |
NO2 |
NaOH溶液 |
能选用右图装置正确完成的实验是
| A.用铅粒与稀硫酸制取并收集H2 |
| B.用少量MnO2和H2O2制取并收集O2 |
| C.用生石灰和浓氨水制取并收集NH3 |
| D.用浓硫酸和浓盐酸制取并收集HCl |
实验室制取下列物质的实验中未利用冷凝原理的是
| A.乙酸乙酯 | B.乙酸丁酯 | C.溴乙烷 | D.乙烯 |
实验室制备下列气体的方法可行的是( )
| |
气体 |
方法 |
| A |
氨气 |
加热氯化铵固体 |
| B |
二氧化氮 |
将铝片加到冷浓硝酸中 |
| C |
硫化氢 |
向硫化钠固体滴加浓硫酸 |
| D |
氧气 |
加热氯酸钾和二氧化锰的混合物 |
实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )
| 选项 |
a中的物质 |
b中的物质 |
c中收集的气体 |
d中的物质 |
| A |
浓氨水 |
CaO |
NH3 |
H2O |
| B |
浓硫酸 |
Na2SO3 |
SO2 |
NaOH溶液 |
| C |
稀硝酸 |
Cu |
NO2 |
H2O |
| D |
饱和食盐水 |
MnO2 |
Cl2 |
NaOH溶液 |
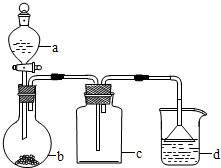
某学生在如下图所示装置中用苯和液溴制取溴苯,请根据下列实验步骤完成有关问题:
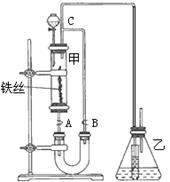
(1)第一步,在分液漏斗中依次加入10 mL苯和5 mL液溴,使之混合均匀,此时观察到溴溶于苯,不反应,溶液呈深棕红色。
第二步,打开分液漏斗活塞,将苯、溴混合液按一定速率逐滴加入玻璃管甲中的铁丝上,观察到的现象是剧烈反应,玻璃管甲和导管C中有橙红色蒸气。从上述两步观察到的现象差异,可得出的结论是______________________。
(2)第三步,几分钟后,打开胶皮管夹A和B,使反应混合液流入U形管中,打开管夹B的原因是______________________;然后通过分液漏斗向U形管中加入适量的NaOH溶液,目的是(用化学方程式表示)_ 。
(3)第四步,关闭胶皮管A和B,连同A和B一起取下U形管,用力振荡并静置后,观察到无色的溴苯,它在U形管中液体的_ (填“上”或“下”)层。
(4)要证明上述溴跟苯的反应是取代而不是加成反应,请根据装置乙的作用完成下列各题:
小试管内的液体是__________(填名称)。
锥形瓶内的液体是__________(填名称)。
反应后,向锥形瓶内滴加试剂__________(填名称)溶液,作用是 。
(5)写出上述苯跟溴反应的化学方程式__________________________。
菠菜是一种富含草酸(乙二酸)的绿色蔬菜,但食用时要避免和豆腐同时食用,因为二者容易产生难溶于水的物质而在体内生成结石。草酸也是有机化工中的重要原料,广泛应用于化工生产中。为探究草酸的某些性质,某中学化学兴趣小组查阅了一些资料如下:
| 物质 |
结构 |
某些性质 |
| 草酸 |
分子式:H2C2O4·2H2O |
无色,易溶于水;其钠盐和钾盐易溶于水,钙盐难溶于水 |
| 结构简式:HOOC-COOH |
熔点:101℃;升华温度:125℃;170℃以上分解 |
回答下列问题:
(1)甲组同学按照如图所示的装置,通过实验检验草酸晶体的分解产物。
装置C中可观察到的现象是①导管口有气泡出现 ②石灰水变浑浊,由此可知草酸晶体分解的产物有__________。装置B的主要作用是_______________。若无此装置C中可能发生的反应的化学方程式为___________________。
(2)乙组同学认为草酸晶体分解的产物中含有CO,为了进行验证,选用甲组实验中的装置A、B和下图所示的部分装置进行实验。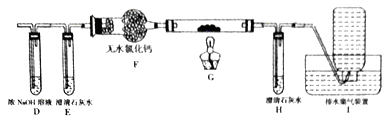
①乙组的实验装置中,装置E和H中的澄清石灰水的作用分别是_________和__________;装置G反应管中盛有的固体物质是___________;I中集气瓶收集到的气体主要是_______________。
②能证明草酸晶体分解产物中有CO的现象是____________________________。