25℃,a L 0.1000 mol/L CH3COOH溶液与b L 0.1000 mol/L NaOH溶液混合,下列说法正确的是
| A.若a>b,则pH一定小于7 |
| B.若a<b,则一定存在:n(OH-)-n(H+)>0.1(b-a) |
| C.c(Na+)>c(CH3COO-)>c(OH-)>c(H+),则a≤b |
| D.若pH =7,则a>b,且 c(Na+)=c(CH3COO-)+c(CH3COOH) |
下列有关化学实验事实描述正确的是( )
A.Na2CO3溶液呈碱性的原因是:CO32-+2H2O H2CO3+2OH- H2CO3+2OH- |
| B.用NaAlO2溶液可以鉴别Na2CO3溶液和NaHCO3溶液 |
| C.有NH4+浓度相等的NH4Cl、CH3COONH4和NH4Al(SO4)2三种溶液,测得相同温度下溶质浓度最大的是NH4Al(SO4)2溶液 |
| D.AlCl3溶液和NaAlO2溶液加热蒸干所得主要成分都是Al(OH)3固体 |
下列叙述不正确的是
| A.NH4Cl溶液加水稀释后,恢复至原温度,pH和KW均增大 |
| B.0.1 mol/L CH3COONa溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| C.pH=4的CH3COOH溶液和pH=4的NH4Cl溶液中,c(H+)相等 |
| D.在NaHCO3溶液中:c(OH—)+c(CO32—)=c(H+)+c(H2CO3) |
下列溶液中有关物质的量浓度关系和计算不正确的是
A.c(NH4+)相等的(NH4)2SO4、(NH4)2Fe(SO4)2和NH4Cl溶液中,溶质浓度大小关系是:c[(NH4)2Fe(SO4)2] < c[(NH4)2SO4] < c(NH4Cl)
B.已知25°C时 ,则在0.1mol·L-1AlCl3溶液中,Ag+的物质的量浓度最大可达到
,则在0.1mol·L-1AlCl3溶液中,Ag+的物质的量浓度最大可达到 mol·L-1
mol·L-1
C.0.2mol·L-1 HCl溶液与等体积0.05 mol·L-1 Ba(OH)2溶液混合后,溶液的pH=1
D.室温下,0.1mol·L-1NaHA溶液的pH=4,则有C(HA-) >C(H+)>C(A2-)>C(H2A)
室温下,向含有溶质为0.10mol的下列溶液中通入0.10mol的相应的气体(通入气体对溶液体积的影响可忽略),溶液中部分微粒的物质的量浓度关系正确的是 ( )
| A.向NH4HCO3溶液中通入CO2:c(NH4+)=c(HCO3-)+c(CO32-) |
| B.向Na2SO3溶液通入SO2:c(Na+)= [c(SO32-)+c(HSO3-)+c(H2SO3)] |
| C.向CH3COONa溶液中通入HCl:c(Na+)>c(CH3COOH)=c(Cl-) |
| D.向NH4Cl溶液中通入NH3:c(NH4+)< c(Cl-) |
常温下,用0.1000 mol·L NaOH溶液滴定 20.00mL0.1000 mol·L
NaOH溶液滴定 20.00mL0.1000 mol·L
 溶液所得滴定曲线如右图。
溶液所得滴定曲线如右图。
下列说法正确的是
A.点①所示溶液中: |
B.点②所示溶液中: |
C.点③所示溶液中: |
D.滴定过程中可能出现: |
经测定某溶液中离子只有Na+、Ac—、H+、OH—四种,且离子浓度大小的排列顺序为:c(Ac—)>c(Na+)>c(H+)>c(OH—),则不可能的情形是
| A.由pH=3的HAc与pH=11的NaOH溶液等体积混合而成 |
| B.由0.2 mol/L HAc溶液与0.1 mol/L NaOH溶液等体积混合而成 |
| C.由0.1 mol/L HAc溶液与等物质的量浓度等体积的NaOH溶液混合而成 |
| D.向上述溶液中加入适量NaOH,可能使溶液中离子浓度大小改变为: c(Ac—) > c(Na+) > c(OH—) > c(H+) |
用0.1mol·L—1的盐酸滴定0.1mol·L—1的氨水,在滴定过程中不可能出现的结果是
| A.c(NH4+)>c(Cl-),c(OH-)>c(H+) |
| B.c(Cl-)>c(NH4+),c(H+)>c(OH-) |
| C.c(NH4+)=c(Cl-),c(OH-)=c(H+) |
| D.c(Cl-)>c(NH4+),c(OH-)>c(H+) |
0.02mol·L—1的HCN溶液与0.02mol·L—1的NaCN溶液等体积混合,已知混合溶液中C(CN-)<C(Na+),则下列关系中,正确的是:
| A.C(Na+)>C(CN-)>C( H+)>C(OH-) |
| B.C(HCN)+C (CN-)=0.04mol·L-1 |
| C.C(CN-)>C(HCN) |
| D.C(Na+)+C(H+)= C(CN-)+C(OH-) |
用物质的量都是0.1mol的HCN和NaCN混合后配成1L溶液,已知溶液中的c(CN-)<c(Na+),下列关系式正确的是( )
| A.c(H+)>c(OH-) | B.c(HCN)<c(CN-) |
| C.c(CN-)+c(OH-)=0.1mol·L-1 | D.c(HCN)+c(CN-) =0.2mol·L—11 |
下列说法中正确的是:(均在常温下)( )
①pH=1的强酸溶液,加水稀释后,溶液中所有离子的浓度均降低。
②pH=2的盐酸和pH=1的醋酸,c(H+) 之比为2∶1。
③在Na2CO3和NaHCO3溶液中均存在下列关系c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-)
④已知醋酸电离平衡常数为Ka;醋酸根水解常数为Kh;水的离子积为Kw;
则三者关系为:Ka·Kh=Kw
⑤甲、乙两溶液都是强电解质,已知甲溶液的pH是乙溶液pH的两倍,则甲、乙两溶液等
体积混合,混合液pH可能等于7
| A.①②③ | B.③④⑤ | C.②④⑤ | D.①③⑤ |
常温下,测得某溶液NaHX的pH >7,该溶液中有关浓度关系式正确的是
| A.c(Na+) > c(H+)+c(X2-) |
| B.c(Na+)=c(H2X)+c(HX-)+c(X2-) |
| C.c(X2-)> c(H2X) |
| D.c(Na+)+ c(H+)=c(OH-)+c(HX-)+c(X2-) |
0.1 mol•L-1 KHS溶液中下列表达式不正确的是( )
| A.c(K +)+c(H+)= c(OH-)+ c(HS-)+2 c(S2-) | B.c(K+)> c(HS-)> c(OH-)> c(S2-)> c(H+) |
| C.c(HS-)+ c(S2-)+ c(H2S)=" 0.1" mol•L-1 | D.c(K+)> c(HS-)> c(OH-)> c(H2S)> c (H+) |
用酒精灯加热下列溶液,蒸干后灼烧,所得固体质量最大的是( )
| A.20 mL 2 mol/L FeCl3溶液 | B.40 mL 1 mol/L NaHCO3溶液 |
| C.20 mL 1 mol/L Na2SO3溶液 | D.40 mL 2 mol/L NH4HCO3溶液 |
下列溶液中离子浓度关系的表示正确的是( )
A.NaHCO3溶液中:c(H+)+c(Na+)=c(OH-)+c(CO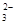 )+c(HCO )+c(HCO ) ) |
| B.pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合后的溶液中:c(OH-)>c(H+)+c(CH3COO-) |
C.0.1 mol·L-1的NH4Cl溶液中:c(Cl-)>c(H+)>c(NH )>c(OH-) )>c(OH-) |
| D.物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合后的溶液中: |
2c(Na+)=c(CH3COOH)+c(CH3COO-)